1 . 实验是探究物质性质的重要方法,下列操作中,实验现象与得出的结论相一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 比较HClO和CH3COOH的酸性强弱 | 用pH计测定NaClO和CH3COONa的pH值,测得pH(NaClO)>pH(CH3COONa) | 酸性:HClO>CH3COOH |
| B | 验证反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 | 向2mL 0.1mol/L FeCl3溶液加入几滴0.1mol/L KI溶液,充分反应。取反应后试样,滴加淀粉溶液,溶液变为蓝色;另取反应后试样,加入KSCN溶液,溶液变成血红色 | 反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 |
| C | 判断 (AgCl)与 (AgCl)与 (AgI)的大小 (AgI)的大小 | 向等浓度的NaCl、NaI的混合溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| D | 判断某 溶液样品中是否含有 溶液样品中是否含有 | 向某 溶液样品中加入硫酸酸化的 溶液样品中加入硫酸酸化的 溶液,紫色褪去 溶液,紫色褪去 | 该样品中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 实验小组用如图装置探究Cl2、Fe3+、I2的氧化性强弱(夹持装置和加热装置已省略,气密性已检验)。
已知:I2遇淀粉溶液变蓝

实验过程:
I.打开弹簧夹K1和K2,通入一段时间N2,再将导管插入B中,继续通入N2一段时间,然后夹紧K1;
Ⅱ.打开活塞a,滴加一定量浓盐酸后关闭活塞a,给A加热;
Ⅲ.当B中的溶液变为黄色时,停止加热,夹紧K2;
IV.打开活塞b,将少量B中溶液滴入C中,关闭活塞b。
(1)操作I中通入一段时间N2的目的是
(2)浸有NaOH溶液的棉花的作用是
(3)B中溶液变黄说明氧化性Cl2>Fe3+,反应的离子方程式是
(4)为探究Fe3+和I2的氧化性强弱,甲、乙、丙三位同学分别完成了上述实验,并检测B中黄色溶液和C中混合溶液中的部分微粒,结果如表所示(忽略空气中O2的影响)。
B中部分微粒 | C中部分微粒 | |
甲 | 既有Fe3+又有Fe2+ | 有I2 |
乙 | 有Fe3+无Fe2+ | 有I2 |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
①检验B中黄色溶液中含有Fe3+的试剂是
②进一步检验IL的实验操作及现象是
③能证明该实验条件下氧化性Fe3+>I2的有
不能证明的请说明理由
④已知碘原子的原子结构示意图为 ,从原子结构角度解释碘原子的得电子能力弱于氯原子的原因
,从原子结构角度解释碘原子的得电子能力弱于氯原子的原因
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组在研究“铁及其化合物性质”时,发现向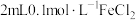 溶液中滴加2滴
溶液中滴加2滴 溶液,无明显现象,再滴加
溶液,无明显现象,再滴加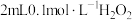 溶液溶液(
溶液溶液( 约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
(1)溶液先变红的原因是_____ (用两个离子方程式表示)。
(2)同学们对溶液褪色的原因提出了不同的看法并进行实验:
I.甲同学认为是 被
被 还原。
还原。
取褪色后溶液,滴加 溶液,无明显现象,证明甲同学观点不正确。
溶液,无明显现象,证明甲同学观点不正确。
Ⅱ.乙同学认为是 被氧化。
被氧化。
取褪色后溶液,滴加 溶液,出现红色。
溶液,出现红色。
根据上述实验现象,同学们认为溶液褪色的原因可能有两种:
乙同学认为 被
被 氧化。
氧化。
丙同学认为_____ 。
为了探究溶液褪色的原因究竞是上述的哪一种,该兴趣小组进行了如下实验。
向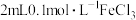 溶液中滴加2滴
溶液中滴加2滴 溶液,后通入
溶液,后通入 。发现溶液
。发现溶液_____ ,证明溶液褪色的原因不是乙同学认为的原因,而是丙同学认为的原因。
(3)该兴趣小组通过查阅资料,发现 可以被氧化成
可以被氧化成 和两种可直接排放到空气中的气体。
和两种可直接排放到空气中的气体。
设计实验方案验证褪色后的溶液中存在 :
:_____ 。
(4)写出上述实验中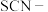 被氧化的离子方程式:
被氧化的离子方程式:_____ 。
(5)根据题目所给信息及实验现象推断物质还原性强弱:
_____ 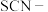 (填“>”或“<”),理由:
(填“>”或“<”),理由:_____ 。
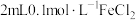 溶液中滴加2滴
溶液中滴加2滴 溶液,无明显现象,再滴加
溶液,无明显现象,再滴加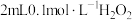 溶液溶液(
溶液溶液( 约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:(1)溶液先变红的原因是
(2)同学们对溶液褪色的原因提出了不同的看法并进行实验:
I.甲同学认为是
 被
被 还原。
还原。取褪色后溶液,滴加
 溶液,无明显现象,证明甲同学观点不正确。
溶液,无明显现象,证明甲同学观点不正确。Ⅱ.乙同学认为是
 被氧化。
被氧化。取褪色后溶液,滴加
 溶液,出现红色。
溶液,出现红色。根据上述实验现象,同学们认为溶液褪色的原因可能有两种:
乙同学认为
 被
被 氧化。
氧化。丙同学认为
为了探究溶液褪色的原因究竞是上述的哪一种,该兴趣小组进行了如下实验。
向
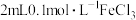 溶液中滴加2滴
溶液中滴加2滴 溶液,后通入
溶液,后通入 。发现溶液
。发现溶液(3)该兴趣小组通过查阅资料,发现
 可以被氧化成
可以被氧化成 和两种可直接排放到空气中的气体。
和两种可直接排放到空气中的气体。设计实验方案验证褪色后的溶液中存在
 :
:(4)写出上述实验中
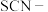 被氧化的离子方程式:
被氧化的离子方程式:(5)根据题目所给信息及实验现象推断物质还原性强弱:

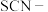 (填“>”或“<”),理由:
(填“>”或“<”),理由:
您最近一年使用:0次
名校
4 . 下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
 | 向 的 的 溶液中加入等体积浓 溶液中加入等体积浓 溶液,振荡 溶液,振荡 | 分层,下层由紫红色变为浅粉红色,上层呈棕黄色 |  在浓 在浓 溶液中的溶解能力大于在 溶液中的溶解能力大于在 的溶解能力 的溶解能力 |
 | 向 溶液中滴加 溶液中滴加 溶液,再加入少量 溶液,再加入少量 固体 固体 | 溶液先变成血红色后无明显变化 |  与 与 反应不可逆 反应不可逆 |
| C | 向 溶液中先滴加4滴 溶液中先滴加4滴 溶液,再滴加4滴 溶液,再滴加4滴 溶液 溶液 | 先产生白色沉淀,再产生黄色沉淀 |  转化为 转化为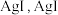 溶解度小于 溶解度小于 溶解度 溶解度 |
 | 向 溶液中滴加 溶液中滴加 溶液 溶液 | 出现黄色沉淀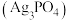 |  发生了水解反应 发生了水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 我国锰矿资源主要为贫碳酸锰矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。 ,
, 。
。
(1) 中锰元素的价态有+2价和+3价,则下列表示
中锰元素的价态有+2价和+3价,则下列表示 组成的式子正确的是___________(填标号)。
组成的式子正确的是___________(填标号)。
(2)“滤渣1”的主要成分是___________ (填化学式)。
(3)“氧化”的目的是将 转化为
转化为 ,写出发生反应的离子方程式
,写出发生反应的离子方程式___________ ,检测 是否完全氧化的试剂是
是否完全氧化的试剂是___________ (写试剂名称)。
(4)“除钙镁”后的滤液中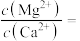
___________ 。
(5)“碳化”过程需要加热,但温度不能太高,试分析温度不能太高的原因___________ 。
(6)“焙烧”过程中随温度不同生成的锰的氧化物也不同。图中A点对应的氧化物是___________ ,为了获得 ,需要加热到
,需要加热到___________  (已知:A、B、C三点对应的物质均为纯净氧化物)。
(已知:A、B、C三点对应的物质均为纯净氧化物)。
 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。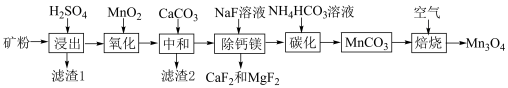
 ,
, 。
。(1)
 中锰元素的价态有+2价和+3价,则下列表示
中锰元素的价态有+2价和+3价,则下列表示 组成的式子正确的是___________(填标号)。
组成的式子正确的是___________(填标号)。A.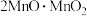 | B.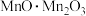 | C.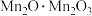 | D. |
(2)“滤渣1”的主要成分是
(3)“氧化”的目的是将
 转化为
转化为 ,写出发生反应的离子方程式
,写出发生反应的离子方程式 是否完全氧化的试剂是
是否完全氧化的试剂是(4)“除钙镁”后的滤液中
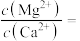
(5)“碳化”过程需要加热,但温度不能太高,试分析温度不能太高的原因
(6)“焙烧”过程中随温度不同生成的锰的氧化物也不同。图中A点对应的氧化物是
 ,需要加热到
,需要加热到 (已知:A、B、C三点对应的物质均为纯净氧化物)。
(已知:A、B、C三点对应的物质均为纯净氧化物)。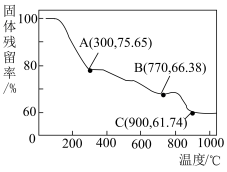
您最近一年使用:0次
2024-03-08更新
|
208次组卷
|
4卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学甘肃省张掖市某重点校2023-2024学年高三下学期模拟考化学试题(已下线)大题预测卷(黑龙江、吉林专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)陕西省西安工业大学附属中学2023-2024学年高三下学期3月月考理科综合试题-高中化学
名校
解题方法
6 . 蛋黄含多种微量元素、营养丰富,某实验小组设计实验检验蛋黄中的铁元素并测定其含量:
(一)蛋黄中铁元素的检验

(1)蛋黄灰化时,无需选择下列仪器中的_______ (填代号)。
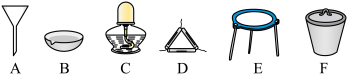
(2)实验中加入氯水的目的是_______ ,写出①涉及反应的离子方程式_______ 。
(3)由以上实验做出如下猜测,其中合理的是_______(填代号)。
(二)蛋黄中铁元素的含量测定
实验步骤如下:
Ⅰ.取5.000g蛋黄,灰化。向灰分中加入盐酸,微热10min,过滤,并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并,加入过量盐酸羟胺(还原剂);
Ⅱ.取50mL_______,将全部溶液注入该容器中,加蒸馏水定容;
Ⅲ.甲同学使用酸性高锰酸钾做氧化剂,利用其消耗量计算得到试样铁的浓度为9.5×10-4mmol/mL。乙同学利用分光光度法(利用有色物质对光的吸收测定物质浓度的方法)测得铁的浓度为2×10-4mmol/mL。
请根据上述实验,回答:
(4)步骤Ⅱ横线处的仪器为_______ 。
(5)步骤Ⅱ定容操作若俯视容量瓶刻度线,会造成测算所得蛋黄样品含铁量_______ (填“偏高”或“偏低”或“无影响”);
(6)根据乙同学实验数据计算蛋黄中铁元素的含量为_______ mg/100g。
(一)蛋黄中铁元素的检验

(1)蛋黄灰化时,无需选择下列仪器中的

(2)实验中加入氯水的目的是
(3)由以上实验做出如下猜测,其中合理的是_______(填代号)。
| A.蛋黄中几乎不含铁元素 |
| B.蛋黄中的铁元素很难用蒸馏水直接溶出 |
| C.仅用盐酸无法溶出蛋黄灰分中的铁元素 |
| D.灰化的目的是将蛋黄中的铁元素氧化 |
(二)蛋黄中铁元素的含量测定
实验步骤如下:
Ⅰ.取5.000g蛋黄,灰化。向灰分中加入盐酸,微热10min,过滤,并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并,加入过量盐酸羟胺(还原剂);
Ⅱ.取50mL_______,将全部溶液注入该容器中,加蒸馏水定容;
Ⅲ.甲同学使用酸性高锰酸钾做氧化剂,利用其消耗量计算得到试样铁的浓度为9.5×10-4mmol/mL。乙同学利用分光光度法(利用有色物质对光的吸收测定物质浓度的方法)测得铁的浓度为2×10-4mmol/mL。
请根据上述实验,回答:
(4)步骤Ⅱ横线处的仪器为
(5)步骤Ⅱ定容操作若俯视容量瓶刻度线,会造成测算所得蛋黄样品含铁量
(6)根据乙同学实验数据计算蛋黄中铁元素的含量为
您最近一年使用:0次
名校
解题方法
7 .  溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓
溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓 得溶液 b,溶液b较溶液 a黄色加深。已知:
得溶液 b,溶液b较溶液 a黄色加深。已知: (黄色);浓度较小时
(黄色);浓度较小时  (用
(用 表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
 溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓
溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓 得溶液 b,溶液b较溶液 a黄色加深。已知:
得溶液 b,溶液b较溶液 a黄色加深。已知: (黄色);浓度较小时
(黄色);浓度较小时  (用
(用 表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
表示)几乎无色。取溶液进行如下实验,对现象分析错误的是A.测溶液 a的  约为1.3,证明 约为1.3,证明  发生了水解 发生了水解 |
B.向 b中加入  后,会产生白色沉淀 后,会产生白色沉淀 |
C.向 b中滴入  溶液变血红色,说明 溶液变血红色,说明  的配位键稳定性大于 的配位键稳定性大于  |
D.将溶液 a稀释,颜色变浅,主要是因为  浓度降低导致 浓度降低导致 |
您最近一年使用:0次
2024-01-31更新
|
204次组卷
|
4卷引用:黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期开学验收考试化学
名校
8 . 化学小组探究Cu与Fe2(SO4)3溶液的反应,实验如下:
已知:经检验白色沉淀为CuSCN。
(1)实验i中发生反应的离子方程式为___________
(2)实验i中检测到Fe3+,依据的实验现象是___________
(3)对实验ii中Fe3+产生的原因作如下假设:
假设1:Cu与Fe2(SO4)3的反应是一个可逆反应
假设2:溶液中的Fe2+被___________ 氧化
假设3:在实验ii的条件下,Fe2+被Cu2+氧化
①将假设2补充完整
②通过查找___________ 数据,可定量判断Cu与Fe2(SO4)3的反应是否为可逆反应。
(4)设计实验验证假设。
资料:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂氧化性增强,还原反应越易发生。
①假设1不成立的实验证据是___________
②实验iii的目的是___________
③溶液a是___________
④结合电极反应以及资料,解释实验ii中Fe3+产生的原因___________
| 序号 | 实验方案 | 实验现象 |
| 实验i |  | 振荡试管,观察到溶液变为蓝色,待反应充分后,试管底部有 Cu粉剩余。 |
| 实验ii | 取实验i中的上层清液,向其中滴加0.1mol·L-1 KSCN溶液 | 溶液局部变红,同时产生白色沉淀,振荡试管,红色消失。 |
(1)实验i中发生反应的离子方程式为
(2)实验i中检测到Fe3+,依据的实验现象是
(3)对实验ii中Fe3+产生的原因作如下假设:
假设1:Cu与Fe2(SO4)3的反应是一个可逆反应
假设2:溶液中的Fe2+被
假设3:在实验ii的条件下,Fe2+被Cu2+氧化
①将假设2补充完整
②通过查找
(4)设计实验验证假设。
资料:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂氧化性增强,还原反应越易发生。
| 序号 | 实验iii | 实验iv |
| 方案 | 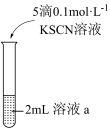 | 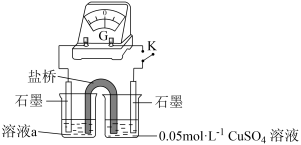 |
| 现象 | 放置较长时间,溶液颜色不变红 | 闭合开关K,电流计指针不动,向右侧CuSO4溶液中滴加0.1mol·L-1KSCN,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol·L-1KSCN,溶液变红。 |
②实验iii的目的是
③溶液a是
④结合电极反应以及资料,解释实验ii中Fe3+产生的原因
您最近一年使用:0次
名校
解题方法
9 . 聚合硫酸铁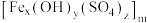 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁,配成 溶液。
溶液。
②准确量取①中溶液 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。
③准确量取①中溶液 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。
该聚合硫酸铁组成中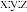 为
为
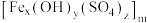 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁,配成
 溶液。
溶液。②准确量取①中溶液
 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。③准确量取①中溶液
 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。该聚合硫酸铁组成中
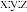 为
为A. | B. | C.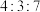 | D. |
您最近一年使用:0次
2023-12-30更新
|
165次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期开学考试化学试题
10 . 探究pH对 溶液的配制和保存的影响。
溶液的配制和保存的影响。
I. 溶液的配制
溶液的配制
将 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
(1)用离子方程式表示①中溶液显酸性的主要原因___________ 。
(2)甲同学认为①溶液中一定有+3价铁。他用激光笔照射“溶液”,观察到光路;向含有KSCN的①溶液中滴入试剂a,溶液变红,说明其推断正确。试剂a是___________ 。
II. 溶液的保存
溶液的保存
将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
(3)①中的浑浊主要是FeOOH,用离子方程式表示其生成过程___________ 。
(4)该实验的初步结论:保存 溶液的最佳pH是
溶液的最佳pH是____________ 。
(5)进一步探究pH对 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:

i.向左池滴加浓硫酸至 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;
ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因___________ 。
b.依据实验i和ii推断:③比②中 更易变质的原因是
更易变质的原因是___________ 。
c.按上述原理进行实验,证实①中 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,___________ 。
 溶液的配制和保存的影响。
溶液的配制和保存的影响。I.
 溶液的配制
溶液的配制将
 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:| 编号 | 溶剂 | 溶液性状 | |
| ① | 蒸馏水 | 浅黄色澄清溶液 |  ;滴加1mol/LKSCN溶液无明显变化 ;滴加1mol/LKSCN溶液无明显变化 |
| ② |  | 无色澄清溶液 |  ;滴加1mol/LKSCN溶液微微变红 ;滴加1mol/LKSCN溶液微微变红 |
| ③ |  | 无色澄清溶液 | 滴加1mol/LKSCN溶液微微变红 |
(2)甲同学认为①溶液中一定有+3价铁。他用激光笔照射“溶液”,观察到光路;向含有KSCN的①溶液中滴入试剂a,溶液变红,说明其推断正确。试剂a是
II.
 溶液的保存
溶液的保存将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
| 编号 | 溶液性状 | |
| ① | 橙色浑浊 | 用 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 |
| ② | 无色溶液 | 滴加1mol/L的KSCN溶液后显浅红色 |
| ③ | 无色溶液 | 滴加1mol/L的KSCN溶液后显红色,颜色比②略深 |
(4)该实验的初步结论:保存
 溶液的最佳pH是
溶液的最佳pH是(5)进一步探究pH对
 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
i.向左池滴加浓硫酸至
 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因
b.依据实验i和ii推断:③比②中
 更易变质的原因是
更易变质的原因是c.按上述原理进行实验,证实①中
 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
您最近一年使用:0次



