1 . 下列有关实验、现象及结论等叙述正确的个数有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近半年使用:0次
2024-04-19更新
|
273次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高一下学期开学考试化学试题
2 . 能证明溶液中含有 的试剂是
的试剂是
 的试剂是
的试剂是| A.铜粉 | B. 溶液 溶液 | C.稀硫酸 | D.酚酞溶液 |
您最近半年使用:0次
名校
3 . KSCN是实验室常用的化学试剂。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。
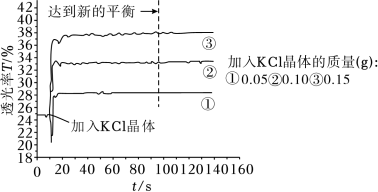
已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl- [FeCl4]-(黄色)。
[FeCl4]-(黄色)。
①采用FeCl3稀溶液是为了避免_______ (填离子符号)的颜色对实验干扰。
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度_______ (填“增大”“减小”或“不变”),从平衡移动的角度分析可能的原因_______ 。
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O +I2=S4O
+I2=S4O +2I-;
+2I-;
ii.I2+I- I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;
iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为_______ ;根据信息预测最终测定的结果将_______ (填“偏大”“偏小”或“无影响”)。
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式_______ ;到达滴定终点时消耗标准液20.00mL,样品中铜元素质量分数为_______ ,滴定后仍存在少量CuI沉淀,测得溶液中c(I-)=0.2mol•L-1,则c(SCN-)=_______ 。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。

已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl-
 [FeCl4]-(黄色)。
[FeCl4]-(黄色)。①采用FeCl3稀溶液是为了避免
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O
 +I2=S4O
+I2=S4O +2I-;
+2I-;ii.I2+I-
 I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式
您最近半年使用:0次
2024-04-05更新
|
49次组卷
|
3卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
4 . 某班同学用如下实验探究Fe2+与Fe3+的转化,回答下列问题,
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为_______ 。
②对比三组实验,说明加入蒸馏水后沉淀的产生与_______ 有关。
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为_______ 。
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.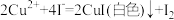 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为_______ 。
(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性, (棕色):
(棕色):
⑤使用的FeSO4溶液中存在少量铁屑,其目的是_______ 。
⑥实验中产生NO的原因为_______ (用离子方程式表示)。
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为
②对比三组实验,说明加入蒸馏水后沉淀的产生与
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.
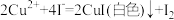 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性,
 (棕色):
(棕色):⑤使用的FeSO4溶液中存在少量铁屑,其目的是
⑥实验中产生NO的原因为
您最近半年使用:0次
名校
解题方法
5 . 菠菜中富含铁元素,用下列步骤完成铁元素的检验,各步选用的实验仪器不需要的是
| |
|
|
| A.将菠菜剪碎后研磨 | B.用蒸馏水溶解 | C.过滤得到滤液 | D.检验滤液中的Fe3+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-03更新
|
43次组卷
|
2卷引用:湖南省衡阳市祁东县成章高级中学2023-2024学年高一下学期入学考试化学试卷
名校
6 . 铁是人体必需的微量元素之一。黑木耳中的含铁量较高,为检验和测定干黑木耳样品中的铁元素,设计实验如下。回答下列问题:
Ⅰ.铁元素的检验

(1)“操作”是指________ ;上述流程中需要用到的仪器有托盘天平、烧杯、玻璃棒、酒精灯、漏斗,还有下图中的________ (填写仪器名称)。

(2)检验待测液中是否含有 、
、
Ⅱ.铁元素含量的测定
利用 标准溶液测定干黑木耳样品中铁元素的含量
标准溶液测定干黑木耳样品中铁元素的含量
步骤Ⅰ:取 待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀 溶液,用
溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液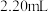 。
。
(3)步骤Ⅰ加入过量铜粉的目的是_________________________________ 。
(4)步骤Ⅱ滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_____________________ 。
(5)用 标准溶液滴定至终点的标志是:
标准溶液滴定至终点的标志是:___________ 。
(6)黑木耳中铁的含量为________ mg/100g(即每100g黑木耳中含铁元素质量)。
(7)若步骤Ⅰ过滤后未洗涤将使测定结果________ (填“偏大”或“偏小”或“无影响”)。
Ⅰ.铁元素的检验

(1)“操作”是指

(2)检验待测液中是否含有
 、
、
| 检验试剂 | 现象 | 结论 |
| KSCN溶液 | 溶液变为红色 | 滤液中含有 |
| ① | ② | 滤液中含有 |
Ⅱ.铁元素含量的测定
利用
 标准溶液测定干黑木耳样品中铁元素的含量
标准溶液测定干黑木耳样品中铁元素的含量步骤Ⅰ:取
 待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀
 溶液,用
溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液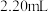 。
。(3)步骤Ⅰ加入过量铜粉的目的是
(4)步骤Ⅱ滴加
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(5)用
 标准溶液滴定至终点的标志是:
标准溶液滴定至终点的标志是:(6)黑木耳中铁的含量为
(7)若步骤Ⅰ过滤后未洗涤将使测定结果
您最近半年使用:0次
2024-04-03更新
|
134次组卷
|
2卷引用:天津市宁河区芦台第一中学2024届高三下学期适应性模拟训练(3月)化学试题
名校
7 . 下列实验目的、方案设计和现象、结论都正确的是
| 选项 | 实验目的 | 方案设计和现象 | 结论 |
| A | 验证浓硫酸的性质 | 将浓硫酸滴入蔗糖中并搅拌,得到黑色蓬松的固体,并产生刺激性气味的气体 | 浓硫酸具有强氧化性和脱水性 |
| B | 探究钠在空气中久置后所得固体成分 | 取少量固体,加入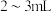 蒸馏水,有气体产生 蒸馏水,有气体产生 | 固体中一定含 |
| C | 检验某溶液中是否含有 | 取少量待检液于试管中,滴加新制氯水后滴加 溶液,溶液变为红色 溶液,溶液变为红色 | 该溶液含有 |
| D | 检验 和浓盐酸反应后是否有酸剩余 和浓盐酸反应后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入稀硝酸、 溶液 溶液 | 产生大量白色沉淀,则盐酸有剩余 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-03更新
|
245次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高一下学期入学考试化学试题
名校
8 . 下列实验的操作、现象和所得结论都正确的是
| 实验操作 | 现象 | 实验结论 | |
| A | 红热的铁与水蒸气反应后的固体物质,用稀硫酸溶解,滴入几滴KSCN溶液 | 未显红色 | 固体物质中不含+3价铁元素 |
| B | 向某溶液先滴加硝酸酸化,再滴加 溶液 溶液 | 出现白色沉淀 | 原溶液中一定含有 |
| C | 将纯Al片与纯Mg片用导线连接,浸入到氢氧化钠溶液中 | Al片表面产生大量气泡 | 金属性:Mg>Al |
| D | 某溶液中先滴加 溶液,再加足量稀HNO3 溶液,再加足量稀HNO3 | 滴加 溶液时,出现白色沉淀,再加足量稀HNO3,沉淀不溶解 溶液时,出现白色沉淀,再加足量稀HNO3,沉淀不溶解 | 溶液中含有Cl- |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . 明矾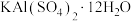 在日常生活中用途非常广泛。用废铝灰(含Al、
在日常生活中用途非常广泛。用废铝灰(含Al、 、Fe、
、Fe、 、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
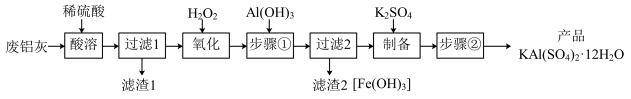
已知: 开始沉淀到沉淀完全时溶液的pH为1.9~3.7;
开始沉淀到沉淀完全时溶液的pH为1.9~3.7; 开始沉淀到完全沉淀时溶液的pH为5.5~8.5。
开始沉淀到完全沉淀时溶液的pH为5.5~8.5。
(1)“酸溶”时, 溶解的离子方程式为
溶解的离子方程式为_____ 。
(2)“氧化”时,发生反应的离子方程式为_____ 。
(3)“步骤①”调节pH约为3.7的目的是_____ ;检验“过滤2”滤液中是否含 可用试剂
可用试剂_____ 。
(4)“步骤②”包含的操作有_____ 、_____ 、过滤、洗涤及干燥。
(5)已知废铝灰中铝元素的含量为a%,则mkg废铝灰理论上可制得明矾_____ kg。
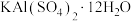 在日常生活中用途非常广泛。用废铝灰(含Al、
在日常生活中用途非常广泛。用废铝灰(含Al、 、Fe、
、Fe、 、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
已知:
 开始沉淀到沉淀完全时溶液的pH为1.9~3.7;
开始沉淀到沉淀完全时溶液的pH为1.9~3.7; 开始沉淀到完全沉淀时溶液的pH为5.5~8.5。
开始沉淀到完全沉淀时溶液的pH为5.5~8.5。(1)“酸溶”时,
 溶解的离子方程式为
溶解的离子方程式为(2)“氧化”时,发生反应的离子方程式为
(3)“步骤①”调节pH约为3.7的目的是
 可用试剂
可用试剂(4)“步骤②”包含的操作有
(5)已知废铝灰中铝元素的含量为a%,则mkg废铝灰理论上可制得明矾
您最近半年使用:0次
名校
10 . 硫脲 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:① ;
;
②25℃时硫脲溶解度为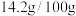 水;
水;
③实验室常用FeS与稀 在常温下制
在常温下制 。
。
(1)盛放石灰乳的仪器的名称是_______ ,B的加热方式宜选择_______ (填标号)。
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现_______ (填实验现象)时表明B中生成了 。
。
(3)实验发现,硫脲产率与投料比 的关系如图所示。
的关系如图所示。
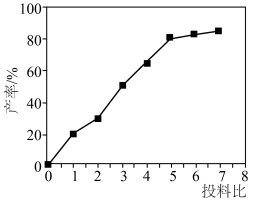
最佳投料比为_______ 。
实验(二):探究硫脲的性质。
资料显示:①150℃时 转化成
转化成 。
。
②酸性 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。
(4)取少量 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加_______ ,可检验是否有 生成。
生成。
(5)取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
(6)甲同学取少量 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。
①乙同学认为甲同学的实验不能证明生成了 ,理由是
,理由是_______ 。
②乙同学设计如图装置验证氧化产物中含有 。
。
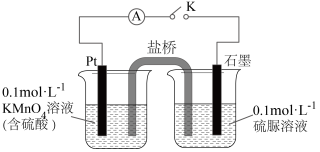
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为_______ ,经检验石墨电极附近还有 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为_______ 。
 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:①
 ;
;②25℃时硫脲溶解度为
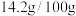 水;
水;③实验室常用FeS与稀
 在常温下制
在常温下制 。
。(1)盛放石灰乳的仪器的名称是
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现
 。
。(3)实验发现,硫脲产率与投料比
 的关系如图所示。
的关系如图所示。
最佳投料比为
实验(二):探究硫脲的性质。
资料显示:①150℃时
 转化成
转化成 。
。②酸性
 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。(4)取少量
 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加 生成。
生成。(5)取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成(6)甲同学取少量
 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。①乙同学认为甲同学的实验不能证明生成了
 ,理由是
,理由是②乙同学设计如图装置验证氧化产物中含有
 。
。
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为
 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为
您最近半年使用:0次
2024-04-01更新
|
206次组卷
|
2卷引用:四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学