1 . 某班同学用如下实验探究Fe2+与Fe3+的转化,回答下列问题,
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为_______ 。
②对比三组实验,说明加入蒸馏水后沉淀的产生与_______ 有关。
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为_______ 。
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.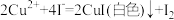 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为_______ 。
(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性, (棕色):
(棕色):
⑤使用的FeSO4溶液中存在少量铁屑,其目的是_______ 。
⑥实验中产生NO的原因为_______ (用离子方程式表示)。
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为
②对比三组实验,说明加入蒸馏水后沉淀的产生与
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.
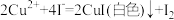 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性,
 (棕色):
(棕色):⑤使用的FeSO4溶液中存在少量铁屑,其目的是
⑥实验中产生NO的原因为
您最近一年使用:0次
名校
2 . 下列有关“实验操作”、“现象”及“实验结论”都正确的是
| 选项 | 实验操作 | 现象 | 实验结论 |
| A | 取少量某溶液,滴加 溶液 溶液 | 产生白色沉淀 | 说明溶液中含 |
| B | 用足量的盐酸溶解铁与水蒸气反应后的固体,再向溶液中滴加 溶液 溶液 | 溶液不变红 | 铁与水蒸气反应生成的产物中不含 价的铁 价的铁 |
| C | 取氯化镁和氯化铝溶液于两支试管,分别向其中加入过量的氢氧化钠溶液, | 观察到氯化镁的试管中出现白色沉淀,氯化铝的试管中先出现白色沉淀,后溶解 | 说明镁的金属性强于铝 |
| D | 将湿润的有色布条放入充满氯气的集气瓶中 | 布条褪色 | 氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-20更新
|
190次组卷
|
4卷引用:安徽省桐城中学2023-2024学年高一下学期开学检测化学试题
安徽省桐城中学2023-2024学年高一下学期开学检测化学试题 浙江省湖州市第二中学2023-2024学年高一上学期12月月考化学试题 (已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)浙江省淳安县汾口中学2023-2024学年高一上学期期末模拟(1月月考)化学试题
3 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如下图所示(CuS不溶于水),下列说法中不正确的是

| A.过程①中,生成CuS的反应为H2S+Cu2+=CuS↓+2H+ |
| B.过程②中,Fe3+作氧化剂 |
| C.过程③中,氧化剂和还原剂的物质的量之比为4:1 |
D.回收S的总反应为2H2S+O2 2H2O+2S↓ 2H2O+2S↓ |
您最近一年使用:0次
2023-12-15更新
|
731次组卷
|
12卷引用:安徽省安庆市第七中学2023-2024学年高一下学期开学考试化学试题
安徽省安庆市第七中学2023-2024学年高一下学期开学考试化学试题安徽省合肥市六校联盟2023-2024学年高一上学期1月期末化学试题湖南省长沙市周南中学2023-2024学年高一下学期开学考试化学试题北京师范大学2023--2024学年附属实验中学高一上学期化学12月统练黑龙江省肇东市第四中学2023-2024学年高一上学期期末考试化学试卷福建省三明第一中学2023-2024学年高一上学期12月月考化学试题山东省淄博第七中学2023-2024学年高一上学期阶段检测(月考)化学试题北京师范大学附属实验中学2023-2024学年高一上学期12月月考化学试题海南省白沙学校2023-2024学年高一上学期期末考试化学试题湖南省长沙市明德中学2023-2024学年高一上学期期末考试化学试题湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 江西省上饶市广丰一中2023-2024学年高一上学期12月考试化学试卷
名校
解题方法
4 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.澄清透明的溶液中: |
B.能使酚酞变红的溶液: |
C.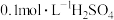 溶液: 溶液: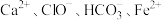 |
D. 溶液: 溶液: |
您最近一年使用:0次
2023-11-23更新
|
474次组卷
|
5卷引用:安徽省桐城中学2023-2024学年高一下学期开学检测化学试题
安徽省桐城中学2023-2024学年高一下学期开学检测化学试题 安徽省合肥市第一中学2023-2024学年高一上学期素质拓展训练(三)化学试题 江苏省南通市海安高级中学2023-2024学年高一上学期期中考试化学试题(已下线)专题03 铁 金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)江苏省南通市海安市实验中学2023-2024学年高一上学期11月期中化学试题
名校
5 . 下列离子方程式的书写正确的是
A.氯气与水的反应: |
B.用稀盐酸与碳酸钙反应制取 : :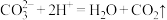 |
C.用氯化铁溶液腐蚀铜线路板: |
D.氧化铜与稀硫酸反应: |
您最近一年使用:0次
2023-08-05更新
|
335次组卷
|
5卷引用:安徽省淮北市第一中学2023-2024学年高一下学期开学考试 化学试卷
安徽省淮北市第一中学2023-2024学年高一下学期开学考试 化学试卷四川省绵阳实验高级中学2022-2023学年高一上学期线上期末考试化学试题(已下线)专题02 离子反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)吉林省“BEST合作体”2023-2024学年高一上学期期末考试化学试题陕西省西安市高陵区第三中学2023-2024学年高一上学期期末化学试卷
名校
6 . 在无色透明溶液中,下列离子能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
2023-07-29更新
|
230次组卷
|
2卷引用:安徽省芜湖市第二中学2023-2024学年高二上学期入学学情评价化学试题
名校
7 . 金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1) 溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为
溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为___________ 。
(2)经检测某酸性废水中所含离子及其浓度如表所示:
则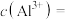
___________ mol/L。
(3)已知 的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:
的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:___________ 。
(4)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是___________ 、___________ 。
② 在空气中加热反应生成
在空气中加热反应生成 时,氧化剂和还原剂的物质的量之比为
时,氧化剂和还原剂的物质的量之比为___________ 。
(5)用托盘天平(1g以下用游码)称量绿矾( )晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是
)晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是___________ 。
a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻线,未补加水
d.定容时,俯视刻度线
(1)
 溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为
溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为(2)经检测某酸性废水中所含离子及其浓度如表所示:
| 离子 |  |  |  |  |  |
浓度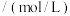 | 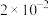 | 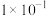 | 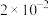 | 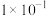 |
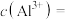
(3)已知
 的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:
的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:(4)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是
②
 在空气中加热反应生成
在空气中加热反应生成 时,氧化剂和还原剂的物质的量之比为
时,氧化剂和还原剂的物质的量之比为(5)用托盘天平(1g以下用游码)称量绿矾(
 )晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是
)晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻线,未补加水
d.定容时,俯视刻度线
您最近一年使用:0次
2023-07-15更新
|
316次组卷
|
3卷引用:安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题
安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题安徽省黄山市2022-2023学年高一上学期期末质量检测化学试题(已下线)专题06 铁、铝及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
解题方法
8 . 下列除杂试剂选用正确且除杂过程中不涉及氧化还原反应的是
| 选项 | 物质 | 杂质 | 除杂试剂 |
| A | Fe | Al | NaOH溶液 |
| B | NaCl溶液 | MgCl2 | NaOH溶液、稀盐酸 |
| C | CO2 | CO | CuO |
| D | FeSO4溶液 | Fe2(SO4)3 | Cu粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列滴加实验中,产生的实验现象描述错误的是
| 实验 | 编号 | 试剂a | 试剂b | 现象 |
 | ① |  溶液 溶液 |  溶液 溶液 | 出现血红色沉淀 |
| ② | 盐酸 |  溶液 溶液 | 开始时,无气体产生;一段时间后产生无色气体 | |
| ③ |  溶液 溶液 |  溶液 溶液 | 立刻产生白色沉淀 | |
| ④ |  溶液 溶液 | 稀氨水 | 立刻产生白色沉淀 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
10 . 元素价一类二维图是学习元素化合物知识的重要模型,下图为铁元素的价一类二维图:

请问答下列问题:
(1)炽热的铁水注入模具前,模具必须彻底干燥,是为了避免_______ 反应的发生(写化学方程式)。
(2)高温下利用铝粉与甲反应可用来焊接钢轨。某化学兴趣小组欲用以下装置探究甲与铝粉的反应,实验发现:反应放出大量的热,并发出耀眼的光芒,纸漏斗的下部被烧穿,有熔融物落入沙中。
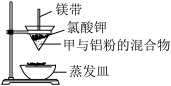
①铝粉与甲反应的化学方程式为_______ 。
②该小组玲玲同学欲探究该熔融物中是否含有+3价铁,进行了如下实验:取出适量的熔融物,加入稀盐酸充分溶解,滴加KSCN溶液,无明显现象,说明熔融物中无+3价铁。芳芳同学不同意此观点,原因为:_______ 。
(3)戊、己分别能与碱反应能生成丙和丁。若己为硫酸盐,向其溶液中加入NaOH溶液时,出现的现象有_______ 。
(4)将表面附有铁锈(主要成分是甲)的铁钉放入稀硫酸中,开始反应时主要离子方程式是_______ ;反应片刻后,向反应后溶液滴加KSCN溶液,溶液未出现红色,其原因为_______ (用离子方程式表示)。
(5)将1.12 g铁粉加入40 mL 2 mol·L 的戊溶液中(戊为氯化物),充分反应后,溶液中
的戊溶液中(戊为氯化物),充分反应后,溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为_______ ,标准状况下至少通入_______ mL  才可完全除去溶液中的
才可完全除去溶液中的 。
。

请问答下列问题:
(1)炽热的铁水注入模具前,模具必须彻底干燥,是为了避免
(2)高温下利用铝粉与甲反应可用来焊接钢轨。某化学兴趣小组欲用以下装置探究甲与铝粉的反应,实验发现:反应放出大量的热,并发出耀眼的光芒,纸漏斗的下部被烧穿,有熔融物落入沙中。

①铝粉与甲反应的化学方程式为
②该小组玲玲同学欲探究该熔融物中是否含有+3价铁,进行了如下实验:取出适量的熔融物,加入稀盐酸充分溶解,滴加KSCN溶液,无明显现象,说明熔融物中无+3价铁。芳芳同学不同意此观点,原因为:
(3)戊、己分别能与碱反应能生成丙和丁。若己为硫酸盐,向其溶液中加入NaOH溶液时,出现的现象有
(4)将表面附有铁锈(主要成分是甲)的铁钉放入稀硫酸中,开始反应时主要离子方程式是
(5)将1.12 g铁粉加入40 mL 2 mol·L
 的戊溶液中(戊为氯化物),充分反应后,溶液中
的戊溶液中(戊为氯化物),充分反应后,溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为 才可完全除去溶液中的
才可完全除去溶液中的 。
。
您最近一年使用:0次



