解题方法
1 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是A. 中 中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
B.该反应中氧化产物与还原产物的物质的量之比为 |
| C.依据该反应原理,可设计原电池 |
D.完全反应后,可用 溶液检验反应后的溶液中是否存在 溶液检验反应后的溶液中是否存在 |
您最近一年使用:0次
名校
2 . KSCN是实验室常用的化学试剂。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。
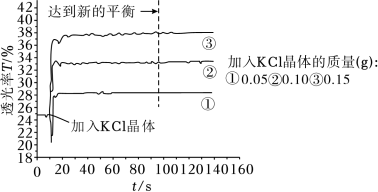
已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl- [FeCl4]-(黄色)。
[FeCl4]-(黄色)。
①采用FeCl3稀溶液是为了避免_______ (填离子符号)的颜色对实验干扰。
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度_______ (填“增大”“减小”或“不变”),从平衡移动的角度分析可能的原因_______ 。
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O +I2=S4O
+I2=S4O +2I-;
+2I-;
ii.I2+I- I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;
iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为_______ ;根据信息预测最终测定的结果将_______ (填“偏大”“偏小”或“无影响”)。
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式_______ ;到达滴定终点时消耗标准液20.00mL,样品中铜元素质量分数为_______ ,滴定后仍存在少量CuI沉淀,测得溶液中c(I-)=0.2mol•L-1,则c(SCN-)=_______ 。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。

已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl-
 [FeCl4]-(黄色)。
[FeCl4]-(黄色)。①采用FeCl3稀溶液是为了避免
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O
 +I2=S4O
+I2=S4O +2I-;
+2I-;ii.I2+I-
 I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式
您最近一年使用:0次
2024-04-05更新
|
53次组卷
|
3卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
名校
解题方法
3 . 菠菜中富含铁元素,用下列步骤完成铁元素的检验,各步选用的实验仪器不需要的是
| |
|
|
| A.将菠菜剪碎后研磨 | B.用蒸馏水溶解 | C.过滤得到滤液 | D.检验滤液中的Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-03更新
|
46次组卷
|
2卷引用:湖南省衡阳市祁东县成章高级中学2023-2024学年高一下学期入学考试化学试卷
名校
解题方法
4 . 有关铁的化合物的说法中,正确的是
A. 是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色 是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色 |
B. 与 与 产生血红色沉淀 产生血红色沉淀 |
C. 、 、 都可以由化合反应制得 都可以由化合反应制得 |
D.向煮沸的氢氧化钠溶液中逐滴加入5滴 饱和溶液,继续煮沸至液体呈红褐色,停止加热,制得 饱和溶液,继续煮沸至液体呈红褐色,停止加热,制得 胶体 胶体 |
您最近一年使用:0次
解题方法
5 . 攀枝花铁矿,探明储量的钒钛磁铁矿达近百亿吨,其中钒、钛储量分别占全国已探明储量的87%和94.3%,分别居世界第三位和第一位,有“世界钒钛之都”之称,是全国四大铁矿区之一,炼铁厂以磁铁矿石、焦炭、空气等为主要原料炼铁,主要反应过程如图所示:

请根据所学知识回答下列问题。
(1)磁铁矿的主要成分是___________ (填化学式),铁元素在元素周期表中位于第___________ 周期第___________ 族。
(2)生铁和钢相比,含碳量更高的是___________ 。
(3)原料中焦炭的作用是___________ 。写出反应③的化学方程式:___________ 。
(4)铁的化合物之一聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m高铁酸盐均可用作水处理剂。以绿矾(FeSO4·7H2O)为原料,可制备聚合硫酸铁和高铁酸盐。
①为检验绿矾是否变质,可采取的操作方法是___________ 。
②取2ml FeSO4溶液于试管中,向其中滴加氢氧化钠溶液,观察到生成的白色沉淀迅速变为灰绿色, 最终变为红褐色,写出此过程中涉及的氧化还原反应的化学方程式:___________ 。已知在浓碱溶液中,NaClO能将Fe(OH)3,氧化为含FeO 的紫红色溶液,请写出该过程中发生反应的离子方程式:
的紫红色溶液,请写出该过程中发生反应的离子方程式:___________ 。

请根据所学知识回答下列问题。
(1)磁铁矿的主要成分是
(2)生铁和钢相比,含碳量更高的是
(3)原料中焦炭的作用是
(4)铁的化合物之一聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m高铁酸盐均可用作水处理剂。以绿矾(FeSO4·7H2O)为原料,可制备聚合硫酸铁和高铁酸盐。
①为检验绿矾是否变质,可采取的操作方法是
②取2ml FeSO4溶液于试管中,向其中滴加氢氧化钠溶液,观察到生成的白色沉淀迅速变为灰绿色, 最终变为红褐色,写出此过程中涉及的氧化还原反应的化学方程式:
 的紫红色溶液,请写出该过程中发生反应的离子方程式:
的紫红色溶液,请写出该过程中发生反应的离子方程式:
您最近一年使用:0次
解题方法
6 . 下表是各物质及其所含的少量杂质,以及除去这些杂质所选用的试剂或操作方法,其中错误的是
| 选项 | 物质 | 杂质 | 除杂试剂或操作方法 |
| A | FeCl2 溶液 | FeCl3 | 加入过量铁粉,再过滤 |
| B | NaHCO3 溶液 | Na2CO3 | 通入过量的 CO2气体 |
| C | NaNO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,再过滤 |
| D | MgO 固体 | Al2O3 | 加入过量的NaOH溶液,再过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式中,正确的是
A. 与 与 溶液反应: 溶液反应: |
B.氯化铁溶液与过量的锌反应: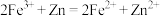 |
C. 溶液与 溶液与 溶液反应: 溶液反应: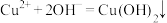 |
D. 溶液与 溶液与 溶液混合: 溶液混合: |
您最近一年使用:0次
2024-02-03更新
|
45次组卷
|
3卷引用:湖南省岳阳市 岳阳县第一中学2023-2024学年高一下学期开学化学试题
8 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如下图所示(CuS不溶于水),下列说法中不正确的是

| A.过程①中,生成CuS的反应为H2S+Cu2+=CuS↓+2H+ |
| B.过程②中,Fe3+作氧化剂 |
| C.过程③中,氧化剂和还原剂的物质的量之比为4:1 |
D.回收S的总反应为2H2S+O2 2H2O+2S↓ 2H2O+2S↓ |
您最近一年使用:0次
2023-12-15更新
|
731次组卷
|
12卷引用:湖南省长沙市周南中学2023-2024学年高一下学期开学考试化学试题
湖南省长沙市周南中学2023-2024学年高一下学期开学考试化学试题湖南省长沙市明德中学2023-2024学年高一上学期期末考试化学试题湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 安徽省安庆市第七中学2023-2024学年高一下学期开学考试化学试题北京师范大学2023--2024学年附属实验中学高一上学期化学12月统练黑龙江省肇东市第四中学2023-2024学年高一上学期期末考试化学试卷福建省三明第一中学2023-2024学年高一上学期12月月考化学试题山东省淄博第七中学2023-2024学年高一上学期阶段检测(月考)化学试题北京师范大学附属实验中学2023-2024学年高一上学期12月月考化学试题海南省白沙学校2023-2024学年高一上学期期末考试化学试题安徽省合肥市六校联盟2023-2024学年高一上学期1月期末化学试题江西省上饶市广丰一中2023-2024学年高一上学期12月考试化学试卷
名校
解题方法
9 . 周南中学化学研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并回答下列问题:
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为___________ 。
(2)反应前A中投放碎瓷片的目的是___________ 。
(3)装置E中的现象是___________ 。
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻管B冷却后,取少许其中的固体物质溶于___________ 后(写物质名称),将所得溶液分成两份。一份滴加几滴 溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为
溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为___________ (填序号)。
①一定有 ②一定有
②一定有 ③只有
③只有 ④只有
④只有
另一份用胶头滴管加入___________ (填试剂和现象),可以证明溶液中存在 。
。
探究三:设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(5)计算反应后B装置中铁元素的质量分数为___________ 。
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为
(2)反应前A中投放碎瓷片的目的是
(3)装置E中的现象是
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻管B冷却后,取少许其中的固体物质溶于
 溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为
溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为①一定有
 ②一定有
②一定有 ③只有
③只有 ④只有
④只有
另一份用胶头滴管加入
 。
。探究三:设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(5)计算反应后B装置中铁元素的质量分数为
您最近一年使用:0次
名校
10 . 取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为 ),反应现象没有明显差别的是
),反应现象没有明显差别的是
 ),反应现象没有明显差别的是
),反应现象没有明显差别的是| 选项 | 试剂① | 试剂② |
| A | 盐酸 |  溶液 溶液 |
| B |  溶液 溶液 |  溶液 溶液 |
| C |  溶液 溶液 | 酸性 溶液 溶液 |
| D |  溶液 溶液 |  溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-17更新
|
86次组卷
|
2卷引用:湖南省长沙市周南中学2023-2024学年高二上学期入学考试化学试题