1 . 实验是探究物质性质的重要方法,下列操作中,实验现象与得出的结论相一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 比较HClO和CH3COOH的酸性强弱 | 用pH计测定NaClO和CH3COONa的pH值,测得pH(NaClO)>pH(CH3COONa) | 酸性:HClO>CH3COOH |
| B | 验证反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 | 向2mL 0.1mol/L FeCl3溶液加入几滴0.1mol/L KI溶液,充分反应。取反应后试样,滴加淀粉溶液,溶液变为蓝色;另取反应后试样,加入KSCN溶液,溶液变成血红色 | 反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 |
| C | 判断 (AgCl)与 (AgCl)与 (AgI)的大小 (AgI)的大小 | 向等浓度的NaCl、NaI的混合溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| D | 判断某 溶液样品中是否含有 溶液样品中是否含有 | 向某 溶液样品中加入硫酸酸化的 溶液样品中加入硫酸酸化的 溶液,紫色褪去 溶液,紫色褪去 | 该样品中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列除去物质中的少量杂质(括号内为杂质),选用的试剂正确的是
| 选项 | 物质 | 除杂试剂 |
| A | N2(O2) | 灼热的CuO |
| B | CO2(HCl) | 足量Na2CO3溶液 |
| C | FeCl2溶液(FeCl3) | 足量铁屑 |
| D | KCl溶液(MgCl2) | 适量NaOH溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为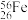 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向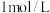 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
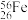 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向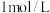 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近一年使用:0次
4 . 针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是___________ (填元素符号),最高价氧化物对应水化物酸性最强的是___________ (填氧化物对应水化物的化学式)。
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程___________ 。
(3)①②⑦的原子半径由大到小的顺序为___________ (填元素符号)。
(4)①和⑧非金属性比较①___________ ⑧(填>、<或=),请设计实验证明___________ (用一个化学方程式表示)。
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(6)为证明某溶液中不含Fe3+而可能含有Fe2+,选用下列试剂进行实验,可行的操作顺序___________。
①加入少量的氯水 ②加入少量酸性KMnO4溶液 ③加入KSCN溶液
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程
(3)①②⑦的原子半径由大到小的顺序为
(4)①和⑧非金属性比较①
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(6)为证明某溶液中不含Fe3+而可能含有Fe2+,选用下列试剂进行实验,可行的操作顺序___________。
①加入少量的氯水 ②加入少量酸性KMnO4溶液 ③加入KSCN溶液
| A.①③ | B.③② | C.③① | D.①② |
您最近一年使用:0次
解题方法
5 . 除去下列物质中的杂质,所用试剂和方法正确的是
| 选项 | 物质 | 杂质 | 除杂质所用试剂(过量) | 操作方法 |
| ① | 铝粉 | 铁粉 | NaOH 溶液 | 过滤 |
| ② | KNO3溶液 | K2SO4 | Ba(NO3)2 溶液 | 过滤 |
| ③ | Cl2 | HCl | 饱和 NaCl 溶液、浓硫酸 | 洗气 |
| ④ | FeCl3 | CuCl2 | 铁屑 | 过滤 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
解题方法
6 . 下列各组离子能在溶液中大量共存的是
A.K+、H+、 、OH- 、OH- | B.Fe3+、SCN-、Cl-、Na+ |
C.Na+、H+、Cl-、 | D.Na+、Cu2+、Cl-、 |
您最近一年使用:0次
解题方法
7 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是A. 中 中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
B.该反应中氧化产物与还原产物的物质的量之比为 |
| C.依据该反应原理,可设计原电池 |
D.完全反应后,可用 溶液检验反应后的溶液中是否存在 溶液检验反应后的溶液中是否存在 |
您最近一年使用:0次
解题方法
8 . 下列离子方程式书写正确的是
A.少量铁粉与盐酸混合: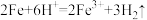 |
B.往 溶液中加入过量氨水: 溶液中加入过量氨水: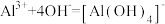 |
C.往 溶液中加入过量铜粉: 溶液中加入过量铜粉: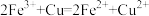 |
D.往KBr溶液中加入碘水: |
您最近一年使用:0次
9 . 除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是
| A.CO2(SO2):饱和NaHCO3溶液 | B.NO(NO2):水 |
| C.FeCl2溶液(FeCl3):加入足量的铜粉、过滤 | D.MgO (Al2O3):NaOH溶液、过滤 |
您最近一年使用:0次
名校
解题方法
10 . 钠、铝、铁是三种重要的金属。请回答:
(1)将一小块金属钠投入水中,发生反应的离子方程式为_____________ ;可观察到的实验现象是________ (填编号)。a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(2)铝和氢氧化钠反应的化学方程式为:________________
(3)Fe跟Cl2在一定条件下反应,所得产物的化学式是________ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:a.若向其中一支试管中滴加KSCN溶液,则溶液变成________ 色。
b.向另一支试管中滴加NaOH溶液,现象为________________ 。
c.氢氧化亚铁被氧气氧化的化学方程式为:_____________ 。
(1)将一小块金属钠投入水中,发生反应的离子方程式为
(2)铝和氢氧化钠反应的化学方程式为:
(3)Fe跟Cl2在一定条件下反应,所得产物的化学式是
b.向另一支试管中滴加NaOH溶液,现象为
c.氢氧化亚铁被氧气氧化的化学方程式为:
您最近一年使用:0次



