解题方法
1 . 除去下列物质中的杂质,所用试剂和方法正确的是
| 选项 | 物质 | 杂质 | 除杂质所用试剂(过量) | 操作方法 |
| ① | 铝粉 | 铁粉 | NaOH 溶液 | 过滤 |
| ② | KNO3溶液 | K2SO4 | Ba(NO3)2 溶液 | 过滤 |
| ③ | Cl2 | HCl | 饱和 NaCl 溶液、浓硫酸 | 洗气 |
| ④ | FeCl3 | CuCl2 | 铁屑 | 过滤 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
解题方法
2 . 下列各组离子能在溶液中大量共存的是
A.K+、H+、 、OH- 、OH- | B.Fe3+、SCN-、Cl-、Na+ |
C.Na+、H+、Cl-、 | D.Na+、Cu2+、Cl-、 |
您最近一年使用:0次
解题方法
3 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是A. 中 中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
B.该反应中氧化产物与还原产物的物质的量之比为 |
| C.依据该反应原理,可设计原电池 |
D.完全反应后,可用 溶液检验反应后的溶液中是否存在 溶液检验反应后的溶液中是否存在 |
您最近一年使用:0次
4 . 下列有关实验、现象及结论等叙述正确的个数有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2024-04-19更新
|
299次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高一下学期开学考试化学试题
5 . 能证明溶液中含有 的试剂是
的试剂是
 的试剂是
的试剂是| A.铜粉 | B. 溶液 溶液 | C.稀硫酸 | D.酚酞溶液 |
您最近一年使用:0次
名校
6 . 下列实验目的、方案设计和现象、结论都正确的是
| 选项 | 实验目的 | 方案设计和现象 | 结论 |
| A | 验证浓硫酸的性质 | 将浓硫酸滴入蔗糖中并搅拌,得到黑色蓬松的固体,并产生刺激性气味的气体 | 浓硫酸具有强氧化性和脱水性 |
| B | 探究钠在空气中久置后所得固体成分 | 取少量固体,加入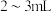 蒸馏水,有气体产生 蒸馏水,有气体产生 | 固体中一定含 |
| C | 检验某溶液中是否含有 | 取少量待检液于试管中,滴加新制氯水后滴加 溶液,溶液变为红色 溶液,溶液变为红色 | 该溶液含有 |
| D | 检验 和浓盐酸反应后是否有酸剩余 和浓盐酸反应后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入稀硝酸、 溶液 溶液 | 产生大量白色沉淀,则盐酸有剩余 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-03更新
|
252次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高一下学期入学考试化学试题
名校
解题方法
7 . 明矾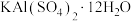 在日常生活中用途非常广泛。用废铝灰(含Al、
在日常生活中用途非常广泛。用废铝灰(含Al、 、Fe、
、Fe、 、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
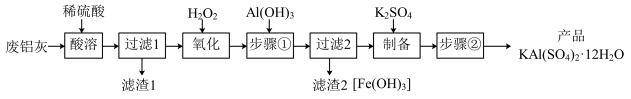
已知: 开始沉淀到沉淀完全时溶液的pH为1.9~3.7;
开始沉淀到沉淀完全时溶液的pH为1.9~3.7; 开始沉淀到完全沉淀时溶液的pH为5.5~8.5。
开始沉淀到完全沉淀时溶液的pH为5.5~8.5。
(1)“酸溶”时, 溶解的离子方程式为
溶解的离子方程式为_____ 。
(2)“氧化”时,发生反应的离子方程式为_____ 。
(3)“步骤①”调节pH约为3.7的目的是_____ ;检验“过滤2”滤液中是否含 可用试剂
可用试剂_____ 。
(4)“步骤②”包含的操作有_____ 、_____ 、过滤、洗涤及干燥。
(5)已知废铝灰中铝元素的含量为a%,则mkg废铝灰理论上可制得明矾_____ kg。
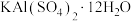 在日常生活中用途非常广泛。用废铝灰(含Al、
在日常生活中用途非常广泛。用废铝灰(含Al、 、Fe、
、Fe、 、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:
已知:
 开始沉淀到沉淀完全时溶液的pH为1.9~3.7;
开始沉淀到沉淀完全时溶液的pH为1.9~3.7; 开始沉淀到完全沉淀时溶液的pH为5.5~8.5。
开始沉淀到完全沉淀时溶液的pH为5.5~8.5。(1)“酸溶”时,
 溶解的离子方程式为
溶解的离子方程式为(2)“氧化”时,发生反应的离子方程式为
(3)“步骤①”调节pH约为3.7的目的是
 可用试剂
可用试剂(4)“步骤②”包含的操作有
(5)已知废铝灰中铝元素的含量为a%,则mkg废铝灰理论上可制得明矾
您最近一年使用:0次
名校
解题方法
8 . 绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al,Al2O3和Fe2O3)制备磁性Fe3O4胶体粒子、绿矾和净水剂Na2FeO4的实验流程如图:
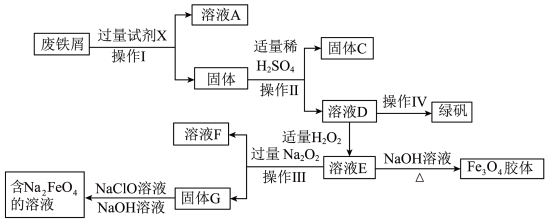
请回答下列问题:
(1)试剂X化学式为______ 。
(2)铁元素在元素周期表的位置为______ 。
(3)固体C化学名称为______ 。溶液D中加入 溶液,无红色产生,原因是
溶液,无红色产生,原因是______ (用离子方程式表示)。
(4)为得到绿矾晶体需要将溶液D倒入______ (填仪器名称)中进行浓缩,结晶。
(5)D中加入适量H2O2生成E的离子方程式______ 。若D中含3amolFe2+,则理论上加入______  H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
(6)由固体G生成Na2FeO4的离子方程式为______ 。

请回答下列问题:
(1)试剂X化学式为
(2)铁元素在元素周期表的位置为
(3)固体C化学名称为
 溶液,无红色产生,原因是
溶液,无红色产生,原因是(4)为得到绿矾晶体需要将溶液D倒入
(5)D中加入适量H2O2生成E的离子方程式
 H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。(6)由固体G生成Na2FeO4的离子方程式为
您最近一年使用:0次
名校
解题方法
9 . 下列各组离子在指定溶液中一定能大量共存的是
A.常温下,在 的溶液中:Na+、Fe2+、 的溶液中:Na+、Fe2+、 、Cl- 、Cl- |
B.1mol/L的NaAlO2溶液中:Al3+、Na+、SO2-、 |
C.含有Fe3+的溶液中:K+、Na+、SCN-、 |
D.常温下,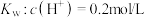 的溶液:K+、Na+、 的溶液:K+、Na+、 、 、 |
您最近一年使用:0次
名校
解题方法
10 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: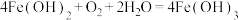 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |
您最近一年使用:0次