名校
解题方法
1 . 还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另取少量反应后的固体加入稀硝酸使其完全溶解,得溶液b.下列说法正确的是
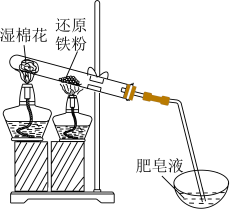
A.铁与水蒸气反应: |
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成 |
C.向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉未完全反应 溶液,出现蓝色沉淀,说明铁粉未完全反应 |
D.向溶液b中滴加 溶液,溶液变红,证实了固体中含有 溶液,溶液变红,证实了固体中含有 |
您最近半年使用:0次
今日更新
|
473次组卷
|
3卷引用:北京市西城区2024届高三统一测试(一模)化学试题
北京市西城区2024届高三统一测试(一模)化学试题2024届河南省焦作市博爱县第一中学高三下学期三模化学试题(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)
解题方法
2 . 某合作学习小组将铜片放进氯化铁溶液中,观察到溶液呈无色,产生红褐色固体,铜片表面有白色物质。
Ⅰ.探究红褐色固体成分
(1)过滤得到红褐色固体,所需的仪器有___________ (填标号)。___________ 溶液,溶液变血红色,证明是氢氧化铁。
②产生氢氧化铁的原因可能是___________ (用化学方程式表示)。
Ⅱ.查阅资料:CuCl是白色难溶物
(3)探究产生白色物质的原因。设计实验方案如下:
①由以上实验可知,产生白色物质的条件是___________ 。
②实验2生成白色物质的化学方程式为:___________ 。
③请你从氧化还原反应规律角度分析实验1中未产生白色物质的原因___________ 。
(4)以石墨为电极电解 溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为
溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为___________ 。
(5)基于上述分析,用 溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用
溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用 、KCl、盐酸混合物腐蚀覆铜板,原理为:
、KCl、盐酸混合物腐蚀覆铜板,原理为: 。
。
①基态 的价电子轨道表示式为
的价电子轨道表示式为___________ 。
②KCl的作用是___________ 。
(6)氧化还原反应的应用十分广泛。写出一种氧化剂在生活中的应用___________ 。
Ⅰ.探究红褐色固体成分
(1)过滤得到红褐色固体,所需的仪器有
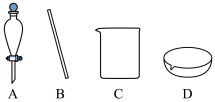
②产生氢氧化铁的原因可能是
Ⅱ.查阅资料:CuCl是白色难溶物
(3)探究产生白色物质的原因。设计实验方案如下:
| 实验 | 铜粉/g | 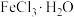 /g /g | 蒸馏水/mL | 实验现象 |
| 1 | 0.1 | 1.8 | 2 | 棕黄色溶液变为墨绿色 |
| 2 | 0.5 | 1.8 | 2 | 棕黄色溶液变为白色浊液 |
②实验2生成白色物质的化学方程式为:
③请你从氧化还原反应规律角度分析实验1中未产生白色物质的原因
(4)以石墨为电极电解
 溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为
溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为(5)基于上述分析,用
 溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用
溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用 、KCl、盐酸混合物腐蚀覆铜板,原理为:
、KCl、盐酸混合物腐蚀覆铜板,原理为: 。
。①基态
 的价电子轨道表示式为
的价电子轨道表示式为②KCl的作用是
(6)氧化还原反应的应用十分广泛。写出一种氧化剂在生活中的应用
您最近半年使用:0次
解题方法
3 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 用 | 氧化性: |
B |
|
|
C | 液氨可用作制冷剂 | 氨气极易溶于水 |
D | Na着火不能用水扑灭 | Na可与水反应产生 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . 粉煤灰是燃煤产生的工业固体废料,主要成分有 、
、 ,还含有少量
,还含有少量 、CaO等。采用酸碱联合的方法从粉煤灰中综合回收氧化铝及二氧化硅的工艺流程如下:
、CaO等。采用酸碱联合的方法从粉煤灰中综合回收氧化铝及二氧化硅的工艺流程如下:
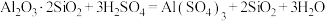

(1)“结晶”操作:缓缓加热,浓缩至___________ ,放置冷却,得到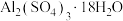 。
。
(2)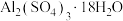 在250~300℃下失重40.5%得
在250~300℃下失重40.5%得 ,
,
___________ 。
(3)“还原焙烧”过程中发生反应的化学方程式为___________ 。
(4)设计实验检验粗氧化铝中是否含有 :
:___________ 。
(5)向硅酸钠溶液中通入过量 制备白炭黑的化学方程式为
制备白炭黑的化学方程式为___________ 。
 、
、 ,还含有少量
,还含有少量 、CaO等。采用酸碱联合的方法从粉煤灰中综合回收氧化铝及二氧化硅的工艺流程如下:
、CaO等。采用酸碱联合的方法从粉煤灰中综合回收氧化铝及二氧化硅的工艺流程如下: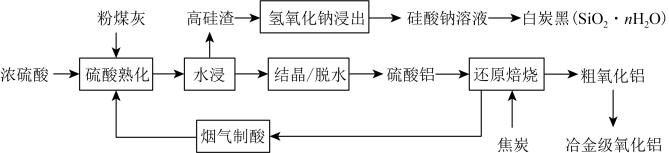
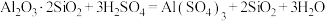

(1)“结晶”操作:缓缓加热,浓缩至
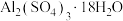 。
。(2)
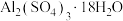 在250~300℃下失重40.5%得
在250~300℃下失重40.5%得 ,
,
(3)“还原焙烧”过程中发生反应的化学方程式为
(4)设计实验检验粗氧化铝中是否含有
 :
:(5)向硅酸钠溶液中通入过量
 制备白炭黑的化学方程式为
制备白炭黑的化学方程式为
您最近半年使用:0次
解题方法
5 . 下列反应的离子方程式正确的是
| A.向FeCl3溶液中通入H2S气体:2Fe3++H2S=2Fe2++S↓+2H+ |
B.向AlCl3溶液中滴加过量氨水:Al+4NH3·H2O= +4 +4 +2H2O +2H2O |
| C.将Cl2通入冷的石灰乳中制漂白粉:2OH-+Cl2=Cl-+ClO-+H2O |
D.向Ba(OH)2溶液中滴加H2SO4溶液至沉淀完全:Ba2++ +H++OH-=BaSO4↓+H2O +H++OH-=BaSO4↓+H2O |
您最近半年使用:0次
解题方法
6 . 化学反应在生产生活中应用广泛。下列离子方程式书写正确且能解释相应应用的是
| 选项 | 应用 | 离子方程式 |
| A | 使用碳酸钠溶液浸泡锅炉水垢 | 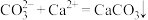 |
| B | 使用 溶液腐蚀铜制电路板 溶液腐蚀铜制电路板 |  |
| C | 海水提溴时,吸收塔利用 溶液吸收从吹出塔出来的溴蒸气 溶液吸收从吹出塔出来的溴蒸气 | 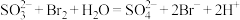 |
| D | 使用盐酸清洗铜器表面的铜绿 | 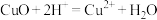 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
7 . 下列鉴别或检验不能 达到实验目的的是
| A.鉴别羊毛线和棉线:取样,分别点燃 | B.鉴别晶体与非晶体:取样,进行 射线衍射实验 射线衍射实验 |
C.用 溶液检验 溶液检验 是否变质 是否变质 | D.用 溶液检验 溶液检验 是否变质 是否变质 |
您最近半年使用:0次
名校
8 . 根据下列实验操作和现象得出的结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向稀硫酸酸化的FeSO4,溶液中滴入H2O2溶液 | 溶液变黄 | 氧化性:H2O2>Fe3+ |
| B | 向CO还原Fe2O3,所得到的产物中加入稀盐酸,再滴加KSCN溶液 | 溶液不变红 | Fe2O3一定已全部被CO还原 |
| C | 向NaCl溶液中滴入几滴AgNO3溶液,再加入氨水,振荡 | 先产生白色沉淀,加氨水后沉淀消失 | AgCl不溶于水,但可溶于氨水 |
| D | 用pH试纸分别测定浓度均为0.1mol·L-1的CH3COONa溶液,NaNO2溶液的pH | 前者pH约为9,后者pH约为8 | Ka(CH3COOH)<Ka(HNO2) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 .  是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓
是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓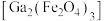 、铁酸锌
、铁酸锌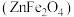 ,还含少量
,还含少量 及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。 在酸性条件下不稳定,易转化为
在酸性条件下不稳定,易转化为 。
。
②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于 时可视为沉淀完全。
时可视为沉淀完全。
③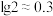 ,
,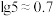 。
。
回答下列问题:
(1)写出两条加快“浸出”速率的措施:_____ 。
(2) 中铁元素的化合价为
中铁元素的化合价为_____ , 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为_____
(3)“调 ”时需调节溶液
”时需调节溶液 的最小值为
的最小值为_____ 。
(4)“滤液1”中主要含有的金属阳离子为_____ ,检验“滤液1”中是否含有 的试剂为
的试剂为_____ (填名称)。
(5)“转化2”加入铁粉时主要发生反应的离子方程式为_____ 。
(6)“电解”反萃取液(溶质为 )制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为
)制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为_____ (填化学式)。
(7)采用MOCVD(金属有机化合物化学气相沉积)技术制备GaN时,反应会产生一种标准状况下密度约为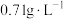 的可燃性气体,写出该反应的化学方程式:
的可燃性气体,写出该反应的化学方程式:_____ (不写条件)。
 是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓
是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓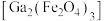 、铁酸锌
、铁酸锌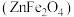 ,还含少量
,还含少量 及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
 在酸性条件下不稳定,易转化为
在酸性条件下不稳定,易转化为 。
。②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于
 时可视为沉淀完全。
时可视为沉淀完全。| 氢氧化物 |  |  |  |  |
 |  |  | 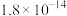 | 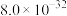 |
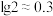 ,
,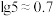 。
。回答下列问题:
(1)写出两条加快“浸出”速率的措施:
(2)
 中铁元素的化合价为
中铁元素的化合价为 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(3)“调
 ”时需调节溶液
”时需调节溶液 的最小值为
的最小值为(4)“滤液1”中主要含有的金属阳离子为
 的试剂为
的试剂为(5)“转化2”加入铁粉时主要发生反应的离子方程式为
(6)“电解”反萃取液(溶质为
 )制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为
)制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为(7)采用MOCVD(金属有机化合物化学气相沉积)技术制备GaN时,反应会产生一种标准状况下密度约为
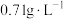 的可燃性气体,写出该反应的化学方程式:
的可燃性气体,写出该反应的化学方程式:
您最近半年使用:0次
10 . 根据下列实验操作、现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溴乙烷与NaOH乙醇溶液加热反应产生的气体通入盛有酸性高锰酸钾溶液的试管中 | 试管中的溶液紫红色褪去 | 溴乙烷发生了消去反应,生成了乙烯气体 |
| B | 向FeCl2、KBr的混合溶液中滴入少量氯水,充分反应后再加入一定量的CCl4,振荡、静置分层,观察下层颜色;再向上层溶液中滴加KSCN溶液 | 下层溶液呈无色,往上层溶液中滴加KSCN溶液后,溶液变为血红色 | 氧化性:Cl2>Br2>Fe3+ |
| C | 向某溶液中加入NaOH浓溶液并加热,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 该溶液中一定没有 |
| D | 向滴有KSCN的FeCl3溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次

 溶液刻蚀铜质电路板
溶液刻蚀铜质电路板
 可用于治疗胃酸过多
可用于治疗胃酸过多


