解题方法
1 . 下列有关物质性质与用途对应关系不正确 的是
| A.Na2CO3溶液呈碱性,可用除油污 | B.明矾易溶于水,可用作净水剂 |
| C.ClO2具有强氧化性,可用作消毒剂 | D.FeCl3具有氧化性,可用于蚀刻电路板 |
您最近半年使用:0次
2 . 检验某溶液中是否含有 ,下列操作中正确的是
,下列操作中正确的是
 ,下列操作中正确的是
,下列操作中正确的是A.滴加 溶液 溶液 | B.加入氧化铁 | C.滴加 溶液 溶液 | D.通入氯气 |
您最近半年使用:0次
名校
解题方法
3 . 已知FeCl3溶液和KI溶液能发生反应:2Fe3++2I-⇌2Fe2++I2.下列关于该反应的说法错误的是
| A.升高温度会加快反应速率 |
| B.增大Fe3+和I-的浓度能加快反应速率 |
| C.当上述可逆反应达到平衡时,溶液中c(Fe3+)与c(Fe2+)相等 |
| D.向反应后的溶液中加入CCl4,充分振荡后静置,取上层溶液滴加KSCN溶液,溶液变成血红色 |
您最近半年使用:0次
2024-02-08更新
|
74次组卷
|
2卷引用:江苏省连云港市2023-2024学年高二上学期普通高中学业水平合格性考试模拟化学试题
4 . 下列实验现象描述正确的是
| A.KOH溶液中滴加酚酞试液,一段时间后溶液呈无色 |
| B.新制Cu(OH)2悬浊液中加入葡萄糖溶液并加热,产生砖红色沉淀 |
| C.FeCl3溶液中滴入KSCN溶液,溶液呈蓝色 |
| D.H2在Cl2中燃烧,发出黄色火焰 |
您最近半年使用:0次
5 . 下列物质的性质与用途具有对应关系的是
| A.浓硫酸具有脱水性,可用来干燥Cl2 |
| B.FeCl3溶液显酸性,可用于印刷电路板 |
| C.Na2O2呈淡黄色,可用作呼吸面具中的供氧剂 |
| D.活性铁粉具有还原性,可用作食品抗氧化剂 |
您最近半年使用:0次
6 . 下列实验方案能达到预期目的是
A.用分液的方法分离溴水中的 |
B.用铜粉除去 溶液中混有的少量 溶液中混有的少量 |
| C.用焰色试验(又称焰色反应)鉴别NaCl溶液和KCl溶液 |
D.用稀盐酸产生能使澄清石灰水变浑浊的气体检验溶液中是否含有 |
您最近半年使用:0次
7 . 四氧化三铁(Fe3O4)俗称磁性氧化铁,在工业上应用广泛,可作催化剂、磁记录材料等。Fe3O4的一种制备方法如下:
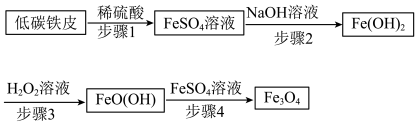
(1)低碳铁皮与稀硫酸反应时,会形成许多微小原电池。
①形成原电池时,Fe作___________ 。
A.正极 B.负极
②反应过程中,溶液的pH___________ 。
A.变大 B.变小 C.不变
(2)检验步骤1得到的FeSO4溶液中是否存在 ,可选用的试剂是___________。
,可选用的试剂是___________。
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7(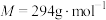 )固体,配制成
)固体,配制成 K2Cr2O7标准溶液。
K2Cr2O7标准溶液。
①称量时,需用到的仪器有___________ 。
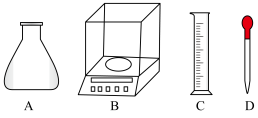
②根据计算,选用的容量瓶规格应为___________ 。
A.100mL B.250mL C.500mL D.1000mL
(4)步骤2用下图所示装置制备 。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
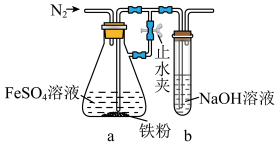
止水夹关闭前后,通入N2的作用分别为___________ 、___________ 。
(5)步骤3的反应原理为: 。反应中每消耗34gH2O2,转移的电子数为
。反应中每消耗34gH2O2,转移的电子数为___________ 。
(6)步骤4在不同时刻得到的Fe3O4粒径大小如下图所示。
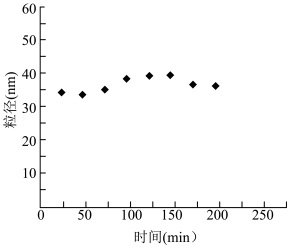
①实验过程中,Fe3O4不易形成沉淀,结合上图分析原因___________ 。
②写出一种可使Fe3O4较快形成沉淀的方法___________ 。

(1)低碳铁皮与稀硫酸反应时,会形成许多微小原电池。
①形成原电池时,Fe作
A.正极 B.负极
②反应过程中,溶液的pH
A.变大 B.变小 C.不变
(2)检验步骤1得到的FeSO4溶液中是否存在
 ,可选用的试剂是___________。
,可选用的试剂是___________。| A.KSCN溶液 | B.KMnO4溶液 | C.稀硝酸 | D.BaCl2溶液 |
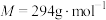 )固体,配制成
)固体,配制成 K2Cr2O7标准溶液。
K2Cr2O7标准溶液。①称量时,需用到的仪器有

②根据计算,选用的容量瓶规格应为
A.100mL B.250mL C.500mL D.1000mL
(4)步骤2用下图所示装置制备
 。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
止水夹关闭前后,通入N2的作用分别为
(5)步骤3的反应原理为:
 。反应中每消耗34gH2O2,转移的电子数为
。反应中每消耗34gH2O2,转移的电子数为(6)步骤4在不同时刻得到的Fe3O4粒径大小如下图所示。

①实验过程中,Fe3O4不易形成沉淀,结合上图分析原因
②写出一种可使Fe3O4较快形成沉淀的方法
您最近半年使用:0次
8 . 下列关于铁及其化合物的说法,正确的是
| A.Fe具有氧化性 | B.Fe2O3为黑色固体 |
| C.用KSCN溶液来检验Fe3+ | D.用铁桶盛放CuSO4溶液 |
您最近半年使用:0次
解题方法
9 . 铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有_____ 元素。
(2)铁元素有三种常见的氧化物,分别是FeO、 、
、 。其中具有磁性的是
。其中具有磁性的是_____ ,可作红色颜料的是_____ 。
(3)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为_____ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,此过程中利用了维生素C的_____ 性。
(4) 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。向反应后的溶液中加入_____ ,可回收Cu,并得到 溶液。
溶液。
Ⅱ.高铁酸钾( )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
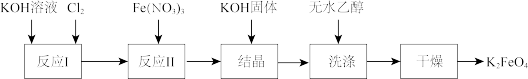
(5)下列说法错误的是_____。
(6)用电解饱和食盐水获得原料氯气的过程中有2mol电子发生转移,试计算理论上最多可制得氯气的体积(标准状况)是_____ L。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有
(2)铁元素有三种常见的氧化物,分别是FeO、
 、
、 。其中具有磁性的是
。其中具有磁性的是(3)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为(4)
 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为 溶液。
溶液。Ⅱ.高铁酸钾(
 )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
(5)下列说法错误的是_____。
A. 中铁元素的化合价为+6价 中铁元素的化合价为+6价 |
| B.用无水乙醇洗涤可以减少产品的损耗 |
C.反应Ⅱ中的氧化剂是 |
| D.高铁酸根离子具有强氧化性,能杀菌消毒 |
您最近半年使用:0次
名校
解题方法
10 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。日常生活中可通过食物摄入铁元素,例如黑木耳中就含有比较丰富的铁元素。某研究性学习小组为测定某地黑木耳中铁的含量,开展了如下研究与实践活动。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取a g黑木耳,洗净切碎,用蒸水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取a g黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。

回答下列问题:
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质___________ 溶于水(选填“能”或“不能”)。
(2)取少量滤液于试管中,滴入KSCN溶液,溶液变红。则滤液中铁元素的存在形式有 、
、___________ (填离子符号)。
(3)滤液与Fe生成A的离子方程式是___________ 。
(4)由A转化为B可加入的试剂X可以是___________ (填字母)
a. (
( ) b.
) b. c.
c.
(5)由C转化成D的现象是:白色沉淀迅速变为灰绿色,最终变为___________ 。
(6)将a g黑木耳中的铁元素经流程A→C-D进行完全转化,将D经过一系列处理,得到b g红棕色固体。若流程中加入的铁反应掉c g,则该黑木耳中铁元素的质量分数为___________ (用含a、b、c的代数式表示)。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取a g黑木耳,洗净切碎,用蒸水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取a g黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。

回答下列问题:
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质
(2)取少量滤液于试管中,滴入KSCN溶液,溶液变红。则滤液中铁元素的存在形式有
 、
、(3)滤液与Fe生成A的离子方程式是
(4)由A转化为B可加入的试剂X可以是
a.
 (
( ) b.
) b. c.
c.
(5)由C转化成D的现象是:白色沉淀迅速变为灰绿色,最终变为
(6)将a g黑木耳中的铁元素经流程A→C-D进行完全转化,将D经过一系列处理,得到b g红棕色固体。若流程中加入的铁反应掉c g,则该黑木耳中铁元素的质量分数为
您最近半年使用:0次
2023-09-20更新
|
222次组卷
|
2卷引用:云南省2023年春季学期期末普通高中学业水平考试化学试题



