1 . 下列实验现象描述正确的是
| A.KOH溶液中滴加酚酞试液,一段时间后溶液呈无色 |
| B.新制Cu(OH)2悬浊液中加入葡萄糖溶液并加热,产生砖红色沉淀 |
| C.FeCl3溶液中滴入KSCN溶液,溶液呈蓝色 |
| D.H2在Cl2中燃烧,发出黄色火焰 |
您最近一年使用:0次
解题方法
2 . 某化学兴趣小组为制取氯气并探究其性质,按下列装置(部分夹持仪器已略去)进行实验。
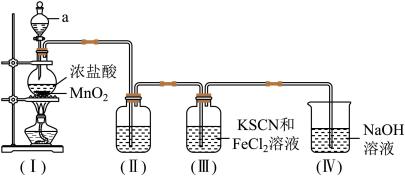
【装置(I)中发生反应的化学方程式:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O】
MnCl2+Cl2↑+2H2O】
【实验探究】
(1)装置(I)中仪器a的名称是___________ 。
(2)为除去Cl2中混有的HCl气体,装置(II)中的溶液是_________ (填“饱和食盐水”或“浓硫酸”)
(3)实验进行一段时间后,装置(III)中溶液颜色变为___________ (填“红色”或“紫色”),该反应中Cl2表现出___________ (填“氧化性”或“还原性”)。
(4)装置(IV)中NaOH溶液的作用是___________ 。
(5)若要生成标准状况下2.24LCl2,理论上参加反应的MnO2的质量是___________ g。(MnO2的摩尔质量为87g·mol-1)
【实验拓展】
(6)图是探究Cl2性质的微型实验,a处是湿润的红纸,b处是浸有淀粉KI溶液的滤纸。向KClO3晶体中滴加浓盐酸后,立即用另一培养皿扣在上面。
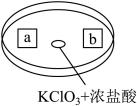
已知:KC1O3+6HCl(浓)=KC1+3C12↑+3H2O
回答下列问题:
①a处湿润的红纸___________ (填“褪色”或“不褪色”)
②b处滤纸变蓝色,写出Cl2与KI反应的化学方程式:___________
【知识应用】
(7)84消毒液(有效成分是NaClO)是常用的消毒剂,NaClO与水和空气里的二氧化碳反应生成___________ 可以消毒杀菌;84消毒液与洁厕灵(其中含盐酸)混合使用会发生反应,补充完整该反应的化学方程式:NaClO+2HCl=NaCl+___________ ↑+H2O。

【装置(I)中发生反应的化学方程式:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O】
MnCl2+Cl2↑+2H2O】【实验探究】
(1)装置(I)中仪器a的名称是
(2)为除去Cl2中混有的HCl气体,装置(II)中的溶液是
(3)实验进行一段时间后,装置(III)中溶液颜色变为
(4)装置(IV)中NaOH溶液的作用是
(5)若要生成标准状况下2.24LCl2,理论上参加反应的MnO2的质量是
【实验拓展】
(6)图是探究Cl2性质的微型实验,a处是湿润的红纸,b处是浸有淀粉KI溶液的滤纸。向KClO3晶体中滴加浓盐酸后,立即用另一培养皿扣在上面。

已知:KC1O3+6HCl(浓)=KC1+3C12↑+3H2O
回答下列问题:
①a处湿润的红纸
②b处滤纸变蓝色,写出Cl2与KI反应的化学方程式:
【知识应用】
(7)84消毒液(有效成分是NaClO)是常用的消毒剂,NaClO与水和空气里的二氧化碳反应生成
您最近一年使用:0次
名校
解题方法
3 . 印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,FeCl2 3.0 mol/L,FeCl3 1.0 mol/L,HCl 3.0 mol/L。取废腐蚀液200 mL按如下流程在实验室进行实验:

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显_______ (填“红色”或“蓝色”、“紫色”),证明废液含有FeCl3。
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是_______ (填化学式)。
(3)操作Ⅰ是_______ ,该操作需用到的玻璃仪器有烧杯、普通漏斗和_______ 。
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为_______ 。
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生_______ (填“是”、“否”)。

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是
(3)操作Ⅰ是
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生
您最近一年使用:0次
名校
解题方法
4 . 下列实验现象描述正确的是
| A.FeCl3溶液中滴入KSCN溶液,溶液呈蓝色 |
| B.新制Cu(OH)2悬浊液中加入葡萄糖溶液并加热,产生砖红色沉淀 |
| C.NaOH溶液中滴入酚酞试液,溶液呈无色 |
| D.品红溶液中通入SO2气体,溶液呈紫色 |
您最近一年使用:0次
5 . 下列实验过程中,观察不到 颜色变化的是
| A.二氧化硫通入品红溶液中 | B.氢氧化钾溶液中滴加稀盐酸 |
| C.乙烯通入溴的四氯化碳溶液中 | D.氯化铁溶液中滴入 溶液 溶液 |
您最近一年使用:0次
2022-01-01更新
|
343次组卷
|
2卷引用:2021年6月福建省普通高中学业水平合格性考试化学试题
6 . 为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号 填入对应的空格。
供选择的化学试剂或实验方法有:A.加热B.溶解、过滤、蒸发、结晶C.取样,滴加KSCN溶液,观察现象D.将气体通入盛有饱和食盐水的洗气瓶
供选择的化学试剂或实验方法有:A.加热B.溶解、过滤、蒸发、结晶C.取样,滴加KSCN溶液,观察现象D.将气体通入盛有饱和食盐水的洗气瓶
| 序号 | 实验目的 | 试剂或方法 |
(1) | 除去Cl2中混有少量的HCl | |
(2) | 检验Fe2+溶液中是否含有少量Fe3+ | |
(3) | 除去Na2CO3固体中混有的NaHCO3 | |
(4) | 分离Na2SO4和BaSO4固体混合物 |
您最近一年使用:0次
2020-11-27更新
|
226次组卷
|
2卷引用:福建省上杭县第一中学2021-2022学年高一下学期第二次学业水平模拟考试化学试题
名校
7 . 电子工业上常用氯化铁溶液做印刷电路铜板的腐蚀液,使用过的腐蚀废液中的金属离子主要有Fe3+、Fe2+和Cu2+。化学兴趣小组设计如下流程对废液进行处理并回收氯化铁溶液。
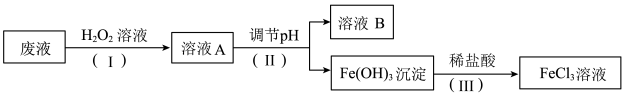
(1)步骤(Ⅰ)中加入H2O2溶液的目的是将Fe2+___ (填“氧化”或“还原”)成Fe3+;取少量溶液A于试管中,滴入1~2滴KSCN溶液,溶液显___ (填“红色”或“蓝色”)。
(2)步骤(Ⅱ)中分离溶液B和沉淀的操作名称是___ ;该操作需用到的玻璃仪器有烧杯、普通漏斗和___ 。
(3)写出步骤(Ⅲ)中Fe(OH)3与稀盐酸反应的化学方程式:____ 。

(1)步骤(Ⅰ)中加入H2O2溶液的目的是将Fe2+
(2)步骤(Ⅱ)中分离溶液B和沉淀的操作名称是
(3)写出步骤(Ⅲ)中Fe(OH)3与稀盐酸反应的化学方程式:
您最近一年使用:0次
2019-10-04更新
|
356次组卷
|
2卷引用:2019年6月福建省普通高中学业水平合格性考试化学试题



