名校
解题方法
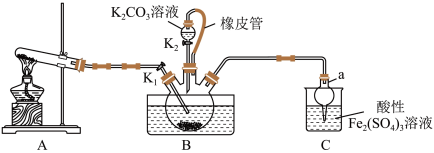
1 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: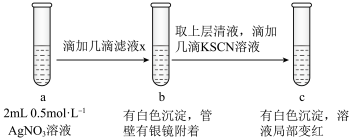
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
名校
解题方法
2 . 下列反应对应的离子方程式正确的是
A.实验室用氨水与氯化铝溶液反应制取 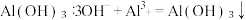 |
B.84 消毒液与洁厕灵混用产生有毒气体:  |
C.用浓氯化铁溶液制作印刷电路板:  |
D.硫氰化钾溶液与氯化铁溶液反应: 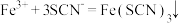 |
您最近一年使用:0次
3 . 某学习小组欲探究氯气与铁的反应及产物中铁元素的价态,设计并实施了以下实验.
已知: 的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.
的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.
Ⅰ.氯气与铁的反应
按下图连接装置并进行制备实验.
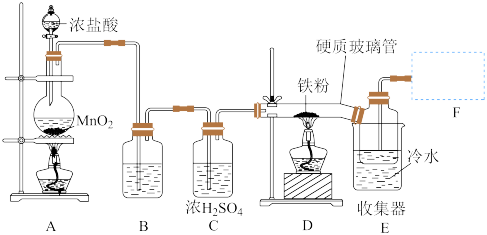
(1)按上图连接好装置,在进行______ 操作后,在各仪器中装入对应的试剂;开始反应时,应先点燃______ 装置的酒精灯(填“A”或“D”)。
(2)写出A中反应的离子方程式______ 。
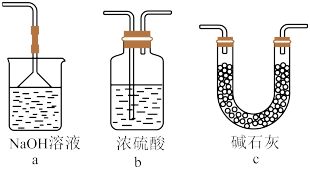
(3)装置B的作用是______ .F应连接的装置是______ (选择其中一个装置,填相应的字母)。
Ⅱ.产物中铁元素价态探究
反应结束后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,该小组设计了以下实验探究产物中铁元素的价态.
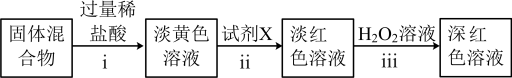
(4)步骤ⅱ添加的试剂X为______ 。
(5)步骤ⅲ中所发生的离子反应方程式为______ 。
(6)通过以上实验及现象,该小组同学认为氯气与铁的反应产物中包含+2和+3价的两种铁盐.实验结论是否正确?请进行判断并说明理由______ 。
已知:
 的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.
的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解.Ⅰ.氯气与铁的反应
按下图连接装置并进行制备实验.

(1)按上图连接好装置,在进行
(2)写出A中反应的离子方程式
(3)装置B的作用是

Ⅱ.产物中铁元素价态探究
反应结束后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,该小组设计了以下实验探究产物中铁元素的价态.

(4)步骤ⅱ添加的试剂X为
(5)步骤ⅲ中所发生的离子反应方程式为
(6)通过以上实验及现象,该小组同学认为氯气与铁的反应产物中包含+2和+3价的两种铁盐.实验结论是否正确?请进行判断并说明理由
您最近一年使用:0次
名校
解题方法
4 . 下列转化必须加入氧化剂才能实现的是
A. | B.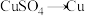 |
C.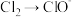 | D. |
您最近一年使用:0次
5 . 武夷山“大红袍”素有“茶中之王”的美誉。检验茶叶中是否含铁元素的操作方案如图所示,下列叙述错误 的是


| A.“操作①”应在蒸发血中灼烧 |
| B.“操作②”用热水可加快溶解速率 |
| C.“操作③”用到的玻璃仪器是漏斗、烧杯、玻璃棒 |
D.“操作④”若检验过程中没有发现 ,则不含铁元素 ,则不含铁元素 |
您最近一年使用:0次
名校
6 . 以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
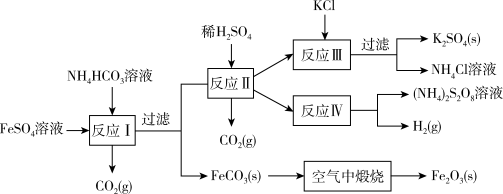
(1)反应Ⅰ前需在 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;
(2)反应Ⅰ需控制反应温度低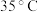 ,其目的是
,其目的是___________ 。
(3)反应Ⅳ常被用于电解生产 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为___________ 。
(4)反应Ⅰ的离子方程式为___________ 。
(5)空气中煅烧的化学方程式为___________ 。

(1)反应Ⅰ前需在
 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;| A.锌粉 | B.铁屑 | C. 溶液 溶液 | D. |
(2)反应Ⅰ需控制反应温度低
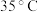 ,其目的是
,其目的是(3)反应Ⅳ常被用于电解生产
 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为(4)反应Ⅰ的离子方程式为
(5)空气中煅烧的化学方程式为
您最近一年使用:0次
7 . 常温下,下列各组离子在制定溶液中一定能大量共存的是
A. 的溶液: 的溶液: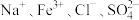 |
B.甲基橙呈红色的溶液: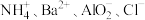 |
C.纯碱的稀溶液: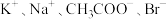 |
D.与铝反应产生大量氢气的溶液: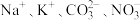 |
您最近一年使用:0次
8 . 柠檬酸亚铁是一种高效补铁剂。利用硫铁矿烧渣(主要含 及少量
及少量 、
、 )制备柠檬酸亚铁的工艺流程如图。
)制备柠檬酸亚铁的工艺流程如图。
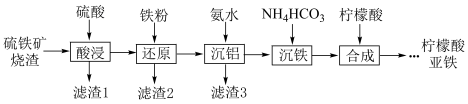
已知:常温下, 时
时 沉淀完全,
沉淀完全, 时
时 开始沉淀。
开始沉淀。
回答下列问题:
(1)滤渣1为________ (填化学式)。
(2)“还原”过程中发生反应的离子方程式为_______ 。检验“还原”过程中反应是否完全进行的试剂为_______ (填化学式)。
(3)“沉铝”过程应调节溶液的pH范围为_______ 。
(4)“沉铁”过程反应生成 和
和 的离子方程式为
的离子方程式为______ 。此过程需控制温度在35℃以下,可能原因是_______ 。
(5)“合成”过程中,需加入少量的抗氧化剂,下列试剂合适的是________(填标号)。
 及少量
及少量 、
、 )制备柠檬酸亚铁的工艺流程如图。
)制备柠檬酸亚铁的工艺流程如图。
已知:常温下,
 时
时 沉淀完全,
沉淀完全, 时
时 开始沉淀。
开始沉淀。回答下列问题:
(1)滤渣1为
(2)“还原”过程中发生反应的离子方程式为
(3)“沉铝”过程应调节溶液的pH范围为
(4)“沉铁”过程反应生成
 和
和 的离子方程式为
的离子方程式为(5)“合成”过程中,需加入少量的抗氧化剂,下列试剂合适的是________(填标号)。
A. | B.Fe | C.Cu | D. |
您最近一年使用:0次
9 . 某小组探究过量铁粉与硝酸酸化的 溶液反应过程中,溶液显黄色的原因,探究过程如下。
溶液反应过程中,溶液显黄色的原因,探究过程如下。
已知: 与
与 生成白色沉淀
生成白色沉淀 。
。
下列说法错误的是
 溶液反应过程中,溶液显黄色的原因,探究过程如下。
溶液反应过程中,溶液显黄色的原因,探究过程如下。| 编号 | 实验操作 | 实验现象 |
| 实验1 | 向硝酸酸化的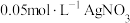 溶液( 溶液(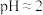 )中加入过量铁粉,搅拌后静置 )中加入过量铁粉,搅拌后静置 | 烧杯底部有黑色固体,约 后溶液明显变黄 后溶液明显变黄 |
| 实验2 | 在实验1中反应 、 、 和 和 时,分别取上层清液滴加等量 时,分别取上层清液滴加等量 溶液 溶液 |  时产生白色沉淀,溶液呈红色; 时产生白色沉淀,溶液呈红色; 时白色沉淀减少,溶液颜色加深; 时白色沉淀减少,溶液颜色加深; 时白色沉淀更少,溶液颜色较 时白色沉淀更少,溶液颜色较 更浅 更浅 |
| 实验3 | 向硝酸酸化的 溶液 溶液 中加入过量铁粉,搅拌后静置,分别取反应 中加入过量铁粉,搅拌后静置,分别取反应 和 和 时的上层清液滴加等量 时的上层清液滴加等量 溶液 溶液 |  时溶液呈浅红色; 时溶液呈浅红色; 时溶液颜色较 时溶液颜色较 时更浅 时更浅 |
 与
与 生成白色沉淀
生成白色沉淀 。
。下列说法错误的是
A.由实验1和实验2可知,黄色溶液中含有 |
B.由实验2的现象推断 颜色变浅是因为Fe还原 颜色变浅是因为Fe还原 |
C.由实验2和3可知 是溶液变黄的主要原因 是溶液变黄的主要原因 |
D.由上述实验可知溶液显黄色是因为 可氧化 可氧化 |
您最近一年使用:0次
解题方法
10 . 在酸性溶液里能大量共存的离子组是
A. 、 、 、 、 | B. 、 、 、 、 |
C. 、 、 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
2024-02-04更新
|
70次组卷
|
2卷引用:福建省南平市2023-2024学年高一上学期期末质量检测化学试题



