2024高三下·浙江·专题练习
解题方法
1 . 在溶液中能大量共存的离子组是
A.Fe3+、Mg2+、I-、NO | B.Mg2+、S2-、CO 、NH 、NH |
| C.Cu²+、SCN-、Cl-、K+ | D.Fe2+、K+、Na+、SO |
您最近一年使用:0次
2 . 某课题组为探究0.1 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:
实验一:
实验二: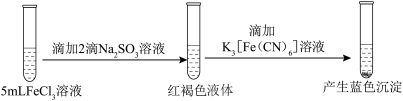
实验三: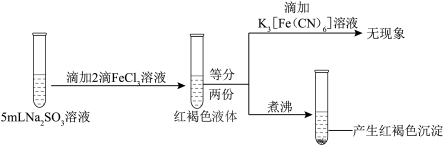
分析实验现象,下列说法中不合理的是
 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:实验一:

实验二:

实验三:

分析实验现象,下列说法中不合理的是
| A.实验一的红褐色液体可产生丁达尔效应 |
B.实验二说明 既发生了水解反应也被 既发生了水解反应也被 还原 还原 |
C.实验三说明 发生了水解反应但未被还原 发生了水解反应但未被还原 |
D.以上三个实验说明 对 对 的水解无影响 的水解无影响 |
您最近一年使用:0次
解题方法
3 . 某小组同学为探究FeSO4的性质设计了如下实验。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)
_______ g,其部分实验操作示意图如下,正确的步骤顺序为_______ (填序号)。
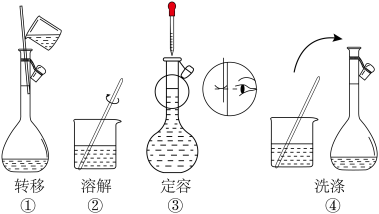
Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:
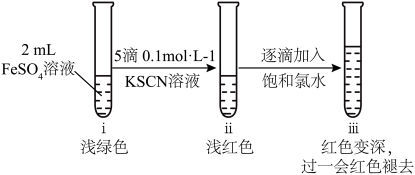
(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在_______ (填离子符号)。
(3)ⅲ中溶液红色变深的主要原因是_______ (用离子方程式表示)。
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
(4)乙同学的猜想是_______ 。为验证甲、乙两位同学的猜想,设计如下实验:将褪色后的溶液分为两等份,一份滴加KSCN溶液,呈血红色;另一份加入氯化铁溶液,无明显现象,则_______ 同学猜想是正确的。
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =_______ g,FeSO4固体在空气氛围中加热时反应的化学方程式为_______ 。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)

Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:

(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在
(3)ⅲ中溶液红色变深的主要原因是
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
| 猜想 | |
| 甲 | +3价铁又被还原成+2价铁 |
| 乙 |
(4)乙同学的猜想是
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =
您最近一年使用:0次
4 . 下列依据实验现象得出的实验结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将 和 和 分别通入滴有几滴紫色石蕊溶液的蒸馏水中 分别通入滴有几滴紫色石蕊溶液的蒸馏水中 | 溶液均变为红色 |  和 和 均是酸性氧化物 均是酸性氧化物 |
| B | 将铜粉加入1.0  溶液中 溶液中 | 溶液变蓝 | 金属铁比铜活泼 |
| C | 常温下,用pH计分别测定0.1 和1 和1  ,溶液的pH ,溶液的pH | pH均等于7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| D | 向两支盛有2mL相同物质的量浓度的银氨溶液的试管中分别加入3滴相同物质的量浓度的Nal和NaCl溶液 | 一支试管中产生黄色沉淀,另一支试管中无明显现象 |  > > |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 化合物甲(化学式可表示为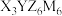 )是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是
)是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是
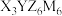 )是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是
)是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是A.第一电离能: |
| B.化合物甲中除含配位键,还含离子键、非极性键 |
C.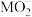 的VSEPR模型为三角形 的VSEPR模型为三角形 |
D.化合物甲的溶液可用于检验 |
您最近一年使用:0次
名校
6 . 根据实验操作、现象,所得结论错误的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将SO2分别通入品红的乙醇溶液和品红的水溶液 | 品红的乙醇溶液不褪色,品红的水溶液慢慢褪色 | 使品红褪色的不是SO2,而是SO2与水反应后的产物 |
| B | 将CO通过装有Fe2O3的硬质玻璃管,并对玻璃管加热 | 将所得产物溶于稀盐酸,再滴加KSCN溶液,溶液不变色 | Fe2O3完全被CO还原 |
| C | 以K2CrO4为指示剂,用AgNO3标准溶液滴定溶液中的Br- | 先出现浅黄色沉淀,后出现砖红色沉淀 | 无法确定Ksp(AgBr)和Ksp(Ag2CrO4)的大小 |
| D | 向淀粉溶液中加入适量稀硫酸,水浴加热。冷却至室温后加入NaOH溶液调至碱性,再加入新制氢氧化铜悬浊液,加热 | 试管中出现砖红色沉淀 | 淀粉发生了水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 实验是探究物质性质的重要方法,下列操作中,实验现象与得出的结论相一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 比较HClO和CH3COOH的酸性强弱 | 用pH计测定NaClO和CH3COONa的pH值,测得pH(NaClO)>pH(CH3COONa) | 酸性:HClO>CH3COOH |
| B | 验证反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 | 向2mL 0.1mol/L FeCl3溶液加入几滴0.1mol/L KI溶液,充分反应。取反应后试样,滴加淀粉溶液,溶液变为蓝色;另取反应后试样,加入KSCN溶液,溶液变成血红色 | 反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 |
| C | 判断 (AgCl)与 (AgCl)与 (AgI)的大小 (AgI)的大小 | 向等浓度的NaCl、NaI的混合溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| D | 判断某 溶液样品中是否含有 溶液样品中是否含有 | 向某 溶液样品中加入硫酸酸化的 溶液样品中加入硫酸酸化的 溶液,紫色褪去 溶液,紫色褪去 | 该样品中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 以含锌废液(主要成分为 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备 的实验流程如下。设
的实验流程如下。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备 的实验流程如下。设
的实验流程如下。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是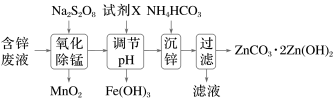
A.1mol过二硫酸钠( )中含有过氧键(-O-O-)数目为 )中含有过氧键(-O-O-)数目为 |
B.“氧化除锰”后的溶液中一定存在: 、 、 、 、 |
C.“调节pH”时试剂X可以选用Zn、ZnO、 等物质 等物质 |
D.“氧化除锰”过程中生成 的离子方程式: 的离子方程式: |
您最近一年使用:0次
名校
9 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作 | 结论 |
| A | 将铁锈溶于浓盐酸,再滴入 溶液,紫红色褪去 溶液,紫红色褪去 | 铁锈与浓盐酸反应生成亚铁离子 |
| B | 用洁净的铂丝蘸取溶液在火焰上灼烧,火焰呈黄色 | 溶液中一定有钠元素,可能有钾元素 |
| C | 向 和KSCN的混合溶液中滴入酸化的 和KSCN的混合溶液中滴入酸化的 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 |  的氧化性强于 的氧化性强于 |
| D | 将 通入 通入 溶液后,将混合气体依次通入酸性 溶液后,将混合气体依次通入酸性 溶液、品红溶液、澄清石灰水 溶液、品红溶液、澄清石灰水 | 验证非金属性:S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 为探究固体矿物X(仅含三种元素)的组成和性质,某学习小组进行了如图实验
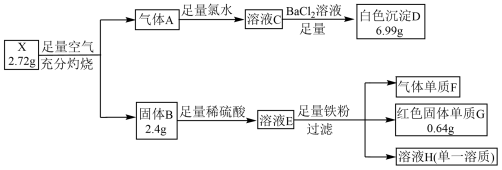
A.气体A→溶液C的离子方程式为:SO2+Cl2+2H2O= +2Cl-+4H+ +2Cl-+4H+ |
| B.X的化学式是CuFe2S3 |
| C.气体单质F为H2 |
| D.可以用Fe(SCN)3溶液来检验溶液H中的阳离子 |
您最近一年使用:0次



