1 . I.用黄铜矿(主要成分为 ,其中
,其中 为
为 价、
价、 为
为 价)制取铜和三氧化二铁的工艺流程如图所示:
价)制取铜和三氧化二铁的工艺流程如图所示:
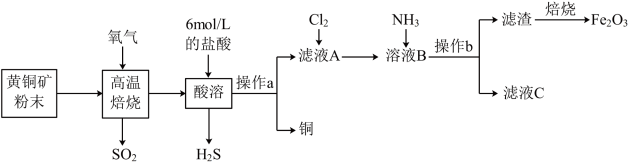
已知: ;
;
(1)将黄铜矿粉碎成粉末的目的是___________ 。高温焙烧反应的还原产物是___________ 。
(2)滤液A中通入 的离子方程式为
的离子方程式为___________ 。
(3)操作b后检验滤渣已经洗涤干净的实验操作为___________ 。
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如下实验:
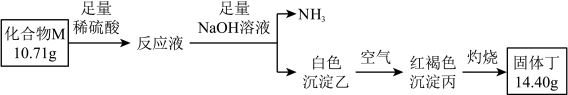
已知: 为白色难溶于水的固体,极容易被氧化。
为白色难溶于水的固体,极容易被氧化。
(4) 的化学式为
的化学式为___________ 。
(5)白色沉淀乙在空气中变成红褐色沉淀丙的原因是___________ (用化学方程式表示)
(6)高温条件下,丁与 反应生成两种单质和水,该反应的化学方程式为
反应生成两种单质和水,该反应的化学方程式为___________ 。
 ,其中
,其中 为
为 价、
价、 为
为 价)制取铜和三氧化二铁的工艺流程如图所示:
价)制取铜和三氧化二铁的工艺流程如图所示:
已知:
 ;
;(1)将黄铜矿粉碎成粉末的目的是
(2)滤液A中通入
 的离子方程式为
的离子方程式为(3)操作b后检验滤渣已经洗涤干净的实验操作为
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如下实验:

已知:
 为白色难溶于水的固体,极容易被氧化。
为白色难溶于水的固体,极容易被氧化。(4)
 的化学式为
的化学式为(5)白色沉淀乙在空气中变成红褐色沉淀丙的原因是
(6)高温条件下,丁与
 反应生成两种单质和水,该反应的化学方程式为
反应生成两种单质和水,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . 某小组为探究 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。

(1)在实验进行的过程中,应该持续通入氮气的目的是___________ 。
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明 的热分解产物中一定含有
的热分解产物中一定含有___________ 。
(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入 溶液变红,说明
溶液变红,说明___________ 。
(4)已知: 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
完成下列小题:
①若反应后 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸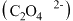 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式___________ 。
②据此计算出该 固体的纯度为
固体的纯度为___________ (保留一位有效数字) 。
③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是___________ 。
 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(1)在实验进行的过程中,应该持续通入氮气的目的是
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明
 的热分解产物中一定含有
的热分解产物中一定含有(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入
 溶液变红,说明
溶液变红,说明(4)已知:
 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。完成下列小题:
①若反应后
 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸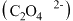 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式②据此计算出该
 固体的纯度为
固体的纯度为③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴
 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是
您最近一年使用:0次
名校
解题方法
3 .  溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓
溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓 得溶液 b,溶液b较溶液 a黄色加深。已知:
得溶液 b,溶液b较溶液 a黄色加深。已知: (黄色);浓度较小时
(黄色);浓度较小时  (用
(用 表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
 溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓
溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓 得溶液 b,溶液b较溶液 a黄色加深。已知:
得溶液 b,溶液b较溶液 a黄色加深。已知: (黄色);浓度较小时
(黄色);浓度较小时  (用
(用 表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
表示)几乎无色。取溶液进行如下实验,对现象分析错误的是A.测溶液 a的  约为1.3,证明 约为1.3,证明  发生了水解 发生了水解 |
B.向 b中加入  后,会产生白色沉淀 后,会产生白色沉淀 |
C.向 b中滴入  溶液变血红色,说明 溶液变血红色,说明  的配位键稳定性大于 的配位键稳定性大于  |
D.将溶液 a稀释,颜色变浅,主要是因为  浓度降低导致 浓度降低导致 |
您最近一年使用:0次
2024-01-31更新
|
207次组卷
|
4卷引用:黑龙江省哈尔滨市第九中学校2023-2024学年高二上学期期末考试化学试卷
4 . 用富含铁元素的食品,可以补充人体所需的铁元素。某班级研究性学习小组对菠菜中的铁元素展开了检测,实验如下:

(1)下列图示装置或操作合理的是________ 。
(2)写出试剂B的化学式___________ 。
(3)试剂C若为双氧水,请写出该反应的离子方程式:___________ ;该实验证明菠菜中含有的铁元素为_____ 价。
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?______ ,原因是什么?___________ 。
(5)另取少量滤液 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是________ ;原因是___________ 、________ (用离子方程式解释)。

(1)下列图示装置或操作合理的是
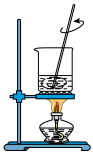 | 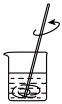 | 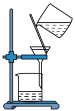 |  |
| A.灼烧 | B.溶解 | C.过滤 | D.检测菠菜液中的铁元素 |
(2)写出试剂B的化学式
(3)试剂C若为双氧水,请写出该反应的离子方程式:
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?
(5)另取少量滤液
 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是
您最近一年使用:0次
5 . 高铁酸钾(K2FeO4)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程:
回答下列问题:
(1)写出①中发生反应的离子方程式:___________ 。
(2)②中加入NaOH固体的目的是___________(填字母序号)。
(3)完成④中反应的离子方程式:___________ ,氧化剂与氧化产物的物质的量之比为___________ ;若反应每生成lmol 转移电子的数目为:
转移电子的数目为:___________ 。
(4)从溶液II中得到K2FeO4晶体的操作是___________ 、洗涤、千燥。
(5)⑥中洗涤时,洗涤剂最好选用___________(填字母序号)。

| 溶解性 | 溶于水,微溶于浓KOH溶液,难溶于有机物 |
| 稳定性 | 温度为0~5℃或强碱性溶液中能稳定存在;酸性或中性溶液中放出O2 |
(1)写出①中发生反应的离子方程式:
(2)②中加入NaOH固体的目的是___________(填字母序号)。
| A.为后续反应提供碱性环境 |
| B.加入NaOH固体做氧化剂有利于除去NaCl |
| C.NaOH固体溶解时会放出较多的热量,有利于后续生成K2FeO4 |
| D.与溶液I中过量的Cl2继续反应,生成更多的NaClO |
(3)完成④中反应的离子方程式:
 转移电子的数目为:
转移电子的数目为:(4)从溶液II中得到K2FeO4晶体的操作是
(5)⑥中洗涤时,洗涤剂最好选用___________(填字母序号)。
| A.KOH溶液 | B.乙醇 | C.H2O | D.FeCl2溶液 |
您最近一年使用:0次
名校
解题方法
6 . 某化学兴趣小组探究 和
和 的化学性质。
的化学性质。
Ⅰ.实验准备:饱和氯水的制备
(1)图中仪器A的名称为___________ 。___________ 。
(3)实验室最适合用于处理多余氯气的是___________ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
Ⅱ.实验探究
①取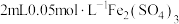 溶液于试管中,滴加3滴
溶液于试管中,滴加3滴 溶液,溶液变红色;
溶液,溶液变红色;
②取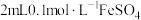 溶液于试管中,先滴加3滴
溶液于试管中,先滴加3滴 溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
【发现问题】小组成员针对实验②中溶液未变红色,而呈现黄色的现象展开了探究。
【查阅文献】
i. 能将
能将 氧化成
氧化成 ,硫氰
,硫氰 常温下为黄色液体,易挥发,可与水发生反应:
常温下为黄色液体,易挥发,可与水发生反应: ;
;
ii.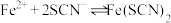 ,
,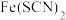 为无色配合物。
为无色配合物。
【提出猜想】猜想一 被氯水氧化成
被氯水氧化成 ,使溶液呈黄色;
,使溶液呈黄色;
猜想二 加入氯水后部分 被氧化为
被氧化为 ,
, (红色),但由于存在反应:
(红色),但由于存在反应: ,实验②生成的
,实验②生成的 浓度比实验①的小,
浓度比实验①的小, 溶液在浓度较低时呈黄色。
溶液在浓度较低时呈黄色。
【验证猜想】
(4)为验证猜想,小组成员设计了以下实验,请补充表格中的操作及现象
【提出质疑】
(5)甲同学提出,实验④并不能证明猜想一正确,理由是___________ 。
【再次探究】
(6)小组成员进行进一步探究,请完成表格中的实验操作及现象
【得出结论】
(7)由实验结论可以判断:本实验条件下还原性强弱:
___________  (填“强于”“弱于”或“等于”)。
(填“强于”“弱于”或“等于”)。
 和
和 的化学性质。
的化学性质。Ⅰ.实验准备:饱和氯水的制备
(1)图中仪器A的名称为
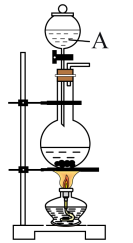
(3)实验室最适合用于处理多余氯气的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液Ⅱ.实验探究
①取
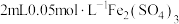 溶液于试管中,滴加3滴
溶液于试管中,滴加3滴 溶液,溶液变红色;
溶液,溶液变红色;②取
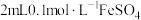 溶液于试管中,先滴加3滴
溶液于试管中,先滴加3滴 溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。【发现问题】小组成员针对实验②中溶液未变红色,而呈现黄色的现象展开了探究。
【查阅文献】
i.
 能将
能将 氧化成
氧化成 ,硫氰
,硫氰 常温下为黄色液体,易挥发,可与水发生反应:
常温下为黄色液体,易挥发,可与水发生反应: ;
;ii.
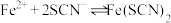 ,
,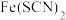 为无色配合物。
为无色配合物。【提出猜想】猜想一
 被氯水氧化成
被氯水氧化成 ,使溶液呈黄色;
,使溶液呈黄色;猜想二 加入氯水后部分
 被氧化为
被氧化为 ,
, (红色),但由于存在反应:
(红色),但由于存在反应: ,实验②生成的
,实验②生成的 浓度比实验①的小,
浓度比实验①的小, 溶液在浓度较低时呈黄色。
溶液在浓度较低时呈黄色。【验证猜想】
(4)为验证猜想,小组成员设计了以下实验,请补充表格中的操作及现象
| 实验序号 | 实验操作 | 现象 | 实验结论 |
| ③ | 取少量实验①的溶液于试管中, | 猜想二正确 | |
| ④ | 取少量实验②的溶液于试管中,滴加3滴饱和 溶液 溶液 | 溶液变浑浊 | 猜想一也正确 |
【提出质疑】
(5)甲同学提出,实验④并不能证明猜想一正确,理由是
【再次探究】
(6)小组成员进行进一步探究,请完成表格中的实验操作及现象
| 实验序号 | 实验操作 | 现象 |
| ⑤ | 滴加3滴蒸馏水 | 无明显现象 | |
| ⑥ | 无明显现象 | ||
| ⑦ | 滴加3滴饱和氯水 | 溶液变橙红色 | |
| ⑧ | 滴加3滴 溶液 溶液 | ||
| 得出结论 | i.由实验⑥的现象可以判断:猜想一不正确, ii.结合实验⑤⑦⑧的现象可以判断:猜想二正确。 | ||
【得出结论】
(7)由实验结论可以判断:本实验条件下还原性强弱:

 (填“强于”“弱于”或“等于”)。
(填“强于”“弱于”或“等于”)。
您最近一年使用:0次
2024-01-22更新
|
457次组卷
|
3卷引用:广东省深圳市龙岗区2023-2024学年高三上学期1月期末考试化学试题
广东省深圳市龙岗区2023-2024学年高三上学期1月期末考试化学试题(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题
7 . 已知在酸性条件下,Cu+能发生如下转化:2Cu+→Cu+Cu2+现将amol的Cu2O投入到500mL含有bmolFeCl3和bmolH2SO4的混合溶液中。下列说法不正确的是
| A.当b≥2a时,发生的离子反应为Cu2O+2Fe3++2H+═2Fe2++2Cu2++H2O |
B.当b≥a 时,反应中转移电子的物质的量为n(e-)=(a 时,反应中转移电子的物质的量为n(e-)=(a )mol )mol |
C.当a≥b时,溶液中Fe2+、Cu2+、Cl-、 的物质的量之比为2:3:6:2 的物质的量之比为2:3:6:2 |
D.当 a≤b时,溶液中c(Cu2+):c(Fe2+)=1:1.生成单质铜的质量为64(a a≤b时,溶液中c(Cu2+):c(Fe2+)=1:1.生成单质铜的质量为64(a )g )g |
您最近一年使用:0次
解题方法
8 . 根据实验操作及现象,得出结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A |  和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体 和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体 | 硫酸表现氧化性, 表现还原性 表现还原性 |
| B | 向酸性 溶液中滴加乙苯,溶液褪色 溶液中滴加乙苯,溶液褪色 | 乙苯的苯环中含有碳碳双键 |
| C | Ag与HI溶液生成黄色沉淀和无色气体 |  和 和 生成AgI,促进Ag和HI溶液发生反应生成AgI和 生成AgI,促进Ag和HI溶液发生反应生成AgI和 |
| D | 在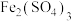 溶液中加入铜粉,溶液变蓝色 溶液中加入铜粉,溶液变蓝色 | 氧化性: , ,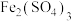 和Cu发生置换反应 和Cu发生置换反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 某实验小组探究Fe2+与H2O2反应中滴加KSCN溶液变红色后又褪色的原因,提出如下假设:
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
| 实验 | 滴加试剂 | 现象 |
| I | i.向2mLFeCl2溶液中滴加2滴0.1mol·L-1KSCN溶液 ii.再滴加5滴5%H2O2溶液(物质的量浓度约为1.5mol·L-1、pH约为5) | i.无明显现象 ii.溶液变红,大约10秒左右红色褪去,并测得生成了两种可直接排放到空气中的气体 |
| II | iii.取褪色后溶液两份,一份滴加FeC13溶液;另一份滴加KSCN溶液 iV.取褪色后溶液,滴加盐酸和BaCl2溶液 | iii.一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色 iV.产生白色沉淀 |
| III | V.向2mL0.1mol·L-1FeCl3溶液中滴加2滴0.1mol·L-1KSCN溶液,观察现象;后通入O2,观察现象 | V.先变红,通入氧气后无明显变化 |
| A.实验I褪色后的溶液中n(H+)变小 | B.通过实验II、III可验证假设c正确 |
C.实验II证明SCN-被氧化成SO | D.实验III的目的是排除假设b |
您最近一年使用:0次
10 . 室温下,下列探究方案能达到探究目的的是
| 序号 | 探究方案 | 探究目的 |
| ① | 用不同浓度、等体积的 溶液分别与相同浓度相同体积的 溶液分别与相同浓度相同体积的 溶液反应,观察现象 溶液反应,观察现象 | 探究浓度对反应速率的影响 |
| ② | 用pH计测定同浓度NaClO和NaF溶液的pH,比较溶液pH大小 | 比较HClO与HF的酸性强弱 |
| ③ | 向 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 | 比较CuS和ZnS的溶度积( )的大小 )的大小 |
| ④ | 向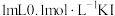 溶液中加入 溶液中加入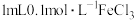 溶液,充分反应后,再加KSCN,观察溶液颜色变化 溶液,充分反应后,再加KSCN,观察溶液颜色变化 | 探究 是否完全反应 是否完全反应 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次




