名校
1 . 化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A. | Na2O2常用于潜水艇或呼吸面具的供氧剂 | Na2O2与CO2反应产生O2 |
| B. | Al2O3常用作耐火材料 | Al2O3熔点高 |
| C. | FeCl3溶液可用于刻制 印刷铜电路板 | FeCl3与Cu发生反应2Fe3++Cu=2Fe2++Cu2+ |
| D. | Al(OH)3可作为治疗胃酸过多的内服药 | 这是利用氢氧化铝的两性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-01-21更新
|
645次组卷
|
2卷引用:甘肃省嘉峪关市酒钢三中2017-2018学年高一上学期第二次月考化学试题
名校
解题方法
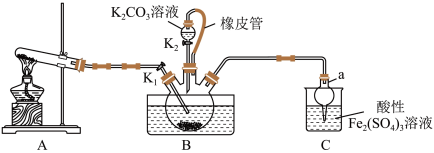
2 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: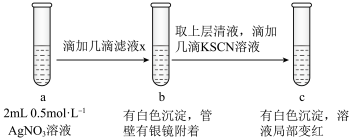
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
解题方法
3 . I.由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4·7H2O),然后制取透明氧化铁颜料的流程如下:
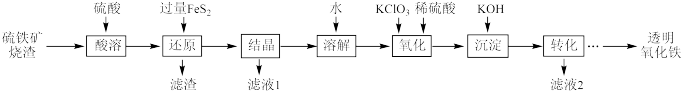
已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为___________ 。
(2)“滤渣”中的主要成分是___________ 。
(3)“还原”过程中涉及的离子方程式为___________ 。
(4)流程中“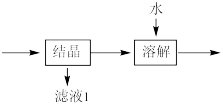 ”环节的目的是
”环节的目的是___________ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以___________ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:
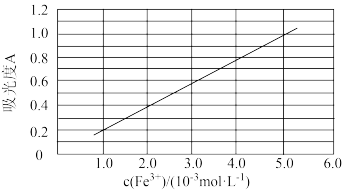
称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红(Fe2O3)的质量分数为___________ %(保留小数点后一位)。
Ⅱ.氧化亚铜(Cu2O)用途广泛,干法生产Cu2O粉末的主要工艺流程如下:
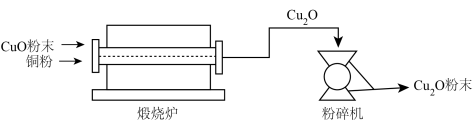
(7)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(8)800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。

已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为
(2)“滤渣”中的主要成分是
(3)“还原”过程中涉及的离子方程式为
(4)流程中“
 ”环节的目的是
”环节的目的是(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红(Fe2O3)的质量分数为
Ⅱ.氧化亚铜(Cu2O)用途广泛,干法生产Cu2O粉末的主要工艺流程如下:

(7)粉碎机中,发生的变化属于
(8)800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为
您最近一年使用:0次
解题方法
4 . 某小组同学探究盐对Fe3+ +3SCN- Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。
实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。
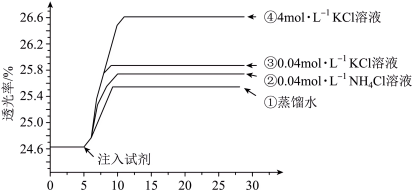
已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1- [FeCl4]-(黄色);
[FeCl4]-(黄色);
ii.Fe3+与NO 不能形成配位化合物;
不能形成配位化合物;
iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要___________ ,用稀盐酸酸化FeCl3溶液的目的是___________ 。
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN- Fe(SCN)3平衡向
Fe(SCN)3平衡向___________ (填“正”或“逆”)反应方向移动。
(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因___________ 。
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是___________ 导致的(答出一种影响因素即可,不需详细说明理由)。
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为___________ (填离子符号),试分析该离子盐效应对Fe3+和SCN-平衡体系有影响的原因___________ 。
(6)拓展应用:盐效应对多种平衡体系有影响。
分析c(Na2SO4)在0~0.20 mol·L-1范围内,PbSO4溶解度发生变化的原因:___________ 。
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途___________ 。
 Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1-
 [FeCl4]-(黄色);
[FeCl4]-(黄色);ii.Fe3+与NO
 不能形成配位化合物;
不能形成配位化合物;iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN-
 Fe(SCN)3平衡向
Fe(SCN)3平衡向(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
| 序号 | 加入试剂 | 溶液透光率 |
| 1 | 1 mL蒸馏水 | A1 |
| 2 | 1 mL 3 mol·L-1 KNO3 | A2 |
| 3 | 1 mL 3 mol·L-1 NaNO3 | A3 |
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为
(6)拓展应用:盐效应对多种平衡体系有影响。
| c(Na2SO4)/(mol·L-1) | 0 | 0.01 | 0.02 | 0.04 | 0.10 | 0.20 |
| PbSO4溶解度/mg | 4.5 | 0.48 | 0.42 | 0.39 | 0.48 | 0.69 |
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途
您最近一年使用:0次
解题方法
5 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有 、
、 、FeO、
、FeO、 等)来制备绿矾(
等)来制备绿矾( )和氧化铝,其工艺流程如图:
)和氧化铝,其工艺流程如图:
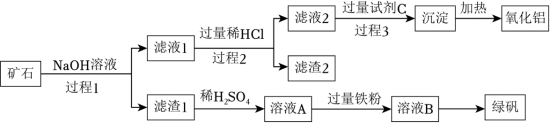
回答下列问题:
(1)过程1中能加快矿石与NaOH溶液反应速率的措施是___________ 。(答一条)
(2)滤渣1的主要成分是___________ ,举例说明滤渣2的用途___________ 。
(3)向溶液A中加入过量铁粉发生反应的离子方程式为:___________ 。
(4)写出由滤液1生成滤液2的离子方程式___________ 。
(5)用来配制试剂C的物质的电子式为:___________ 。
(6)绿矾晶体易被空气中的氧气氧化变质,宜密封保存放置。为探究制备的绿矾样品是否变质,具体的实验操作为___________ 。
 、
、 、FeO、
、FeO、 等)来制备绿矾(
等)来制备绿矾( )和氧化铝,其工艺流程如图:
)和氧化铝,其工艺流程如图:
回答下列问题:
(1)过程1中能加快矿石与NaOH溶液反应速率的措施是
(2)滤渣1的主要成分是
(3)向溶液A中加入过量铁粉发生反应的离子方程式为:
(4)写出由滤液1生成滤液2的离子方程式
(5)用来配制试剂C的物质的电子式为:
(6)绿矾晶体易被空气中的氧气氧化变质,宜密封保存放置。为探究制备的绿矾样品是否变质,具体的实验操作为
您最近一年使用:0次
解题方法
6 . 黑色金属材料是工业上对铁、铬、锰的统称, 、
、 、
、 及其化合物在日常生活生产中的用途相当广泛。
及其化合物在日常生活生产中的用途相当广泛。
Ⅰ. 根据所学知识,回答下列问题:
(1) 具有净水作用,
具有净水作用, 净水的原理是
净水的原理是_______ 。
(2)向 溶液中加入
溶液中加入 溶液至过量,微热。再通入
溶液至过量,微热。再通入 ,可观察到溶液呈紫色(高铁酸钾:
,可观察到溶液呈紫色(高铁酸钾: )。写出此过程发生反应的离子方程式:
)。写出此过程发生反应的离子方程式:_______ 。
(3) 可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用
可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用 配制成溶液,并取
配制成溶液,并取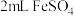 溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向
溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向 溶液和
溶液和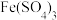 溶液中分别通入
溶液中分别通入 ,观察到
,观察到 溶液变为深棕色,
溶液变为深棕色,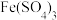 溶液无明显变化。
溶液无明显变化。
①“试管中产生红棕色气体,溶液变为深棕色”的原因是_______ 。
②实验小组改进实验,观察到溶液变为黄色的实验操作是_______ 。
Ⅱ.在 溶液中存在下列平衡:
溶液中存在下列平衡: 。
。
(4)下列有关 溶液的说法正确的是_______(填标号)。
溶液的说法正确的是_______(填标号)。
Ⅲ. 可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。

(5) 时,剩余固体中
时,剩余固体中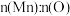 为
为_______ 。
(6)图中C点对应固体的成分为_______ (填化学式)。
 、
、 、
、 及其化合物在日常生活生产中的用途相当广泛。
及其化合物在日常生活生产中的用途相当广泛。Ⅰ. 根据所学知识,回答下列问题:
(1)
 具有净水作用,
具有净水作用, 净水的原理是
净水的原理是(2)向
 溶液中加入
溶液中加入 溶液至过量,微热。再通入
溶液至过量,微热。再通入 ,可观察到溶液呈紫色(高铁酸钾:
,可观察到溶液呈紫色(高铁酸钾: )。写出此过程发生反应的离子方程式:
)。写出此过程发生反应的离子方程式:(3)
 可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用
可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用 配制成溶液,并取
配制成溶液,并取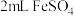 溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向
溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向 溶液和
溶液和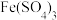 溶液中分别通入
溶液中分别通入 ,观察到
,观察到 溶液变为深棕色,
溶液变为深棕色,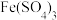 溶液无明显变化。
溶液无明显变化。①“试管中产生红棕色气体,溶液变为深棕色”的原因是
②实验小组改进实验,观察到溶液变为黄色的实验操作是
Ⅱ.在
 溶液中存在下列平衡:
溶液中存在下列平衡: 。
。(4)下列有关
 溶液的说法正确的是_______(填标号)。
溶液的说法正确的是_______(填标号)。| A.加入少量硫酸,溶液的橙色加深 |
| B.加入少量水稀释,溶液中离子总数增加 |
C.入少量 溶液,平衡逆向移动 溶液,平衡逆向移动 |
D.加入少量 固体,平衡正向移动, 固体,平衡正向移动, 转化率变大 转化率变大 |
Ⅲ.
 可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。
(5)
 时,剩余固体中
时,剩余固体中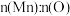 为
为(6)图中C点对应固体的成分为
您最近一年使用:0次
解题方法
7 .  的配位化合物较稳定且用途广泛。
的配位化合物较稳定且用途广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验:

已知:向 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子;
的配离子; 不能与
不能与 形成配位离子。下列说法正确的是
形成配位离子。下列说法正确的是
 的配位化合物较稳定且用途广泛。
的配位化合物较稳定且用途广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验:
已知:向
 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子;
的配离子; 不能与
不能与 形成配位离子。下列说法正确的是
形成配位离子。下列说法正确的是A. 和 和 最外层电子数相同 最外层电子数相同 |
| B.向溶液Ⅰ中滴加少量NaOH溶液,溶液逐渐变为浅紫色 |
C.配离子 中 中 的键角与 的键角与 分子中 分子中 的键角相等 的键角相等 |
D.可用NaF和KSCN溶液检验 溶液中是否含有 溶液中是否含有 |
您最近一年使用:0次
8 . 氢氧化铝 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠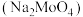 具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂(主要成分
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂(主要成分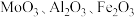 等)中回收
等)中回收 和
和 ,其工艺流程如图:
,其工艺流程如图:

已知 与
与 相似,均能在高温下跟
相似,均能在高温下跟 发生类似的反应,滤液中
发生类似的反应,滤液中 元素的存在形式为
元素的存在形式为 。
。
请回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ ,写出①焙烧时 跟
跟 反应的化学方程式
反应的化学方程式___________ 。
(2)检验第②步操作后所得的滤渣中含有 所用的试剂是
所用的试剂是___________ 。
(3)第③步操作中加入 不能过量,原因是
不能过量,原因是___________ ,可以通过测定溶液的___________ 来控制硫酸的用量,该步操作中生成 的离子方程式为
的离子方程式为___________ 。
(4)从题目信息可知,下图曲线___________ (填字母)为 的溶解度曲线。
的溶解度曲线。
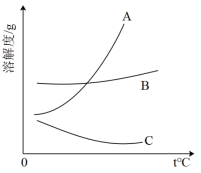
第④步操作中的过滤操作用到的玻璃仪器有___________ 。
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得 ,写出
,写出 发生铝热反应的化学方程式
发生铝热反应的化学方程式___________ 。
 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠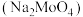 具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂(主要成分
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂(主要成分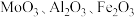 等)中回收
等)中回收 和
和 ,其工艺流程如图:
,其工艺流程如图:
已知
 与
与 相似,均能在高温下跟
相似,均能在高温下跟 发生类似的反应,滤液中
发生类似的反应,滤液中 元素的存在形式为
元素的存在形式为 。
。请回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为 跟
跟 反应的化学方程式
反应的化学方程式(2)检验第②步操作后所得的滤渣中含有
 所用的试剂是
所用的试剂是(3)第③步操作中加入
 不能过量,原因是
不能过量,原因是 的离子方程式为
的离子方程式为(4)从题目信息可知,下图曲线
 的溶解度曲线。
的溶解度曲线。
第④步操作中的过滤操作用到的玻璃仪器有
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得
 ,写出
,写出 发生铝热反应的化学方程式
发生铝热反应的化学方程式
您最近一年使用:0次
名校
9 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由实验现象可推知:___________ 。
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
(2)将补全下列实验操作步骤正确排序da___________ e(填标号);重复上述操作步骤,直至A恒重,记为m3g。
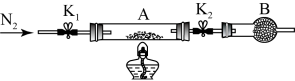
a、点燃酒精灯,加热 b、熄灭酒精灯 c、关闭K1和K2 d、打开K1和K2,缓缓通入N2 e、称量A f、冷却至室温
(3)缓缓通入N2的目的是___________ 。
为探究硫酸亚铁的分解产物,将(2)已恒重的装置A(取出ag后)接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
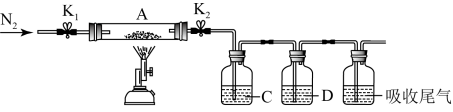
(4)①C、D中的溶液依次为BaCl2、品红。C、D中可观察到的现象分别为___________ 、___________ 。
②写出硫酸亚铁高温分解反应的化学方程式___________ 。
(5)为了测定A中样品的纯度,将取出ag样品溶于水,配制成500mL溶液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
在滴定的过程中,当___________ 即为滴定终点。
(6)上表中第一次实验中记录数据明显大于后两次,其原因可能是___________(填字母)。
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由实验现象可推知:
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
(2)将补全下列实验操作步骤正确排序da

a、点燃酒精灯,加热 b、熄灭酒精灯 c、关闭K1和K2 d、打开K1和K2,缓缓通入N2 e、称量A f、冷却至室温
(3)缓缓通入N2的目的是
为探究硫酸亚铁的分解产物,将(2)已恒重的装置A(取出ag后)接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

(4)①C、D中的溶液依次为BaCl2、品红。C、D中可观察到的现象分别为
②写出硫酸亚铁高温分解反应的化学方程式
(5)为了测定A中样品的纯度,将取出ag样品溶于水,配制成500mL溶液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
(6)上表中第一次实验中记录数据明显大于后两次,其原因可能是___________(填字母)。
| A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积 |
| B.滴定前滴定管尖嘴有气泡,滴定结束无气泡 |
| C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗 |
| D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低 |
您最近一年使用:0次
2022-12-10更新
|
99次组卷
|
2卷引用:上海市奉贤区致远高级中学2021-2022学年高二上学期期末教学评估(等级考)化学试题
10 . 硫氰化钾 是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备
是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备 并进行相关探究实验。
并进行相关探究实验。

已知:① 是一种不溶于水且密度大于水的非极性试剂;
是一种不溶于水且密度大于水的非极性试剂;
② 。
。
请回答下列问题:
(1) 的电子式为
的电子式为___________ 。
(2)装置A用于实验室制备氨气,该反应的化学方程式为___________ 。
(3)装置B中,三口烧瓶内盛有 、水和固体催化剂,通入氨气的导管需要插入
、水和固体催化剂,通入氨气的导管需要插入 液体中,其目的是
液体中,其目的是___________ 。
(4)待三口烧瓶内液体不再分层时,熄灭装置A处的酒精灯,关闭 ,移开水浴。将装置B继续加热至
,移开水浴。将装置B继续加热至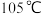 ,待
,待 完全分解后,打开
完全分解后,打开 ,缓缓滴入适量
,缓缓滴入适量 溶液,充分反应后制得
溶液,充分反应后制得 溶液。装置C中仪器a的名称为
溶液。装置C中仪器a的名称为___________ ,装置C处的烧杯中产生淡黄色浑浊的原因是___________ (用离子方程式表示)。
(5)过滤装置C中吸收尾气后的悬浊液,得到滤液x。现取少量滤液x进行如图所示的探究实验。
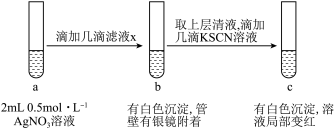
已知: 。
。
①试管b中产生银镜的原因是___________ (用离子方程式表示)。
②观察到试管c中出现上述实验现象后,用力振荡试管c,又观察到红色褪去且白色沉淀增多,结合平衡移动的知识解释其原因___________ 。
 是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备
是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备 并进行相关探究实验。
并进行相关探究实验。
已知:①
 是一种不溶于水且密度大于水的非极性试剂;
是一种不溶于水且密度大于水的非极性试剂;②
 。
。请回答下列问题:
(1)
 的电子式为
的电子式为(2)装置A用于实验室制备氨气,该反应的化学方程式为
(3)装置B中,三口烧瓶内盛有
 、水和固体催化剂,通入氨气的导管需要插入
、水和固体催化剂,通入氨气的导管需要插入 液体中,其目的是
液体中,其目的是(4)待三口烧瓶内液体不再分层时,熄灭装置A处的酒精灯,关闭
 ,移开水浴。将装置B继续加热至
,移开水浴。将装置B继续加热至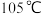 ,待
,待 完全分解后,打开
完全分解后,打开 ,缓缓滴入适量
,缓缓滴入适量 溶液,充分反应后制得
溶液,充分反应后制得 溶液。装置C中仪器a的名称为
溶液。装置C中仪器a的名称为(5)过滤装置C中吸收尾气后的悬浊液,得到滤液x。现取少量滤液x进行如图所示的探究实验。

已知:
 。
。①试管b中产生银镜的原因是
②观察到试管c中出现上述实验现象后,用力振荡试管c,又观察到红色褪去且白色沉淀增多,结合平衡移动的知识解释其原因
您最近一年使用:0次



