名校
解题方法
1 . I.将200mLH2SO4 和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干 燥、称量,得到46.6g 白色沉淀。则:
(1)原溶液中c( )=
)=_______ ;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为_______ 。
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是______________________ ,检验是否变质的方法是_______
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为_______
(1)原溶液中c(
 )=
)=(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为
您最近一年使用:0次
名校
解题方法
2 . 将19.2 g Cu和Fe2O3的混合物完全溶解在500 mL稀硫酸中,然后向溶液中加铁粉,剩余固体质量与加入铁粉质量的关系如图所示。
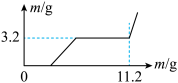
(1)混合物中Cu与Fe2O3的质量比为________ 。(不要计算过程)
(2)稀硫酸的物质的量浓度为________ 。(不要计算过程)

(1)混合物中Cu与Fe2O3的质量比为
(2)稀硫酸的物质的量浓度为
您最近一年使用:0次
20-21高一上·浙江绍兴·阶段练习
解题方法
3 . (1)分别取等物质的量浓度的氢氧化钠溶液100 mL,再通入一定量的CO2,随后分别各取10 mL溶液,向其中逐滴滴入0.2 mol/L的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图(分A、B两种情况):
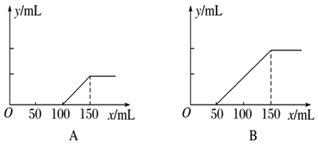
原氢氧化钠溶液的物质的量浓度为___________ mol/L。
(2)向一定量的Fe、FeO、Fe2O3 的混合物中加入100 mL浓度为2.0 mol/L的盐酸,恰好使混合物完全溶解,放出224 mL的气体(标准状况),所得溶液中加入KSCN溶液后无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是___________ 。

原氢氧化钠溶液的物质的量浓度为
(2)向一定量的Fe、FeO、Fe2O3 的混合物中加入100 mL浓度为2.0 mol/L的盐酸,恰好使混合物完全溶解,放出224 mL的气体(标准状况),所得溶液中加入KSCN溶液后无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
您最近一年使用:0次
名校
解题方法
4 . 向100 mL FeCl3和CuCl2的混合溶液中加入铁粉,其固体质量的变化如图所示,假设溶液体积不变,求:

(1)原混合溶液中FeCl3的物质的量___________
(2)c点溶液中FeCl2的物质的量浓度___________

(1)原混合溶液中FeCl3的物质的量
(2)c点溶液中FeCl2的物质的量浓度
您最近一年使用:0次
20-21高一上·浙江绍兴·阶段练习
5 . 铁粉和氧化铁粉末的混合物共32.8g,加入到200mL的盐酸中,固体完全溶解,得到标准状况下4.48L氢气。经测定,反应后的溶液中c(H+)为0.5mol/L,反应后的溶液中加入KSCN不变红(忽略反应前后溶液体积变化)。请计算:
(1)反应中放出氢气的质量为__ 。
(2)原混合物中铁和氧化铁的物质的量之比为__ 。
(3)原盐酸的物质的量浓度为_ mol/L。
(1)反应中放出氢气的质量为
(2)原混合物中铁和氧化铁的物质的量之比为
(3)原盐酸的物质的量浓度为
您最近一年使用:0次
20-21高一上·浙江绍兴·阶段练习
解题方法
6 . 铁、铜混合粉末18.0 g加入到100 mL5.0 mol/LFeCl3溶液中,充分反应后,剩余固体质量为2.8g。请计算:
(1)原固体混合物中铜的质量是___________ g。
(2)反应后溶液中n(Fe3+)=___________ mol;n(Cu2+)=___________ mol。
(1)原固体混合物中铜的质量是
(2)反应后溶液中n(Fe3+)=
您最近一年使用:0次
名校
7 . 称取一定量Fe2O3与Cu2O的混合粉末,用足量CO还原后,质量减轻8g。若原混合粉末用1L1mol∙L-1的稀H2SO4充分反应后,剩余固体质量为6.4g。已知:Cu2O+2H+=Cu+Cu2++H2O
(1)反应后硫酸的物质的量浓度为___ (设溶液体积不变)。
(2)原红色固体粉末中Fe2O3的物质的量为___ 。
(1)反应后硫酸的物质的量浓度为
(2)原红色固体粉末中Fe2O3的物质的量为
您最近一年使用:0次
2020-12-27更新
|
442次组卷
|
3卷引用:浙江省台州市2019—2020学年高一上学期期末质量评估考试化学试题
解题方法
8 . 向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL l.0mol·L−1的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中加入KSCN溶液无血红色出现。
请回答下列问题:
(1)生成的气体为__________ (填化学式),物质的量为__________ mol。
(2)所得溶液中溶质为__________ (填化学式),物质的量浓度为__________ mol·L−1。
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为__________ g。
(4)该混合物中铁原子与氧原子的个数比N(Fe)∶N(O)=__________ 。
请回答下列问题:
(1)生成的气体为
(2)所得溶液中溶质为
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(4)该混合物中铁原子与氧原子的个数比N(Fe)∶N(O)=
您最近一年使用:0次
名校
解题方法
9 . 铁、铜混合粉末20.0 g加入到100 mL5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2 g(忽略反应前后溶液体积变化)。计算:还原剂失去电子的物质的量_____ ;反应后溶液中FeCl2的物质的量浓度_____ mol·L-1。
您最近一年使用:0次
解题方法
10 . 铁、铜混合粉末18.0g加入到100 mL 5.0 mol·L-1FeCl3溶液中,充分反应后,剩余固体质量为2.8g。
求:(1)原固体混合物中铜的质量是__________ g ;
(2)反应后溶液中n(Fe2+)+ n(Cu2+)=________ mol。
求:(1)原固体混合物中铜的质量是
(2)反应后溶液中n(Fe2+)+ n(Cu2+)=
您最近一年使用:0次



