名校
解题方法
1 . Fe和 的混合物38.4g,加入
的混合物38.4g,加入 的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。
的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。
(1)发生反应的离子方程式有:___________ 。
(2)所得溶液中 的物质的量浓度为
的物质的量浓度为___________  (假设反应后溶液体积仍为200mL)。
(假设反应后溶液体积仍为200mL)。
(3) 的质量为多少克?
的质量为多少克?___________ (列出计算过程,此问无过程就无分)
(4)收集到气体在标准状况下的体积为___________ L。
 的混合物38.4g,加入
的混合物38.4g,加入 的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。
的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。(1)发生反应的离子方程式有:
(2)所得溶液中
 的物质的量浓度为
的物质的量浓度为 (假设反应后溶液体积仍为200mL)。
(假设反应后溶液体积仍为200mL)。(3)
 的质量为多少克?
的质量为多少克?(4)收集到气体在标准状况下的体积为
您最近半年使用:0次
2 . 通过下列步骤可以测定金属锡样品的纯度:
步骤1:将样品溶于盐酸中,将Sn全部转化为SnCl2;
步骤2:加入过量的FeCl3溶液,将SnCl2全部转化为SnCl4;
步骤3:用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,发生的反应为6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
现有金属锡样品0.613 g,经上述各步反应后,共用去0.100 mol•L-1K2Cr2O7溶液16.00 mL。
(1)步骤2中发生反应的化学方程式为_____ 。
(2)求样品中锡的质量分数_____ (假定杂质不参加反应)。
步骤1:将样品溶于盐酸中,将Sn全部转化为SnCl2;
步骤2:加入过量的FeCl3溶液,将SnCl2全部转化为SnCl4;
步骤3:用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,发生的反应为6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
现有金属锡样品0.613 g,经上述各步反应后,共用去0.100 mol•L-1K2Cr2O7溶液16.00 mL。
(1)步骤2中发生反应的化学方程式为
(2)求样品中锡的质量分数
您最近半年使用:0次
3 . 向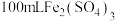 和
和 的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。忽略溶液体积的变化。
的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。忽略溶液体积的变化。
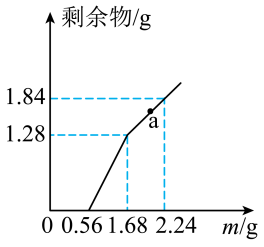
(1)原溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为_________ 。
(2)a点时溶液中溶质的物质的量浓度为_________ 。
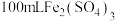 和
和 的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。忽略溶液体积的变化。
的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。忽略溶液体积的变化。
(1)原溶液中
 和
和 的物质的量浓度之比为
的物质的量浓度之比为(2)a点时溶液中溶质的物质的量浓度为
您最近半年使用:0次
解题方法
4 . 为确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入15.0mL某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。
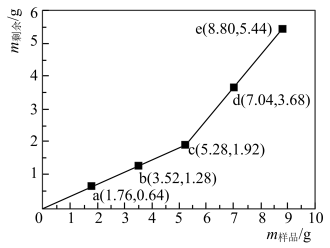
(1)该混合物中n(Fe2O3)︰n(Cu)=_______ 。
(2)稀硫酸的浓度为_______ mol/L。

(1)该混合物中n(Fe2O3)︰n(Cu)=
(2)稀硫酸的浓度为
您最近半年使用:0次
名校
解题方法
5 . 某磁黄铁矿的主要成分是FexS(S为=-2价),磁黄铁矿中既含有二价铁又含有三价铁。将一定量的该磁黄铁矿与盐酸完全反应(注:矿石中其他成分不与盐酸反应),生成1.6g硫单质、0.45molFeCl2和一定量H2S气体,且溶液中滴加KSCN溶液不变血红色。请计算并回答下列问题:
(1)该磁黄铁矿FexS中,Fe2+(二价铁)与Fe3+(三价铁)的物质的量之比为_______ 。
(2)该磁黄铁矿FexS中,x=_______ 。
(1)该磁黄铁矿FexS中,Fe2+(二价铁)与Fe3+(三价铁)的物质的量之比为
(2)该磁黄铁矿FexS中,x=
您最近半年使用:0次
名校
6 . 已知 2FeCl3+Fe=3FeCl2。在 FeCl3 溶液中加入一定量的 Fe,当反应进行到氯化铁和氯化亚铁的质量分数相等时,求此刻已参加反应的氯化铁和剩余的氯化铁的质量比_______ 。(相对分子质量 FeCl3:162.5 FeCl2:127 )
您最近半年使用:0次
名校
解题方法
7 . 计算(要有计算过程)
(1)常温常压下,用等质量的 、
、 、
、 三种气体分别吹出三个气球,求三个气球的体积之比为
三种气体分别吹出三个气球,求三个气球的体积之比为______ 。
(2)把 溶液和
溶液和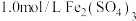 溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中
溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中 的物质的量浓度
的物质的量浓度___________ 。
(3)某种胃药的有效成分为碳酸钠,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①向一粒研碎后的药片(0.10g)中加入20.00ml蒸馏水;
②配置 稀盐酸和
稀盐酸和 溶液;
溶液;
③加入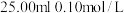 稀盐酸;
稀盐酸;
④用 溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
某同学4次测定所消耗的NaOH溶液的体积如下:
根据这个同学的实验数据,计算这种药片中碳酸钙的质量分数_________ 。
(1)常温常压下,用等质量的
 、
、 、
、 三种气体分别吹出三个气球,求三个气球的体积之比为
三种气体分别吹出三个气球,求三个气球的体积之比为(2)把
 溶液和
溶液和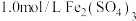 溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中
溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中 的物质的量浓度
的物质的量浓度(3)某种胃药的有效成分为碳酸钠,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①向一粒研碎后的药片(0.10g)中加入20.00ml蒸馏水;
②配置
 稀盐酸和
稀盐酸和 溶液;
溶液;③加入
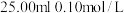 稀盐酸;
稀盐酸;④用
 溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;某同学4次测定所消耗的NaOH溶液的体积如下:
| 测定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
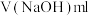 | 13.00 | 12.90 | 13.10 | 13.50 |
您最近半年使用:0次
解题方法
8 . 向铁和氧化铁的混合物中加入600mL 稀盐酸后恰好完全反应,所得溶液滴加硫氰化钾不显红色,并收集到672mL氢气(标准状况下测定)。回答下列问题:
稀盐酸后恰好完全反应,所得溶液滴加硫氰化钾不显红色,并收集到672mL氢气(标准状况下测定)。回答下列问题:
(1)反应后溶液中的溶质为_______ mol。
(2)原混合物中单质铁的质量为_______ g。
 稀盐酸后恰好完全反应,所得溶液滴加硫氰化钾不显红色,并收集到672mL氢气(标准状况下测定)。回答下列问题:
稀盐酸后恰好完全反应,所得溶液滴加硫氰化钾不显红色,并收集到672mL氢气(标准状况下测定)。回答下列问题:(1)反应后溶液中的溶质为
(2)原混合物中单质铁的质量为
您最近半年使用:0次
解题方法
9 . 完成下列问题。
I.
(1) 个
个 分子含有原子
分子含有原子_______  。
。
(2)同温同压下相同体积的 气体和
气体和 气体的分子数之比为
气体的分子数之比为_______ 。
(3)4.0g某气体X中含有的分子数约为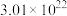 ,则气体X的摩尔质量为
,则气体X的摩尔质量为_______ 。
(4)4.6g钠与氧气充分反应,转移电子_______ 个。
II.已知二氧化锰与浓盐酸在加热条件下发生反应的化学方程式为: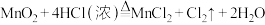 ,用8.7g二氧化锰与足量的浓盐酸混合加热充分反应;
,用8.7g二氧化锰与足量的浓盐酸混合加热充分反应;
(5)转移电子物质的量_______ ,产生的 在标准状况下的体积
在标准状况下的体积_______ 。
(6)将反应后的溶液加水稀释至 ,则此溶液中
,则此溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
III.电子工业常用30%的 溶液腐蚀敷在绝缘板上的铜箱,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜箱,制造印刷电路板。
(7)检验溶液中 存在的试剂是
存在的试剂是_______ 。
(8)写出 溶液与金属铜发生反应的离子方程式
溶液与金属铜发生反应的离子方程式_______ 。
I.
(1)
 个
个 分子含有原子
分子含有原子 。
。(2)同温同压下相同体积的
 气体和
气体和 气体的分子数之比为
气体的分子数之比为(3)4.0g某气体X中含有的分子数约为
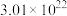 ,则气体X的摩尔质量为
,则气体X的摩尔质量为(4)4.6g钠与氧气充分反应,转移电子
II.已知二氧化锰与浓盐酸在加热条件下发生反应的化学方程式为:
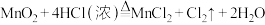 ,用8.7g二氧化锰与足量的浓盐酸混合加热充分反应;
,用8.7g二氧化锰与足量的浓盐酸混合加热充分反应;(5)转移电子物质的量
 在标准状况下的体积
在标准状况下的体积(6)将反应后的溶液加水稀释至
 ,则此溶液中
,则此溶液中 的物质的量浓度是
的物质的量浓度是III.电子工业常用30%的
 溶液腐蚀敷在绝缘板上的铜箱,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜箱,制造印刷电路板。(7)检验溶液中
 存在的试剂是
存在的试剂是(8)写出
 溶液与金属铜发生反应的离子方程式
溶液与金属铜发生反应的离子方程式
您最近半年使用:0次
21-22高一·全国·假期作业
10 . 有一瓶用硫酸酸化的FeSO4溶液,置于空气中一段时间后,溶液中c(H+)=0.1mol·L-1。为测定其中Fe2+被氧化的百分率,进行如下操作:
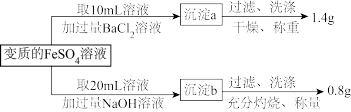
请计算(忽略Fe2+、Fe3+的水解):
(1)20mL变质的FeSO4溶液中,铁元素的总的物质的量为_______ ;
(2)原溶液中Fe2+被氧化的百分率_______ ;
(3)原溶液中硫酸的物质的量浓度为_______ 。

请计算(忽略Fe2+、Fe3+的水解):
(1)20mL变质的FeSO4溶液中,铁元素的总的物质的量为
(2)原溶液中Fe2+被氧化的百分率
(3)原溶液中硫酸的物质的量浓度为
您最近半年使用:0次



