名校
1 . 能证明溶液中含有Fe3+的试剂是( )
| A.氯水 | B.KSCN溶液 |
| C.稀H2SO4 | D.品红溶液 |
您最近一年使用:0次
2020-05-26更新
|
459次组卷
|
6卷引用:湖南省2020年普通高中学业水平合格性考试模拟卷一 化学
名校
解题方法
2 . FeCl2是中学化学常用试剂。请根据题意填空:
往FeCl2溶液中加入KSCN溶液,溶液___ (填“变”或“不变”)色,再往其中通入氯气,溶液呈___ (填“红”或“蓝”)色。除去FeCl2溶液中少量的FeCl3应加(通)入的试剂为___ (填“Fe”或“Cl2”)。
往FeCl2溶液中加入KSCN溶液,溶液
您最近一年使用:0次
2020-05-26更新
|
383次组卷
|
2卷引用:湖南省2020年普通高中学业水平合格性考试模拟卷一 化学
10-11高一下·广东深圳·期中
名校
3 . 将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有
| A.Cu、Fe2+、Fe | B.Fe2+、Fe3+ |
| C.Cu、Cu2+、Fe | D.Cu、Fe3+ |
您最近一年使用:0次
2020-05-22更新
|
178次组卷
|
22卷引用:湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题
湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题湖南省张家界市民族中学2019-2020学年高一上学期第三次月考化学试题(已下线)2010-2011学年广东省深圳市高级中学高一下学期期中考试化学试卷(已下线)2011-2012学年天津市蓟县一中高一第二次月考化学试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高三期中考试化学试卷(已下线)2012年鲁科版高中化学选修4 3.4离子反应练习卷(已下线)2012-2013年黑龙江哈尔滨第十二中学高一上学期期末考试化学试卷2015-2016学年山西省怀仁一中高一12月月考化学试卷2015-2016学年陕西省西北农林科大附中高一上第二次月考化学试卷2016届贵州省务川民族中学高三上学期期中考试化学试卷2015-2016学年黑龙江省双鸭山一中高二6月月考化学试卷2016-2017学年河北石家庄辛集中学高一上阶段考二化学卷2016-2017学年甘肃省嘉峪关市酒钢三中高一上学期期末考试化学试卷甘肃省嘉峪关市酒钢三中2017-2018学年高二上学期第二次月考化学试题甘肃省靖远县第四中学2018-2019学年高一上学期第二次月考化学试题河南省信阳市第六高级中学2018-2019学年高一上学期第三次(1月)月考化学试题山东省济宁市微山县第二中学2019-2020学年高一上学期第三学段质量检测化学试题云南省昆明市农业大学附属中学2019-2020学年高一上学期第二次月考化学试题河北省泊头市第一中学2019-2020学年高一上学期第四次月考化学试题河南省焦作市沁阳市第一中学2019-2020学年高一上学期12月月考化学试题甘肃省白银市会宁县第一中学2020-2021学年高一上学期第二次月考化学试题安徽省合肥市长丰县2020-2021学年高一上学期期末联考化学试题
10-11高一下·浙江杭州·期中
名校
4 . 把SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原的是
| A.SO2 | B.Fe2+ | C.Fe3+ | D.NO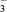 |
您最近一年使用:0次
2020-05-12更新
|
958次组卷
|
24卷引用:2015届湖南省邵阳县石齐学校高三上学期第三次月考化学试卷
(已下线)2015届湖南省邵阳县石齐学校高三上学期第三次月考化学试卷(已下线)2010—2011学年浙江省杭州二中高一下学期期中考试化学试卷(已下线)2011-2012学年浙江省台州中学高一下学期期中考试化学试卷2015-2016学年吉林省松原油田高中高一下期初考试化学卷黑龙江省哈尔滨市第三中学2018届高三上学期第一次验收考试化学试题贵州省麻江县一中2018-2019学年高一上学期期末考试化学试题上海市南洋模范中学2016-2017学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高一上学期期末考试化学试题广西来宾市象州县中学2019-2020学年高一上学期期末考试化学试题安徽省安庆市怀宁县第二中学2019届高三上学期第三次月考化学试题黑龙江省大庆实验中学2019-2020学年高二下学期期末考试化学试题内蒙古包头市重工业集团有限公司第三中学2019-2020学年高一下学期期中考试化学试题鲁科版(2019)高一必修第一册第三章易错疑难集训(三)(已下线)【浙江新东方】高中化学20210304-021吉林省“BEST合作体”2020-2021学年高一下学期期中化学试题吉林省汪清四中2020-2021学年高一下学期第二次阶段考试化学试题福建省泉州第五中学2020-2021学年高一下学期期中考试化学试题浙江省绍兴市柯桥区2021届高三下学期6月选考科目考试化学试题吉林省长春市第二实验中学 2021-2022 学年高一下学期期中考试化学试题福建省泉州市第七中学2021-2022学年高一下学期期中考试化学试题福建省福州第四中学2021-2022学年高一下学期期末考试化学试题安徽省怀宁县第二中学2021-2022学年高三上学期第二次月考化学试题福建省莆田第十五中学2022-2023学年高一下学期第一次月考(3月)化学试题安徽省合肥市第一中学2023-2024学年高一下学期月考化学试题(一)
名校
解题方法
5 . 某兴趣小组将过量Cu与FeCl3溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,观察到瞬间产生白色沉淀,局部出现红色;振荡试管,红色又迅速褪去。已知:
①CuCl2+Cu=2CuCl↓(白色)——该反应速率很慢
②2CuCl2+4KSCN=2CuSCN↓(白色)+(SCN)2+4KCl——该反应速率很快
③(SCN)2是拟卤素,化学性质和氯气相似
下列说法正确的是( )
①CuCl2+Cu=2CuCl↓(白色)——该反应速率很慢
②2CuCl2+4KSCN=2CuSCN↓(白色)+(SCN)2+4KCl——该反应速率很快
③(SCN)2是拟卤素,化学性质和氯气相似
下列说法正确的是( )
| A.用KSCN溶液检验Fe3+时,Cu2+的存在不会对检验产生干扰 |
| B.局部出现红色主要是因为溶液中的Fe2+被空气中的O2氧化成Fe3+,Fe3+与KSCN反应生成Fe(SCN)3 |
| C.白色沉淀是CuCl,是溶液中CuCl2与Cu反应生成的 |
| D.红色迅速褪去的原因是振荡试管时Cu2+与SCN-发生反应,从而使Fe3++3SCN-⇌Fe(SCN)3平衡逆移 |
您最近一年使用:0次
2020-05-10更新
|
935次组卷
|
16卷引用:浙江省衢州、湖州、丽水三地市高三4月教学质量检测化学试题
浙江省衢州、湖州、丽水三地市高三4月教学质量检测化学试题湖南省衡阳市第八中学2023-2024学年高三上学期10月月考化学试题湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)课时18 铜及其化合物 合金-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省扬州中学2021-2022学年高三上学期10月考化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点16 铜及其金属材料-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题03 铁 金属材料-2023年高考化学一轮复习小题多维练(全国通用)(已下线)考点16 铜及其金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷 陕西省渭南市2023-2024学年高三教学质量检测(Ⅰ)化学试题江西省宜春市丰城市第九中学日新班2023-2024学年高二上学期期末考试化学试题
6 . 检验硫酸亚铁溶液中是否含有少量硫酸铁,可选用最佳试剂是
| A.氯水 | B.KMnO4溶液 | C.KSCN溶液 | D.Fe 粉 |
您最近一年使用:0次
2020-05-09更新
|
132次组卷
|
3卷引用:上海市闵行区2020届高三第二次模拟考试化学试题
7 . 向盛有Fe2(SO4)3溶液的试管中滴入几滴KSCN溶液后,溶液呈:( )
| A.血红色 | B.黄色 | C.无色 | D.浅绿色 |
您最近一年使用:0次
2020-04-28更新
|
475次组卷
|
11卷引用:【省级联考】湖南省普通高中2017-2018学年高二下学期学业水平考试化学试题
【省级联考】湖南省普通高中2017-2018学年高二下学期学业水平考试化学试题2018年湖南省普通高中学业水平考试化学试题 湖南省衡阳市欧阳遇实验中学2018-2019学年高一下学期期末考试化学试题吉林省长春市第二十九中学2019-2020学年高一下学期第三次月考化学(文)试题广东省茂名市电白区水东中学2020-2021学年高一上学期12月月考化学试题湖南省邵阳市第十一中学2020-2021学年高一上学期期末考试化学试题湖南省长沙市周南中学2020-2021学年高一上学期期末考试化学试题云南省孟连傣族拉祜族佤族自治县第一中学2020-2021学年高一上学期期中考试化学(文)试题湖南省郴州市2022-2023学年高一下学期学业水平合格性考试模拟监测化学试题四川省2022-2023学年高二(2020级)上学期普通高中学业水平考试化学试题云南省蒙自市第一高级中学2022-2023学年高一下学期5月期中考试化学试题
名校
8 . 化学与生产、实验密切相关。下列有关物质的性质与用途具有对应关系的是( )
A. 熔点高,可用作耐高温材料 熔点高,可用作耐高温材料 |
B. 溶液呈酸性,可用于腐蚀电路板上的 溶液呈酸性,可用于腐蚀电路板上的 |
| C.石墨具有导电性,可用于制铅笔芯 |
D.浓硫酸具有强氧化性,可用于干燥 |
您最近一年使用:0次
2020-04-28更新
|
582次组卷
|
15卷引用:湖南省永州市祁阳县2018-2019学年高二上学期期末考试化学试题
湖南省永州市祁阳县2018-2019学年高二上学期期末考试化学试题江苏省泰州市2018届高三第一次调研化学试题甘肃省白银市第一中学2018届高三3月测试化学试题【校级联考】贵州省遵义市第四教育集团2019届高三上学期第二次联考理综化学试题江苏省启东市2020届高三上学期期中考试化学试题2019届上海奉贤区高考第一次模拟化学试题2020届上海市奉贤区高考化学一模试卷江苏省海安高级中学2020届高三模拟考试化学试题江苏省海安高级中学2020届高三调研考试化学试题天津市河西区2020芦台一中高三模拟测试江苏省扬州中学2021届高三上学期12月月考化学试题江苏省邗江中学2020-2021学年高二(2019级新疆班)下学期期中化学试题重庆市江津中学、铜梁中学、长寿中学等七校联盟2021届高三下学期第三次模拟考试化学试题江苏省泰兴市第一高级中学2021-2022学年高二下学期第一次阶段测试化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高三上学期第一次月考化学试题
解题方法
9 . 甲同学向做过银镜反应的试管滴加0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:
甲同学认为:Fe3+具有氧化性,能够溶解单质Ag。
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag。
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解。
(1)生成银镜反应过程中银氨溶液发生_____________ (氧化、还原)反应。
(2)为得出正确结论,只需设计两个实验验证即可。
实验I:向溶解了银镜的Fe(NO3)3的溶液中加入____________ (填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HCl),现象为___________ ,证明甲的结论正确。
实验Ⅱ:向附有银镜的试管中加入______________ 溶液,观察银镜是否溶解。
两个实验结果证明了丙同学的结论。
(3)丙同学又把5mLFeSO4溶液分成两份:第一份滴加2滴KSCN溶液无变化;第二份加入1mL0.1mol/LAgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红。根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系_______________ 。
(4)丁同学改用如图实验装置做进一步探究:

①K刚闭合时,指针向左偏转,此时石墨作_________ ,(填“正极”或“负极。此过程氧化性:Fe3+_______ Ag+(填>或<)。
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转。此过程氧化性:Fe3+_______ Ag+(填>或<)。
③由上述①②实验,得出的结论是:_______________________ 。
甲同学认为:Fe3+具有氧化性,能够溶解单质Ag。
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag。
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解。
(1)生成银镜反应过程中银氨溶液发生
(2)为得出正确结论,只需设计两个实验验证即可。
实验I:向溶解了银镜的Fe(NO3)3的溶液中加入
实验Ⅱ:向附有银镜的试管中加入
两个实验结果证明了丙同学的结论。
(3)丙同学又把5mLFeSO4溶液分成两份:第一份滴加2滴KSCN溶液无变化;第二份加入1mL0.1mol/LAgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红。根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系
(4)丁同学改用如图实验装置做进一步探究:

①K刚闭合时,指针向左偏转,此时石墨作
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转。此过程氧化性:Fe3+
③由上述①②实验,得出的结论是:
您最近一年使用:0次
名校
解题方法
10 . 消毒剂在生产生活中有极其重要的作用,开发具有广普、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
Ⅰ.含氯消毒剂在生产生活中有极其重要的作用。
(1)Cl2常用于自来水的杀菌消毒。Cl2溶于水后,溶液中具有氧化作用的含氯微粒除Cl2外还有______________ 。
(2)为了提高生活用水的卫生标准,自来水厂常同时使用Cl2和FeSO4·7H2O进行消毒、净化,以改善水质。其原因:一是_________________________________ (用离子方程式和相应的文字解释),二是生成的Fe(OH)3胶体具有较强的吸附 性能,可吸附水中的悬浮杂质,并能形成沉淀,使水净化。
(3)KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。常用作消毒剂,其变化可以表示为:2KClO3+4HCl(浓) = 2KCl+2ClO2↑+Cl2↑+2H2O,若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:_______________________ 。
Ⅱ.铁的化合物高铁酸钠(Na2FeO4)是一种新型净水剂。
(1)高铁酸钠主要通过反应制取:2Fe(OH)3+3X+ 4NaOH=2Na2FeO4+3NaCl+ 5H2O,则X的化学式为_____________ 。
(2)高铁酸钠在水中可以发生反应:4FeO42-+10H2O 4Fe(OH)3+8OH-↑+3O2。由此看来,高铁酸钠能够杀菌消毒是因为它具有
4Fe(OH)3+8OH-↑+3O2。由此看来,高铁酸钠能够杀菌消毒是因为它具有________ 性。
Ⅲ.(1)H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称。H2O2被称为“绿色氧化剂”的理由是________________________________ 。
(2)取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
①加适量H2O2,紫红色褪去,并有气泡产生;
②加入适量的PbO2固体,固体溶解,溶液又变为紫红色;
③后通入足量SO2,发生反应:5SO2+2MnO4-+5Pb2++2H2O==5PbSO4↓+2Mn2++4H+。
则KMnO4、H2O2、PbO2氧化性由强到弱的顺序为_______________________ 。
Ⅰ.含氯消毒剂在生产生活中有极其重要的作用。
(1)Cl2常用于自来水的杀菌消毒。Cl2溶于水后,溶液中具有氧化作用的含氯微粒除Cl2外还有
(2)为了提高生活用水的卫生标准,自来水厂常同时使用Cl2和FeSO4·7H2O进行消毒、净化,以改善水质。其原因:一是
(3)KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。常用作消毒剂,其变化可以表示为:2KClO3+4HCl(浓) = 2KCl+2ClO2↑+Cl2↑+2H2O,若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:
Ⅱ.铁的化合物高铁酸钠(Na2FeO4)是一种新型净水剂。
(1)高铁酸钠主要通过反应制取:2Fe(OH)3+3X+ 4NaOH=2Na2FeO4+3NaCl+ 5H2O,则X的化学式为
(2)高铁酸钠在水中可以发生反应:4FeO42-+10H2O
 4Fe(OH)3+8OH-↑+3O2。由此看来,高铁酸钠能够杀菌消毒是因为它具有
4Fe(OH)3+8OH-↑+3O2。由此看来,高铁酸钠能够杀菌消毒是因为它具有Ⅲ.(1)H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称。H2O2被称为“绿色氧化剂”的理由是
(2)取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
①加适量H2O2,紫红色褪去,并有气泡产生;
②加入适量的PbO2固体,固体溶解,溶液又变为紫红色;
③后通入足量SO2,发生反应:5SO2+2MnO4-+5Pb2++2H2O==5PbSO4↓+2Mn2++4H+。
则KMnO4、H2O2、PbO2氧化性由强到弱的顺序为
您最近一年使用:0次



