1 . 下列有关物质的鉴别或检验的实验方案能达到目的的是
| A.用聚光束仪鉴别硫酸铜溶液和淀粉溶液 |
| B.用氯化钡溶液检验溶液中是否含有硫酸根 |
| C.用KSCN溶液检验电路板刻蚀液中的Fe2+ |
| D.用酸性高锰酸钾溶液鉴别乙醇与丙烯酸溶液 |
您最近一年使用:0次
名校
解题方法
2 . 一种利用磁铁矿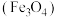 制备铁红的流程如下:
制备铁红的流程如下:
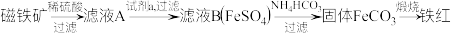
下列说法正确的是
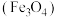 制备铁红的流程如下:
制备铁红的流程如下: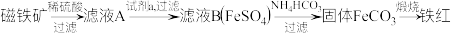
下列说法正确的是
| A.往滤液A中滴加少量酸性KMnO4溶液,可观察到紫红色褪去 |
B.可以用KSCN溶液和氯水检验滤液A中是否有 |
C.FeCO3在空气中煅烧的反应方程式为 |
| D.最终得到铁红中的Fe元素的质量小于原磁铁矿中的Fe元素的质量 |
您最近一年使用:0次
3 . 根据下列实验操作及现象,得出的结论正确的是
选项 | 操作及现象 | 结论 |
A | 向 溶液中滴加苯酚溶液,溶液变紫色 溶液中滴加苯酚溶液,溶液变紫色 |  已变质 已变质 |
B | 向 中滴加稀硫酸,没有明显现象 中滴加稀硫酸,没有明显现象 | 酸性: |
C | 在酸性 溶液中滴加 溶液中滴加 溶液,溶液褪色 溶液,溶液褪色 |  还原 还原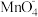 |
D | 在 的四氯化碳溶液中加入KI溶液,下层液体颜色变浅 的四氯化碳溶液中加入KI溶液,下层液体颜色变浅 | KI具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列离子方程式正确且符合题意的是
A.向 浊液中滴加 浊液中滴加 溶液产生蓝色沉淀: 溶液产生蓝色沉淀: |
B.向 溶液中滴加 溶液中滴加 溶液产生气泡: 溶液产生气泡: |
C.向变质的 溶液中滴加 溶液中滴加 溶液,溶液变红色: 溶液,溶液变红色: |
D.向 白色浊液中滴加氨水,溶液变澄清: 白色浊液中滴加氨水,溶液变澄清: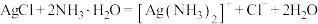 |
您最近一年使用:0次
5 . 下列实验操作和现象及结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了加成反应 |
| B | 向5 mL 0.01 mol/L KI溶液中加入2 mL 0.01 mol/L  溶液,将溶液分成两份,一份滴加淀粉溶液呈蓝色,另一份滴加KSCN溶液呈红色 溶液,将溶液分成两份,一份滴加淀粉溶液呈蓝色,另一份滴加KSCN溶液呈红色 |  和 和 的反应存在限度 的反应存在限度 |
| C | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| D | 向丙烯醛中滴加溴水,溴水褪色 | 丙烯醛分子中含有碳碳双键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-02更新
|
76次组卷
|
2卷引用:2024届新高考教学教研联盟高三下学期第一次联考化学试卷
名校
6 . 下列反应的离子反应方程式正确的是
| A.碘化钾淀粉溶液中加入FeCl3变蓝:2I-+Fe3+= Fe2++I2 |
B.过量的碳酸氢钠溶液与澄清石灰水混合: 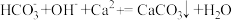 |
| C.向盛有氯化银的试管中滴加氨水:AgCl + 2NH3 = [Ag(NH3)2]+ + Cl- |
D.向氢氧化钠稀溶液中加入适量的铝片: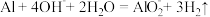 |
您最近一年使用:0次
名校
解题方法
7 . 下列实验操作对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有红棕色气体集气瓶中滴加淀粉-KI溶液 | 溶液呈蓝色 | 该气体为二氧化氮 |
| B | 滴入几滴酸性高锰酸钾溶液于盛有氯化亚铁的溶液中 | 紫红色褪去 | 氧化性: |
| C | 向淀粉溶液中加入适量的稀硫酸,加热,冷却后加入NaOH溶液至碱性,加入少量碘水 | 溶液为变蓝 | 淀粉已完全水解 |
| D | 向盛有5ml0.1mol/LKI溶液的试管中滴入同浓度的FeCl3溶液5~6滴,然后加入2mLCCl4充分振荡,CCl4层呈紫色;静置后在上层清液中滴入KSCN溶液 | 上层清液变为血红色 | FeCl3与KI溶液反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 化学是一门实用性很强的科学。请根据题意填空:
(1)侯德榜是我国近代化学工业的奠基人之一,创立了侯氏制碱法。该工艺制得的纯碱的化学式为___________ (填“Na2CO3”或“NaHCO3”);
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用___________ (填“KSCN”或“H2SO4”)溶液;
(3)“雷雨发庄稼”的原理是空气中的氮气经多步反应生成硝酸盐,被植物吸收,促进生长。其中间产物NO2的颜色是___________ (填“红棕色”或“无色”)。
(1)侯德榜是我国近代化学工业的奠基人之一,创立了侯氏制碱法。该工艺制得的纯碱的化学式为
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用
(3)“雷雨发庄稼”的原理是空气中的氮气经多步反应生成硝酸盐,被植物吸收,促进生长。其中间产物NO2的颜色是
您最近一年使用:0次
9 . 下列各组中的离子,能在溶液中大量共存的是
| A.Fe3+、SCN- | B.Ba2+、CO | C.H+、OH- | D.Na+、NO |
您最近一年使用:0次
名校
解题方法
10 . 研究人员拟设计黄铜矿(主要含 )制备硝酸铜和绿矾晶体的流程如下:
)制备硝酸铜和绿矾晶体的流程如下:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价,已知“焙烧”生成 、CuO和
、CuO和 则其化学反应方程式为
则其化学反应方程式为_______ 。
(2)“置换”步骤中发生的所有反应的离子方程式有
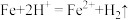 、
、_______ 。
(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、_______ 。
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是_______ (填“稀 ”或“稀
”或“稀 ”)。
”)。
(5)“反应”步骤中,10% 为氧化剂,20%
为氧化剂,20% 提供
提供 ,可以避免污染性气体的产生,写出该“反应”的离子方程式:
,可以避免污染性气体的产生,写出该“反应”的离子方程式:_______ 。
(6)绿矾晶体( )在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
)在空气中极易变质;验证绿矾晶体已变质可选择的试剂为_______ 。
 )制备硝酸铜和绿矾晶体的流程如下:
)制备硝酸铜和绿矾晶体的流程如下: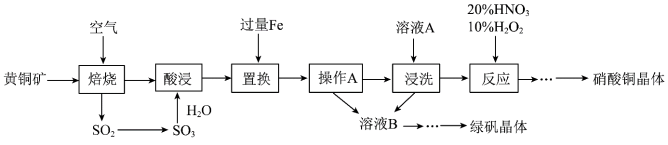
(1)
 中铁元素的化合价为
中铁元素的化合价为 、CuO和
、CuO和 则其化学反应方程式为
则其化学反应方程式为(2)“置换”步骤中发生的所有反应的离子方程式有

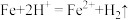 、
、(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是
 ”或“稀
”或“稀 ”)。
”)。(5)“反应”步骤中,10%
 为氧化剂,20%
为氧化剂,20% 提供
提供 ,可以避免污染性气体的产生,写出该“反应”的离子方程式:
,可以避免污染性气体的产生,写出该“反应”的离子方程式:(6)绿矾晶体(
 )在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
)在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
您最近一年使用:0次



