1 . 关于中学化学中常见的物质A、B、C、D,它们之间转化关系如图所示(部分产物和条件已略去),回答下列问题:

(1)若C固体的颜色为黄色,A为金属单质,D为___________ 。
(2)若A为黄绿色气体,D为常见金属,C为___________ 。

(1)若C固体的颜色为黄色,A为金属单质,D为
(2)若A为黄绿色气体,D为常见金属,C为
您最近一年使用:0次
名校
2 . 硫铁矿烧渣的主要成分为Fe2O3 、Fe3O4 ,以及少量SiO2 、Al2O3 等。由硫铁矿烧渣制备铁红(Fe2O3)的一种工艺流程如下:

已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
(1)“酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号)______________ 。
(2)Fe粉除调pH外,另一个作用是___________________ ;Fe粉调节溶液的pH范围为________________________ 。
(3)已知“沉淀、过滤”中生成沉淀为碳酸铁沉淀,则高温条件下,“氧化”步骤中发生反应的化学方程式为___________________________ 。
(4)Fe2O3 也是赤铁矿的主要成分,工业上若想要得到120t纯度为93%生铁需要含杂质20%的(杂志不含铁元素)赤铁矿的质量为多少______________________ 。

已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
(2)Fe粉除调pH外,另一个作用是
(3)已知“沉淀、过滤”中生成沉淀为碳酸铁沉淀,则高温条件下,“氧化”步骤中发生反应的化学方程式为
(4)Fe2O3 也是赤铁矿的主要成分,工业上若想要得到120t纯度为93%生铁需要含杂质20%的(杂志不含铁元素)赤铁矿的质量为多少
您最近一年使用:0次
2017-10-23更新
|
449次组卷
|
6卷引用:湖南省衡阳市第八中学2017-2018学年高一(理科实验班)上学期第一次月考理综化学试题
名校
3 . 纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域。下图是制备纳米Fe3O4磁流体的两种流程:
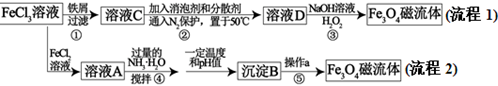
(1)分析流程图中的两种流程,其中_________ (填“流程1”、“流程2”)所有反应不涉及氧化还原反应。步骤①反应的离子方程式为____________ 。
(2)步骤②保持50℃的做法是_________ 。
(3)步骤③中加入的H2O2电子式是_______ ,步骤③制备Fe3O4磁流体的化学方程式为________ 。
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为_________ 。已知沉淀B为四氧化三铁,步骤⑤中操作a具体的步骤是_____________ 。
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01 mol·L-1的K2Cr2O7标准溶液100 mL,则磁流体中含有Fe2+的物质的量为_____ mol。若配制的K2Cr2O7标准溶液装在__________ (填“酸式滴定管”或“碱式滴定管”)时,滴定前平视刻度线,滴定后仰视刻度线,则测定结果是Fe3O4磁流体中的Fe2+含量_____ (填“偏大”、“偏小”或“不变”)。

(1)分析流程图中的两种流程,其中
(2)步骤②保持50℃的做法是
(3)步骤③中加入的H2O2电子式是
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01 mol·L-1的K2Cr2O7标准溶液100 mL,则磁流体中含有Fe2+的物质的量为
您最近一年使用:0次
2017-09-10更新
|
337次组卷
|
2卷引用:湖南省衡阳市第八中学2018届高三(实验班)上学期第一次月考理综化学试题
11-12高二上·湖南张家界·期末
4 . 钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:_______________ 。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3·xH2O),反应的化学方程式为_________________ 。
(3)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被完全除尽后,溶液中继续发生的化合反应的化学方程式为____________________________ 。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3·xH2O),反应的化学方程式为
(3)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被完全除尽后,溶液中继续发生的化合反应的化学方程式为
您最近一年使用:0次



