1 . Ⅰ.已知A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,J是一种黑色固体,I的浓溶液具有还原性,A~I均为中学化学常见物质,它们之间的转化关系如图所示。(部分生成物和反应条件已略去)

请回答下列问题:
(1)写出组成物质D的元素在周期表中的位置:_______ 。
(2)写出反应②的化学方程式:_______ 。
(3)J在H2O2分解反应中作催化剂。若将适量J加入酸化的H2O2溶液中,J溶解生成它的+2价离子,该反应的离子方程式是_______ 。
Ⅱ.某无色溶液,其中可能存在以下离子:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-,现取该溶液进行有关试验,其结果如下:
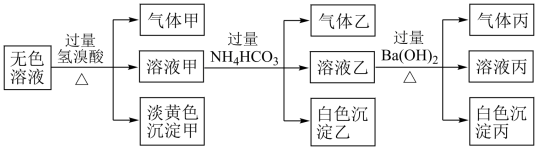
回答下列问题:
(4)生成沉淀甲的离子方程式:_______ ;
(5)已知气体甲由两种氧化物组成(不包括水蒸气和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表中(可不填满,表中每一行对应正确方可得分)_______
(6)针对溶液中可能存在的离子,用实验验证其是否存在的方法是_______ 。

请回答下列问题:
(1)写出组成物质D的元素在周期表中的位置:
(2)写出反应②的化学方程式:
(3)J在H2O2分解反应中作催化剂。若将适量J加入酸化的H2O2溶液中,J溶解生成它的+2价离子,该反应的离子方程式是
Ⅱ.某无色溶液,其中可能存在以下离子:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-,现取该溶液进行有关试验,其结果如下:

回答下列问题:
(4)生成沉淀甲的离子方程式:
(5)已知气体甲由两种氧化物组成(不包括水蒸气和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表中(可不填满,表中每一行对应正确方可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | |||
| 4 |
您最近一年使用:0次
2017-02-17更新
|
773次组卷
|
2卷引用:2017届河南省南阳一中高三上第三次周考化学卷
名校
解题方法
2 . 下列实验操作和现象、结论或目的均正确的是
| 选项 | 操作和现象 | 结论或目的 |
| A | 将 浓溶液滴加到饱和的 浓溶液滴加到饱和的 溶液中 溶液中 | 制备 胶体 胶体 |
| B |  还原 还原 得到的黑色固体加入盐酸溶解后再加入 得到的黑色固体加入盐酸溶解后再加入 溶液,溶液不显红色 溶液,溶液不显红色 | 黑色固体中可能有 |
| C | 取少量 试样加水溶解,滴加高锰酸钾,紫红色褪去 试样加水溶解,滴加高锰酸钾,紫红色褪去 | 该 试样已经变质 试样已经变质 |
| D | 向某溶液中加入 溶液不变红色,再通入 溶液不变红色,再通入 ,再加入 ,再加入 溶液变红色 溶液变红色 | 原溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-12-31更新
|
125次组卷
|
2卷引用:河北省石家庄外国语学校2020-2021学年高一上学期第二阶段考试化学试卷
名校
3 . 利用如图装置进行实验,下列有关实验操作和现象正确的是
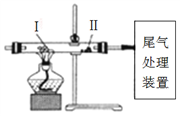

| A.缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色 |
| B.缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色 |
| C.先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积 |
| D.先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色 |
您最近一年使用:0次
2017-04-13更新
|
644次组卷
|
3卷引用:2016-2017学年河北省衡水中学高三下学期期中考试理科综合化学试卷
解题方法
4 . 硫酸亚铁在空气中易被氧化,与硫酸铵反应生成硫酸亚铁铵[化学式为FeSO4·(NH4)2SO4·6H2O]后就不易被氧化。模拟工业制备硫酸亚铁铵晶体的实验装置如下图所示。请回答下列问题:
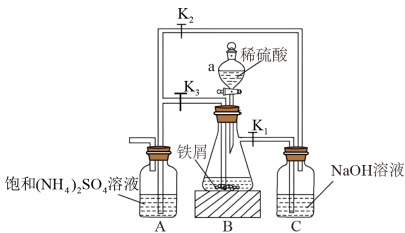
(1)仪器a的名称是______________________ 。
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是___________ ,装置B中发生反应的离子方程式可能是___________ (填序号)。
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是___________ 。反应一段时间后,打开K3,关闭K1和K2。装置B中的溶液会流入装置A,其原因是______________________ 。
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是______________________ 。
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有___________ 、___________ 、洗涤、干燥。
三种盐的溶解度(单位为g/100gH2O)

(1)仪器a的名称是
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有
三种盐的溶解度(单位为g/100gH2O)
温度 | FeSO4 | (NH4)2SO4 | 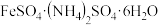 |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
您最近一年使用:0次



