名校
解题方法
1 . CuCl是常见的有机合成催化剂。某实验小组设想用CuCl2和Na2SO3溶液制备CuCl。
资料:①CuCl为难溶于水和酸的白色固体
②CuI为难溶于水的白色固体
③Cu+在酸性环境中易歧化为Cu和
④
Ⅰ.CuCl的制备
(1)用离子方程式表示CuCl制备的设想依据:___________ 。
(2)Na2SO3溶液易变质,使用前需要标定,配制该Na2SO3溶液所需要的玻璃仪器有:试剂瓶、玻璃棒和___________ 。
【实验一】CuCl的制备
(3)将实验一中的白色沉淀分离后,通过___________ (填字母)证明了白色沉淀为CuCl,且不含其他杂质。
A.X射线衍射实验 B.柱色谱 C.核磁共振氢谱
Ⅱ.橙黄色沉淀的成分探究
(4)实验一中橙黄色沉淀存在时间较短,难以获得。为成功制备该沉淀,可将实验一中的CuCl2溶液替换为等体积等浓度的___________ 。
【实验二】实验小组依据体系中相关物质的性质推测:橙黄色沉淀可能为Cu2SO3、CuSO3,或二者的混合物。为进一步证明该推测,实验小组继续做了下列实验。
(5)实验小组观察到实验a中___________ (填字母),证明了橙黄色沉淀中含有Cu2SO3。
A.反应后溶液呈蓝色 B.有紫红色固体析出
(6)若橙黄色沉淀中含有CuSO3,由于___________ ,实验b中上清液呈无色且不能使淀粉溶液变蓝;若橙黄色沉淀仅有Cu2SO3,现象与实验b相同。因此仅通过实验b不能证明橙黄色沉淀中含CuSO3,但可以通过检验上层清液中某种离子的存在证明橙黄色沉淀中含有CuSO3,其实验方案为:___________ 。
资料:①CuCl为难溶于水和酸的白色固体
②CuI为难溶于水的白色固体
③Cu+在酸性环境中易歧化为Cu和

④

Ⅰ.CuCl的制备
(1)用离子方程式表示CuCl制备的设想依据:
(2)Na2SO3溶液易变质,使用前需要标定,配制该Na2SO3溶液所需要的玻璃仪器有:试剂瓶、玻璃棒和
【实验一】CuCl的制备
| 实验操作 | 实验现象 |
 溶液和 溶液和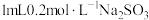 溶液混合 溶液混合 | 立即有橙黄色沉淀生成,3min后沉淀颜色变浅并伴有少量白色沉淀产生,再振荡1min后沉淀全部变为白色。 |
A.X射线衍射实验 B.柱色谱 C.核磁共振氢谱
Ⅱ.橙黄色沉淀的成分探究
(4)实验一中橙黄色沉淀存在时间较短,难以获得。为成功制备该沉淀,可将实验一中的CuCl2溶液替换为等体积等浓度的
【实验二】实验小组依据体系中相关物质的性质推测:橙黄色沉淀可能为Cu2SO3、CuSO3,或二者的混合物。为进一步证明该推测,实验小组继续做了下列实验。
| 实验 | 实验操作 |
| a | 取少量洗净的橙黄色沉淀于试管中,并加入一定量的稀硫酸 |
| b |  注:实验所用试剂均经过除氧处理 |
A.反应后溶液呈蓝色 B.有紫红色固体析出
(6)若橙黄色沉淀中含有CuSO3,由于
您最近一年使用:0次
名校
解题方法
2 . CuCl可用作有机合成的催化剂。工业上用黄铜矿(主要成分是CuFeS2,还含有少量SiO2)制备CuCl的工艺流程如下:
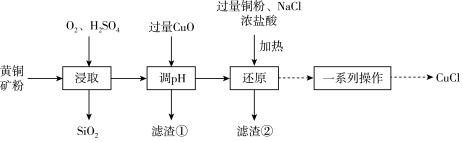
回答下列问题:
(1) 的电子排布式是:
的电子排布式是:_______ 。
(2)“浸取”时,硫元素转化为硫酸根离子,则反应的离子方程式为_______ 。
(3)“滤渣①”的成分是_______ (填化学式)
(4)已知在水溶液中存在平衡: (无色)。“还原”时使用浓盐酸和
(无色)。“还原”时使用浓盐酸和 固体的原因是
固体的原因是_______ ;当出现_______ 现象时,表明“还原”进行完全。
(5)制备 。请补充由还原所得的滤液液制备
。请补充由还原所得的滤液液制备 的操作步骤:
的操作步骤:_______ ,真空干燥。[已知 是一种难溶于水和乙醇的白色固体,潮湿时易被氧化。实验中必须使用的试剂:水、
是一种难溶于水和乙醇的白色固体,潮湿时易被氧化。实验中必须使用的试剂:水、 、
、 、
、 ]。
]。

回答下列问题:
(1)
 的电子排布式是:
的电子排布式是:(2)“浸取”时,硫元素转化为硫酸根离子,则反应的离子方程式为
(3)“滤渣①”的成分是
(4)已知在水溶液中存在平衡:
 (无色)。“还原”时使用浓盐酸和
(无色)。“还原”时使用浓盐酸和 固体的原因是
固体的原因是(5)制备
 。请补充由还原所得的滤液液制备
。请补充由还原所得的滤液液制备 的操作步骤:
的操作步骤: 是一种难溶于水和乙醇的白色固体,潮湿时易被氧化。实验中必须使用的试剂:水、
是一种难溶于水和乙醇的白色固体,潮湿时易被氧化。实验中必须使用的试剂:水、 、
、 、
、 ]。
]。
您最近一年使用:0次
2021-09-15更新
|
383次组卷
|
2卷引用:江苏省如东高级中学2022届高三第一次学情检测化学试题



