1 .  是一种常用的杀菌剂和催化剂。工业上制取
是一种常用的杀菌剂和催化剂。工业上制取 的工艺如图所示(制取
的工艺如图所示(制取 时需补加
时需补加 以保持反应在弱酸性条件下进行)。
以保持反应在弱酸性条件下进行)。

已知:溶液A的主要溶质M为酸式盐;化合物C为正盐;当溶液酸性减弱到一定程度时, 部分转化为
部分转化为 沉淀且满足
沉淀且满足 。
。
回答下列问题:
(1)M的化学式为___________ ;“真空蒸发”的原因是___________ 。
(2)溶液 发生反应的离子方程式为
发生反应的离子方程式为___________ ;若 产量不变,参与反应的化合物
产量不变,参与反应的化合物 与
与 物质的量之比减小时,需补加
物质的量之比减小时,需补加 的量
的量___________ (填“增大”、“减小”或“不变”)。
(3)为探究 的还原性,将一定量
的还原性,将一定量 与某浓度的硝酸反应,溶液的体积为
与某浓度的硝酸反应,溶液的体积为 ,溶液中
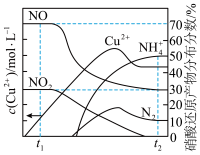
,溶液中 与硝酸还原产物的分布分数随时间的变化如图所示。则
与硝酸还原产物的分布分数随时间的变化如图所示。则 时刻,溶液中发生反应的化学方程式为
时刻,溶液中发生反应的化学方程式为___________ ; 时刻,测得溶液中
时刻,测得溶液中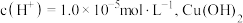 沉淀的质量为
沉淀的质量为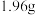 ,则此时溶液中
,则此时溶液中 为
为___________  (忽略溶液体积变化)。
(忽略溶液体积变化)。
 是一种常用的杀菌剂和催化剂。工业上制取
是一种常用的杀菌剂和催化剂。工业上制取 的工艺如图所示(制取
的工艺如图所示(制取 时需补加
时需补加 以保持反应在弱酸性条件下进行)。
以保持反应在弱酸性条件下进行)。
已知:溶液A的主要溶质M为酸式盐;化合物C为正盐;当溶液酸性减弱到一定程度时,
 部分转化为
部分转化为 沉淀且满足
沉淀且满足 。
。回答下列问题:
(1)M的化学式为
(2)溶液
 发生反应的离子方程式为
发生反应的离子方程式为 产量不变,参与反应的化合物
产量不变,参与反应的化合物 与
与 物质的量之比减小时,需补加
物质的量之比减小时,需补加 的量
的量(3)为探究
 的还原性,将一定量
的还原性,将一定量 与某浓度的硝酸反应,溶液的体积为
与某浓度的硝酸反应,溶液的体积为 ,溶液中
,溶液中 与硝酸还原产物的分布分数随时间的变化如图所示。则
与硝酸还原产物的分布分数随时间的变化如图所示。则 时刻,溶液中发生反应的化学方程式为
时刻,溶液中发生反应的化学方程式为 时刻,测得溶液中
时刻,测得溶液中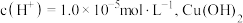 沉淀的质量为
沉淀的质量为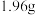 ,则此时溶液中
,则此时溶液中 为
为 (忽略溶液体积变化)。
(忽略溶液体积变化)。
您最近一年使用:0次
名校
2 . CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
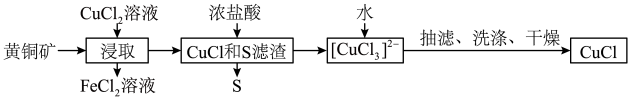
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq) [CuCl3]2-(aq)(无色溶液)
[CuCl3]2-(aq)(无色溶液)
下列叙述错误的是( )

已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)
 [CuCl3]2-(aq)(无色溶液)
[CuCl3]2-(aq)(无色溶液)下列叙述错误的是( )
| A.浸取中的主要反应为CuFeS2+3CuCl2=4CuCl+FeCl2+2S |
| B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板 |
C.加水有利于CuCl(s)+2Cl(aq)- [CuCl3]2-(aq)平衡逆向移动,析出CuCl [CuCl3]2-(aq)平衡逆向移动,析出CuCl |
| D.为提高产率和纯度,可采用乙醇洗涤、真空干燥 |
您最近一年使用:0次
2019-11-13更新
|
282次组卷
|
2卷引用:山东省潍坊昌乐县第二中学2020届高三上学期期末化学模拟试题二



