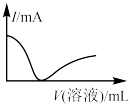
1 . 向一定量的CuSO4溶液中逐滴加入Ba(OH)2溶液至沉淀刚好不再增加,然后再逐滴加入稀盐酸至过量,下列各项中的曲线可近似表示整个过程中混合溶液的导电能力(用电流强度I表示)变化的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 红珊瑚栖息于200~2000米深的海域,它与琥珀、珍珠统称为有机宝石,红珊瑚是由无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,呈红色是因为在海底长期积淀某种元素的氧化物。该元素可能是
| A.Na | B.Fe | C.Si | D.Cu |
您最近半年使用:0次
解题方法
3 . 下列离子反应方程式书写正确的是
A.向酸性高锰酸钾溶液中滴加过氧化氢: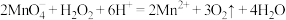 |
B.在氨水中加入少量 溶液: 溶液: |
C.向 溶液中加入 溶液中加入 溶液至 溶液至 沉淀完全 沉淀完全 |
D.苯酚钠溶液中通入少量二氧化碳: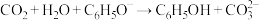 |
您最近半年使用:0次
2024-03-16更新
|
111次组卷
|
2卷引用:浙江省杭州学军中学海创园学校2023-2024学年高二上学期期末考试化学试题
解题方法
4 . 用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备难溶于水的碱式碳酸铜的流程如下:
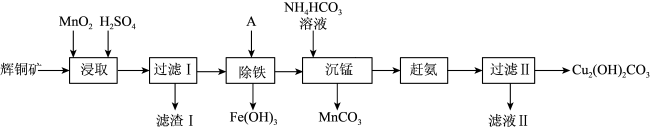
(1)下列措施能加快浸取速率的是___________ 。(填字母)
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)滤渣I中的主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的离子方程式:___________ 。
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________。
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为___________ 。
(5)滤液Ⅱ所含溶质主要是___________ (填化学式)。

(1)下列措施能加快浸取速率的是
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)滤渣I中的主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的离子方程式:
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________。
| A.CO2 | B.CuO | C.氨水 | D.HCl |
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为
(5)滤液Ⅱ所含溶质主要是
您最近半年使用:0次
5 . 下表中,对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是
| 选项 | 陈述I | 陈述II | 判断 |
| A | 碳酸钠溶液显碱性 | 碳酸钠可做胃酸中和剂 | I对,II对,无 |
| B | Fe2+可以与酸性 KMnO4 发生氧化还原反应,能使酸性高锰酸钾溶液褪色 | 用酸性 KMnO4 溶液检验 Fe2(SO4)3溶液中是否含有 FeSO4 | I对,II对,有 |
| C | 铝单质既能与盐酸反应放出氢气,又能与氢氧化钠溶液反应放出氢气 | 常温下铝制容器可以盛装浓硫酸 | I对,II对,有 |
| D | 铜绿的主要成分是碱式碳酸铜,碱式碳酸铜能溶于稀盐酸 | 可用盐酸除去铜器表面的铜绿 | I对,II错,无 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 化学与生活、社会发展息息相关。下列叙述不正确 的是
| A.维生素C有较强的还原性,在部分食品中添加适量维生素C可以延长食品的保质期 |
B.我国十大科技成果之一的“纳米氮化镓 ”是一种胶体 ”是一种胶体 |
| C.“熬胆矾铁釜,久之亦化为铜”,该过程涉及置换反应 |
D.“纳米汽车”用 作车轮, 作车轮, 、金刚石和石墨互为同素异形体 、金刚石和石墨互为同素异形体 |
您最近半年使用:0次
名校
解题方法
7 . 由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向含有浓度相同的Na2S和NaCl的混合溶液中滴入少量AgNO3溶液 | 先产生黑色沉淀 | 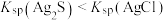 |
B | 某钾盐晶体中滴加浓盐酸,产生的气体通入品红溶液中 | 品红溶液褪色 | 产生的气体可能是Cl2 |
C | 将SO2通入Ca(ClO)2溶液 | 出现白色沉淀 | SO2是酸性氧化物 |
D | 向盛有CuO的试管中加入足量HI溶液,充分振荡后滴入3滴淀粉溶液 | 固体由黑色变为白色,溶液变为黄色,滴入淀粉后溶液变蓝 | HI既体现了还原性又体现了酸性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 某变质的废铜屑主要成分为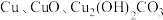 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是

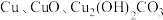 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
A.基态铜原子的价层电子排布式为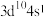 |
B.滤液1的溶质主要成分为 |
C.若分铜过程生成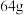 铜,则浸泡过程理论上有 铜,则浸泡过程理论上有 电子转移 电子转移 |
D.可用铁氰化钾溶液检验滤液2中 的存在 的存在 |
您最近半年使用:0次
名校
9 . 化学小组同学学习了  与
与  反应后,猜想
反应后,猜想  也能与
也能与  发生反应。为了验证猜想,进行实验。
发生反应。为了验证猜想,进行实验。
(1)【实验探究】
【实验假设】
甲同学分析了实验Ⅰ无明显现象的原因,做出如下假设:
假设 : 由于反应温度较低,导致
: 由于反应温度较低,导致  氧化性较弱。假设
氧化性较弱。假设 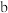 : 由于
: 由于_____________ ,导致  氧化性较弱。(补全假设
氧化性较弱。(补全假设  )
)
针对上述假设,甲同学继续进行如下实验:
【实验探究】
实验结果:实验Ⅰ和实验Ⅱ均未检测出  。
。
(2)【实验探究】
乙同学用 溶液代替
溶液代替  溶液进行实验:
溶液进行实验:
实验 Ⅳ中发生的离子反应方程式为_____________ 。
(3)【实验改进】
乙同学针对实验 Ⅰ进行改进,设计并完成实验Ⅴ: 向试管 中加入几滴浓盐酸,一段时间后,溶液蓝色明显变浅,铜片表面产生白色沉淀。
中加入几滴浓盐酸,一段时间后,溶液蓝色明显变浅,铜片表面产生白色沉淀。
乙同学因此得出结论: 对
对  与
与  发生反应有促进作用。
发生反应有促进作用。
①丙同学认为通过实验Ⅴ不能得出乙同学的结论,原因是_____________ 。
②丙同学继续设计实验:_____________ (填操作和现象),证实了乙同学结论合理。
(4)【结论分析】
综合上述实验可知, 能否氧化
能否氧化  与
与_____________ 有关。
 与
与  反应后,猜想
反应后,猜想  也能与
也能与  发生反应。为了验证猜想,进行实验。
发生反应。为了验证猜想,进行实验。(1)【实验探究】
实验Ⅰ |
|
甲同学分析了实验Ⅰ无明显现象的原因,做出如下假设:
假设
 : 由于反应温度较低,导致
: 由于反应温度较低,导致  氧化性较弱。假设
氧化性较弱。假设 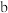 : 由于
: 由于 氧化性较弱。(补全假设
氧化性较弱。(补全假设  )
)针对上述假设,甲同学继续进行如下实验:
【实验探究】
序号 | 实验 | 加入试剂或操作 |
实验Ⅱ |
| 加热试管 |
实验Ⅲ | 加入 |
 。
。(2)【实验探究】
乙同学用
 溶液代替
溶液代替  溶液进行实验:
溶液进行实验:实验Ⅳ |
|
(3)【实验改进】
乙同学针对实验 Ⅰ进行改进,设计并完成实验Ⅴ: 向试管
 中加入几滴浓盐酸,一段时间后,溶液蓝色明显变浅,铜片表面产生白色沉淀。
中加入几滴浓盐酸,一段时间后,溶液蓝色明显变浅,铜片表面产生白色沉淀。乙同学因此得出结论:
 对
对  与
与  发生反应有促进作用。
发生反应有促进作用。①丙同学认为通过实验Ⅴ不能得出乙同学的结论,原因是
②丙同学继续设计实验:
(4)【结论分析】
综合上述实验可知,
 能否氧化
能否氧化  与
与
您最近半年使用:0次
10 . 某废旧金属材料中主要为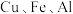 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾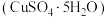 的一种流程如下:
的一种流程如下: 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。
回答下列问题:
(1)“破碎”的目的是___________ 。
(2)“碱浸”时发生反应的离子方程式为___________ 。
(3)“酸浸、氧化”的温度不宜过高,原因是___________ ;“滤渣2”的主要成分是___________ (填化学式)。
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有 的是___________。
的是___________。
(5)测定产品的纯度:准确称取胆矾样品 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为___________ (保留3位有效数字)。
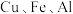 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾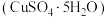 的一种流程如下:
的一种流程如下: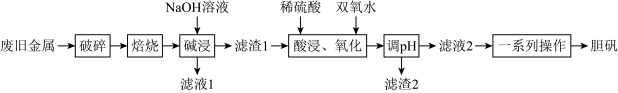
 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。回答下列问题:
(1)“破碎”的目的是
(2)“碱浸”时发生反应的离子方程式为
(3)“酸浸、氧化”的温度不宜过高,原因是
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有
 的是___________。
的是___________。A. 溶液,新制氯水 溶液,新制氯水 | B.酸性高锰酸钾溶液 |
C. 溶液 溶液 | D.淀粉 试纸 试纸 |
(5)测定产品的纯度:准确称取胆矾样品
 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为
您最近半年使用:0次



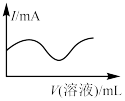


 固体,振荡
固体,振荡


