1 . 二草酸合铜(Ⅱ)酸钾( )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸( )溶液中加入适量
)溶液中加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)长期存放的 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是_______ 。
 )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:Ⅰ.取已知浓度的
 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。Ⅱ.向草酸(
 )溶液中加入适量
)溶液中加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)长期存放的
 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是
您最近半年使用:0次
解题方法
2 . 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值。但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)某青铜器中 Sn、Pb的质量分别为 119g、20.7g,则该青铜器中 Sn和Pb原子的数目之比为___________ 。
(2)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分 CuCl发生复分解反应,该化学方程式为___________ 。
(3)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
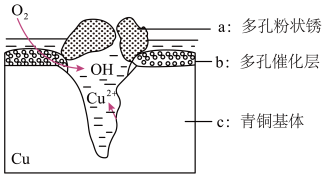
①腐蚀过程中, 负极是___________ (填“a”或“b”或“c”);
②环境中的 Cl⁻扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状铜锈Cu2(OH)3Cl,其离子方程式为___________ 。
(1)某青铜器中 Sn、Pb的质量分别为 119g、20.7g,则该青铜器中 Sn和Pb原子的数目之比为
(2)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分 CuCl发生复分解反应,该化学方程式为
(3)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中, 负极是
②环境中的 Cl⁻扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状铜锈Cu2(OH)3Cl,其离子方程式为
您最近半年使用:0次
3 . 按要求回答下列问题
(1)胆矾的化学式:___________ 。
(2)写出异丁烷的结构简式:___________ 。
(3)用化学方程式表示粗硅的制备:___________ 。
(1)胆矾的化学式:
(2)写出异丁烷的结构简式:
(3)用化学方程式表示粗硅的制备:
您最近半年使用:0次
解题方法
4 . 回答下列问题:
(1)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即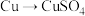 ;
;
方案乙:由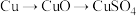 。
。
这两种方案,你认为哪一种方案更合理?_______ ,理由是_______ 。
(2)氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
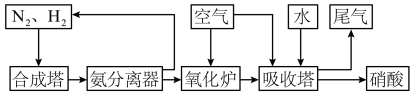
①合成塔中发生反应的化学方程式为_______ 。
②向吸收塔中通入空气的作用是_______ 。
③氧化炉中发生反应的化学方程式为_______ 。标准状况下,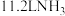 被氧化为
被氧化为 时转移电子的数目为
时转移电子的数目为_______ 。
④吸收塔中出来的尾气 可用具有碱性的
可用具有碱性的 溶液吸收,其中
溶液吸收,其中 既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:_______ 。
(1)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
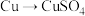 ;
;方案乙:由
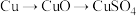 。
。这两种方案,你认为哪一种方案更合理?
(2)氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

①合成塔中发生反应的化学方程式为
②向吸收塔中通入空气的作用是
③氧化炉中发生反应的化学方程式为
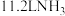 被氧化为
被氧化为 时转移电子的数目为
时转移电子的数目为④吸收塔中出来的尾气
 可用具有碱性的
可用具有碱性的 溶液吸收,其中
溶液吸收,其中 既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
您最近半年使用:0次
名校
5 . Cl2、H2SO4、SO2都是化工生产中的重要物质。请回答下列问题:
(1)化工厂可用浓氨水来检验 是否泄漏,当有少量
是否泄漏,当有少量 泄漏时,发生反应的化学方程式为
泄漏时,发生反应的化学方程式为__________ ,若反应中有0.08mol的氨气被氧化,则转移的电子数目是____________ 。
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为_________ 。上述两种方法中,制取硫酸铜的最佳方法是_______ (填“①”或“②”),理由是___________ 。
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
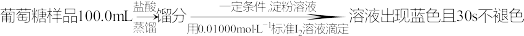 (已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液20.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________ g∙L−1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________ (填“偏高”、“偏低”或“不变”)
(1)化工厂可用浓氨水来检验
 是否泄漏,当有少量
是否泄漏,当有少量 泄漏时,发生反应的化学方程式为
泄漏时,发生反应的化学方程式为(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
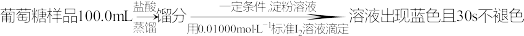 (已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)①按上述方案实验,消耗标准I2溶液20.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为
②在上述实验过程中,若有部分HI被空气氧化,则测定结果
您最近半年使用:0次
名校
解题方法
6 . 从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如下,根据要求回答有关问题:
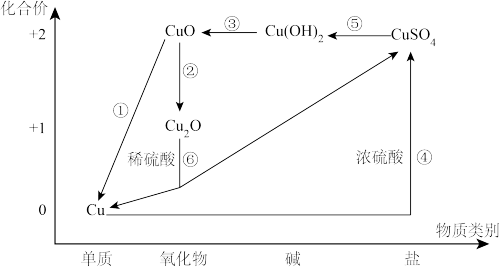
(1)Cu2(OH)2CO3是铜绿的主要成分,其属于_______ (填序号)。
a、碱b、正盐c、碱式盐d、酸式盐e、碳酸盐
(2)转化②中铜元素被_______ (填“氧化”或“还原”)。
(3)转化④的化学方程式为_______ 。
(4)转化⑤的反应类型为_______ (填基本反应类型),Cu(OH)2为_______ (填“强”、“弱”或“非”)电解质。
(5)已知Cu2O为砖红色不溶于水的固体,转化⑥可生成Cu、CuSO4溶液和另一种物质,则转化⑥的离子方程式为_______ 。
(6)Cu2O与稀HNO3可以发生氧化还原反应,完成并配平下列方程式:_______ 。
_______Cu2O+_______HNO3=_______Cu(NO3)2+_______NO↑+_______

(1)Cu2(OH)2CO3是铜绿的主要成分,其属于
a、碱b、正盐c、碱式盐d、酸式盐e、碳酸盐
(2)转化②中铜元素被
(3)转化④的化学方程式为
(4)转化⑤的反应类型为
(5)已知Cu2O为砖红色不溶于水的固体,转化⑥可生成Cu、CuSO4溶液和另一种物质,则转化⑥的离子方程式为
(6)Cu2O与稀HNO3可以发生氧化还原反应,完成并配平下列方程式:
_______Cu2O+_______HNO3=_______Cu(NO3)2+_______NO↑+_______
您最近半年使用:0次
2022-04-06更新
|
261次组卷
|
3卷引用:福建省龙岩第一中学2021-2022学年高一下学期第一次月考化学试题
解题方法
7 . (1)①写出胆矾的化学式___________
②写出葡萄糖的结构简式___________
(2)写出红热的铁与水蒸气反应的化学方程式___________
(3)写出氯化铝溶液中滴加过量氨水的离子反应方程式___________
②写出葡萄糖的结构简式
(2)写出红热的铁与水蒸气反应的化学方程式
(3)写出氯化铝溶液中滴加过量氨水的离子反应方程式
您最近半年使用:0次
20-21高二下·浙江·阶段练习
8 . 牙膏是生活必需品。下面是牙膏中某些主要成分的检验流程图:
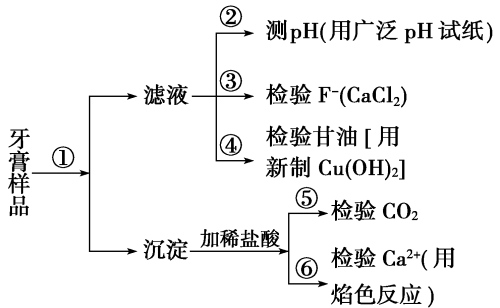
请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是_______ ,所需要的主要玻璃仪器有_______ 。
(2)在②中用pH试纸测溶液的pH的操作方法是_______ 。
(3)写出④中发生反应的化学方程式_______ 。
(4)在⑥中检验Ca2+的存在,除可用焰色反应外,还可利用Ca2+和_______ 溶液的反应来进行。

请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是
(2)在②中用pH试纸测溶液的pH的操作方法是
(3)写出④中发生反应的化学方程式
(4)在⑥中检验Ca2+的存在,除可用焰色反应外,还可利用Ca2+和
您最近半年使用:0次
9 . (1) NH3的电子式_____
(2)胆矾的化学式_____
(3)工业上制粗硅的反应方程式_____
(2)胆矾的化学式
(3)工业上制粗硅的反应方程式
您最近半年使用:0次
10 . 铜是重要的工业原料,现有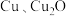 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 该混合物加入
该混合物加入 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 ,且生成
,且生成 (标准状况)的
(标准状况)的 。向所得溶液中加入
。向所得溶液中加入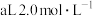 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 沉淀完全。
沉淀完全。
(1) 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为___________ ;
(2)
___________ L。
(3)求混合物中 的质量分数
的质量分数___________ ?(没有计算过程不得分)
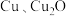 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 该混合物加入
该混合物加入 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 ,且生成
,且生成 (标准状况)的
(标准状况)的 。向所得溶液中加入
。向所得溶液中加入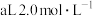 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 沉淀完全。
沉淀完全。(1)
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(2)

(3)求混合物中
 的质量分数
的质量分数
您最近半年使用:0次



