解题方法
1 . 用纯净干燥的氯气与铜反应,装置如下图所示。(已知:生成物为粉末状,易潮解)

(1)实验前先通一会儿氯气以排出装置内的空气,判断氯气已充满整个装置的简单方法是________ 。
(2)干燥的氯气通过灼热铜粉时,A中可观察到________ ,有关反应的化学方程式是________ 。
(3)用氯气将A中的生成物吹入B中进行冷却收集,B与A相连的导管较粗,其目的是________ 。实验结束后,取下B,向其中倒入水,振荡,观察到溶液的颜色是________ ,说明其中含有________ 离子。

(1)实验前先通一会儿氯气以排出装置内的空气,判断氯气已充满整个装置的简单方法是
(2)干燥的氯气通过灼热铜粉时,A中可观察到
(3)用氯气将A中的生成物吹入B中进行冷却收集,B与A相连的导管较粗,其目的是
您最近一年使用:0次
2 . 氯化铜是重要的化工原料,广泛用做有机合成催化剂。实验室可用如图所示装置,用还原铜粉和氯气来制备氯化铜,已知:氯化铜容易潮解。

(1)配平A装置中发生化学反应的方程式:____ KMnO4+_____ HCl(浓) =_____ KCl+_____ MnCl2 + ____ Cl2↑+ _____ H2O,装浓盐酸的仪器名称是____________ 。
(2)B装置的作用是____________ ,C装置中的试剂是____________ 。E装置的作用是____________ 。
(3)F中发生的化学反应的离子方程式为____________ 。
(4)当Cl2排尽空气后,加热D,装置D中的现象是____________ 。
(5)某同学用不纯的铜粉(含少量铁粉)进行实验。铜粉和铁粉完全反应后,取少量产物于一洁净的试管中,加水溶解,再加入____________ (填试剂),出现_____________ (填现象),则证明产物中含有 FeCl3。
(6)用15.8 g KMnO4固体与足量的浓盐酸反应,被氧化的HCl是____________ mol。

(1)配平A装置中发生化学反应的方程式:
(2)B装置的作用是
(3)F中发生的化学反应的离子方程式为
(4)当Cl2排尽空气后,加热D,装置D中的现象是
(5)某同学用不纯的铜粉(含少量铁粉)进行实验。铜粉和铁粉完全反应后,取少量产物于一洁净的试管中,加水溶解,再加入
(6)用15.8 g KMnO4固体与足量的浓盐酸反应,被氧化的HCl是
您最近一年使用:0次
名校
解题方法
3 . (1)研究氯气跟金属的反应时,选用金属铜进行实验。用坩埚钳夹住一束铜丝,灼热后立刻放入充满氯气的集气瓶里。铜丝燃烧后把少量水注入集气瓶里,用玻璃片盖住瓶口,振荡。
①根据哪些实验现象可判断铜丝燃烧后生成了+2价铜的化合物:_______________ 。
②反应的化学方程式为_____________________________________ 。
(2)研究浓硫酸的强氧化性时,选用金属铜跟浓硫酸进行实验,实验装置如下图所示。

①乙中的现象_______ ,试管中的浸有碱液的棉花的作用是____________ 。
②甲中的反应方程式为_____________________________________ 。
(3)上述两个实验为什么都选金属铜作样本来进行实验________ 。
A.铜是一种不活泼金属
B.选用铜作实验可以推测更多金属跟氯气或浓硫酸反应的情况
C.铜是一种常见金属
D.铜跟氯气或浓硫酸反应可生成有色溶液,现象明显
①根据哪些实验现象可判断铜丝燃烧后生成了+2价铜的化合物:
②反应的化学方程式为
(2)研究浓硫酸的强氧化性时,选用金属铜跟浓硫酸进行实验,实验装置如下图所示。

①乙中的现象
②甲中的反应方程式为
(3)上述两个实验为什么都选金属铜作样本来进行实验
A.铜是一种不活泼金属
B.选用铜作实验可以推测更多金属跟氯气或浓硫酸反应的情况
C.铜是一种常见金属
D.铜跟氯气或浓硫酸反应可生成有色溶液,现象明显
您最近一年使用:0次
2019-01-10更新
|
174次组卷
|
3卷引用:【全国百强校】山东省招远市第一中学2018-2019学年高一上学期12月月考化学试题
4 . 某研究小组利用下图所示实验装置(部分加持装置已略去)制备无水CuCl2,并对实验过程中污染性气体进行处理。已知CuCl2易潮解。请回答以下问题:

(1)用上图五个装置制取CuCl2,其连接顺序为______________ (按气流方向,用小写字母表示)。
(2)装置I中发生反应的离子方程式为_____________________________________ 。
(3)装置III干燥管中氯化钙的作用是______________________________ 。
(4)实验开始时,先点燃装置________ (填“I”或“II”)处的酒精灯。
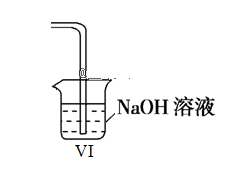
(5)本实验中,用如图装置VI代替装置V是否可行______________ (填 写“可行”或“不可行”)
(6)实验结束后,先关闭装置I处分液漏斗活塞, 再关闭装置IV的g处(用止水夹夹住),此时装置IV中长颈漏斗的作用是_________ 。

(1)用上图五个装置制取CuCl2,其连接顺序为
(2)装置I中发生反应的离子方程式为
(3)装置III干燥管中氯化钙的作用是
(4)实验开始时,先点燃装置
(5)本实验中,用如图装置VI代替装置V是否可行

(6)实验结束后,先关闭装置I处分液漏斗活塞, 再关闭装置IV的g处(用止水夹夹住),此时装置IV中长颈漏斗的作用是
您最近一年使用:0次
2018-12-18更新
|
106次组卷
|
2卷引用:山东省新泰二中2019届高三上学期12月月考化学试题
名校
5 . 湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。一种由铜镉渣生产金属镉的流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
⑴浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是______ 。
⑵除钴过程中,锌粉会与As2O3形成微电池产生AsH3。该微电池的正极反应式为__________ 。
⑶除铁时先加入适量KMnO4,再加入ZnO调节pH。
①除铁过程中,理论上参加反应的物质n(KMnO4): n(Fe2+)=_____ 。
②除铁时加入ZnO控制反应液pH的范围为______ 。
⑷若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:____ 。
⑸净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是__________ 。

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
⑴浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是
⑵除钴过程中,锌粉会与As2O3形成微电池产生AsH3。该微电池的正极反应式为
⑶除铁时先加入适量KMnO4,再加入ZnO调节pH。
①除铁过程中,理论上参加反应的物质n(KMnO4): n(Fe2+)=
②除铁时加入ZnO控制反应液pH的范围为
⑷若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:
⑸净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是
您最近一年使用:0次
2017-02-26更新
|
1185次组卷
|
4卷引用:2017届江苏省盐城中学高三下学期开学考试化学试卷
解题方法
6 . 分A、B、C、D四种物质,A是红色固体,B是黑色固体,各物质间的转化关系如下图,根据推断写出下列物质的化学式:A.__________ ,B.________ ,C.________ ,D.________ 。
写出C生成D的化学方程式_____________________ 。

写出C生成D的化学方程式

您最近一年使用:0次
解题方法
7 . 铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2·2H2O )的流程如下。

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________ (填代号)。
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________ 。
(2)由溶液Ⅱ制备CuCl2·2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________ (填操作名称)、过滤、洗涤干燥。
(3)向0.1 mol·L-1的CuCl2溶液中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:_____________ 若KSP[CuS]=1.2×10-36 ,则生成沉淀时需要S2-的浓度为________ mol·L-1。
(4)某学习小组用碘量法测定CuCl2·2H2O样品的纯度(杂质不发生反应)。实验如下:
a.准确称取CuCl2·2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知:2Cu2++4I-=2CuI+I2)
b.移取25.00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol·L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。(已知:I2+2S2O32-=2I-+S4O62-)
①实验中使用的指示剂名称为____________ ,达到滴定终点时,溶液颜色变化为______________ 。
②该样品中CuCl2·2H2O 的质量分数为_________ (用含m、c、V的代数式表示,不用化简)。

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是
(2)由溶液Ⅱ制备CuCl2·2H2O的操作依次为:边滴加浓盐酸边加热浓缩、
(3)向0.1 mol·L-1的CuCl2溶液中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:
(4)某学习小组用碘量法测定CuCl2·2H2O样品的纯度(杂质不发生反应)。实验如下:
a.准确称取CuCl2·2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知:2Cu2++4I-=2CuI+I2)
b.移取25.00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol·L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。(已知:I2+2S2O32-=2I-+S4O62-)
①实验中使用的指示剂名称为
②该样品中CuCl2·2H2O 的质量分数为
您最近一年使用:0次
8 . 实验室里用下列药品和仪器来制取纯净的无水氯化铜:

图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
(1)如果所制得气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
__________ 接__________ 接________ 接_______ 接_______ 接_______ ;
其中,②与④装置相连时,玻璃管接口(用装置中字母表示)应是接______________ 。
(2)装置⑥中发生反应的离子方程式是______________________________ 。
(3)实验开始时,应首先检验装置的____________ ;实验结束时,应先熄灭________ 处的酒精灯。
(4)在装置⑤的烧杯中,发生反应的化学方程式为______________ 。
(5)待充分反应后,装置①的玻璃管中呈____ 色。冷却后,将制得的产物配成溶液,溶液呈_______ 色。
(6)若反应中有71gCl2生成,则被氧化的HCl的物质的量为__________ ,转移电子数为_________ 。

图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
(1)如果所制得气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
其中,②与④装置相连时,玻璃管接口(用装置中字母表示)应是接
(2)装置⑥中发生反应的离子方程式是
(3)实验开始时,应首先检验装置的
(4)在装置⑤的烧杯中,发生反应的化学方程式为
(5)待充分反应后,装置①的玻璃管中呈
(6)若反应中有71gCl2生成,则被氧化的HCl的物质的量为
您最近一年使用:0次
2016-12-09更新
|
289次组卷
|
2卷引用:2014-2015山东省乐陵市第一中学高一下学期期中化学试卷



