1 . “水煤气(CO和 )”是化学工业常用的原料气,请回答:
)”是化学工业常用的原料气,请回答:
I.已知:焦炭、CO的标准燃烧热分别为 、
、 ,氢气燃烧的热化学反应方程式:
,氢气燃烧的热化学反应方程式: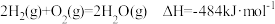
(1)试写出由焦炭和水蒸气生成水煤气的热化学反应方程式:___________
(2)下列说法正确的是___________
II.合成氨工厂以“水煤气”为原料,采用两段间接换热式绝热反应器(反应器中的催化剂对原料气的吸附时间长短,对原料气的转化率会造成一定影响)在常压下进行转换合成氨,装置如图。
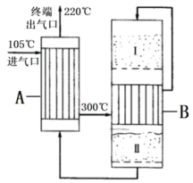
A反应器中主要发生的反应为: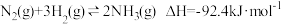
B反应器中主要发生的反应为:
主反应: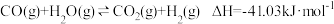
副反应:
由进气口充入一定量含CO、 、
、 、
、 的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、
的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、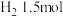 、
、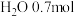 、
、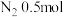 、
、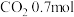 和
和 。
。
已知标准平衡常数: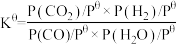 ,其中
,其中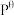 表示标准压强(
表示标准压强( )
)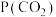 、
、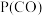 、
、 、
、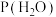 表示各组分的分压,如
表示各组分的分压,如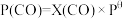 ,
, 为体系中CO的物质的量分数
为体系中CO的物质的量分数
(3)T℃时,主反应的压强平衡常数
___________
(4)平衡时CO的转化率为___________
(5)进气空速对反应产品的收率有一定的影响,实验测得在不同进气空速下,测得平衡时 的收率如下图所示
的收率如下图所示
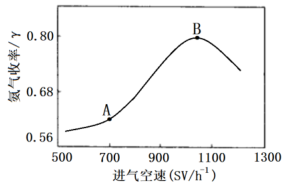
①曲线中A点到B点变化的原因是:___________
②若将绝热转换反应器改为恒温转换反应器,试在图中画出随进气空速变化的 收率曲线
收率曲线___ 。
 )”是化学工业常用的原料气,请回答:
)”是化学工业常用的原料气,请回答:I.已知:焦炭、CO的标准燃烧热分别为
 、
、 ,氢气燃烧的热化学反应方程式:
,氢气燃烧的热化学反应方程式: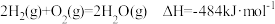
(1)试写出由焦炭和水蒸气生成水煤气的热化学反应方程式:
(2)下列说法正确的是___________
| A.将煤炭在空气中直接加强热进行干馏,制备生成水煤气的原料焦炭 |
| B.水煤气可经过催化合成获得液体燃料、碳氢化合物和含氧有机物 |
| C.水煤气也可采用高温下煤和水蒸气直接作用制得 |
| D.在恒压反应釜中,利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气的流速,有利于水煤气的生成 |
II.合成氨工厂以“水煤气”为原料,采用两段间接换热式绝热反应器(反应器中的催化剂对原料气的吸附时间长短,对原料气的转化率会造成一定影响)在常压下进行转换合成氨,装置如图。

A反应器中主要发生的反应为:
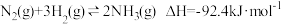
B反应器中主要发生的反应为:
主反应:
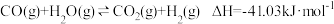
副反应:

由进气口充入一定量含CO、
 、
、 、
、 的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、
的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、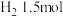 、
、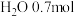 、
、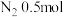 、
、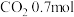 和
和 。
。已知标准平衡常数:
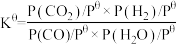 ,其中
,其中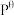 表示标准压强(
表示标准压强( )
)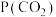 、
、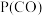 、
、 、
、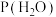 表示各组分的分压,如
表示各组分的分压,如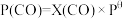 ,
, 为体系中CO的物质的量分数
为体系中CO的物质的量分数(3)T℃时,主反应的压强平衡常数

(4)平衡时CO的转化率为
(5)进气空速对反应产品的收率有一定的影响,实验测得在不同进气空速下,测得平衡时
 的收率如下图所示
的收率如下图所示
①曲线中A点到B点变化的原因是:
②若将绝热转换反应器改为恒温转换反应器,试在图中画出随进气空速变化的
 收率曲线
收率曲线
您最近一年使用:0次
2021-10-20更新
|
637次组卷
|
3卷引用:2021年海南高考化学试题变式题11-19
名校
解题方法
2 . I.甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应I:CH3OH(g) HCHO(g)+H2(g) △H1=+85.2kJ/mol
HCHO(g)+H2(g) △H1=+85.2kJ/mol
反应II:CH3OH(g)+ O2(g)⇌HCHO(g)+H2O(g) △H2
O2(g)⇌HCHO(g)+H2O(g) △H2
反应III:2H2(g)+O2(g)⇌2H2O(g) △H3=-483.6kJ/mol
(1)计算反应Ⅱ的反应热△H2=_____________________________ 。
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g)⇌HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________ (用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
II.CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(3)CO2用于生产乙烯,已知:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定条件下,按不同的投料比X[X= ]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
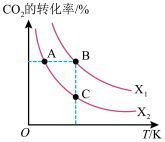
①X1_____ X2(填“>”或“<”,后同),Q_____ 0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为_____ 。
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=_____ [常温下K1(H2CO3)=4.4×10﹣7、K2(H2CO3)=5×10﹣11]。
②欲用5L Na2CO3溶液将23.3g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为__________ 。[已知:常温下Ksp(BaSO4)=1×10﹣7、Ksp(BaCO3)=2.5×10﹣6]。(忽略溶液体积积的变化)
反应I:CH3OH(g)
 HCHO(g)+H2(g) △H1=+85.2kJ/mol
HCHO(g)+H2(g) △H1=+85.2kJ/mol反应II:CH3OH(g)+
 O2(g)⇌HCHO(g)+H2O(g) △H2
O2(g)⇌HCHO(g)+H2O(g) △H2反应III:2H2(g)+O2(g)⇌2H2O(g) △H3=-483.6kJ/mol
(1)计算反应Ⅱ的反应热△H2=
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g)⇌HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=
II.CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(3)CO2用于生产乙烯,已知:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定条件下,按不同的投料比X[X=
 ]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
①X1
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=
②欲用5L Na2CO3溶液将23.3g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为
您最近一年使用:0次
2019-03-14更新
|
741次组卷
|
5卷引用:海南省琼海市嘉积第三中学2021-2022学年高三下学期第三次月考化学科试题
海南省琼海市嘉积第三中学2021-2022学年高三下学期第三次月考化学科试题 【校级联考】江西省重点中学盟校2019届高三上学期第一次联考化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(三)山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题云南民族大学附属中学2019-2020学年高二下学期期中考试化学试题



