真题
名校
1 . 已知:2CO(g)+O2(g)=2CO2(g) ΔH=" --" 566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ 1/2O2(g)ΔH=" --226" kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )

Na2O2(s)+CO2(g)=Na2CO3(s)+ 1/2O2(g)ΔH=" --226" kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )

| A.CO的燃烧热为283 kJ |
| B.上图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH< --452 kJ/mol |
| D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023 |
您最近一年使用:0次
2019-01-30更新
|
1533次组卷
|
18卷引用:2009年普通高等学校招生统一考试理综试题化学部分(天津卷)
2009年普通高等学校招生统一考试理综试题化学部分(天津卷)2009高考真题汇编-化学计算(已下线)北京市门头沟区2010年高三一模(理科综合)化学部分(已下线)2010年天津市天津一中高三第五次月考(理综)化学部分(已下线)2010年黑龙江牡丹江一中高二上学期期中考试化学试卷(已下线)2010~2011学年辽宁省瓦房店市高级中学高一下学期期末考试(已下线)2011-2012学年江西省上饶县中学高二第一次月考化学试卷(已下线)2010-2011学年北京市密云二中高二下期3月份月考化学试卷(已下线)2013届吉林省长春外国语学校高三第一次月考化学试卷2016届河南省顶级名校高三上学期期中测试化学试卷【全国百强校】辽宁省鞍山市第一中学2017-2018学年高一下学期期中考试化学试题(已下线)2010年安徽师大附中高二第二学期期中考查(已下线)09~10学年浙江舟山七校高二下学期期末考试化学试题(已下线)2012届浙江省东阳中学高三下学期阶段检测化学试卷(已下线)2011-2012学年安徽省安工大附中、红星中学高二3月联考化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高一下学期期中考试化学试卷2015-2016学年江苏省启东中学高二上期中选修化学试卷湖南师大附属颐华学校2022-2023学年高二上学期入学考试化学试题
2 . 下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
①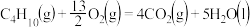
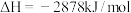
②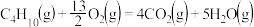
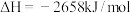
③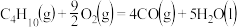

④
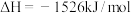
由此判断,正丁烷的燃烧热是
①
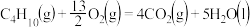
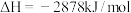
②
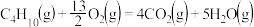
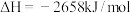
③
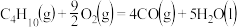

④

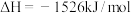
由此判断,正丁烷的燃烧热是
| A.-2878kJ/mol | B.-2658kJ/mol | C.-1746kJ/mol | D.-1526kJ/mol |
您最近一年使用:0次
2016-12-09更新
|
2875次组卷
|
42卷引用:2010年普通高等学校招生统一考试理综试题化学部分(全国卷II)
2010年普通高等学校招生统一考试理综试题化学部分(全国卷II)(已下线)2013-2014河北省邯郸市馆陶县第一中学高二7月调研考试化学试卷2015-2016学年河南省三门峡市陕州中学高二上学期入学考试化学试卷2016-2017学年内蒙古集宁一中高二上期中化学试卷2016-2017学年山西省怀仁县第一中学高二下学期第一次月考化学试卷河南省襄城高中2017-2018学年高二9月月考化学试题甘肃省兰州第一中学2017-2018学年高二12月月化学试题步步为赢 高二化学暑假作业:作业七 化学反应与能量(已下线)2019年8月26日《每日一题》人教选修4—— 燃烧热的概念及判断河北省张家口一中2019-2020学年高二(衔接班)上学期入学考试化学试题广西宾阳县宾阳中学2019-2020学年高二9月月考化学试题四川省遂宁市第二中学2019-2020学年高二上学期期中考试化学试题陕西省咸阳市西藏民族大学附属中学2019-2020学年高二上学期期中考试化学试题四川省武胜烈面中学校2019-2020学年高二下学期开学考试化学试题(已下线)1.1.2 热化学方程式(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)1.1.2 热化学方程式 燃烧热(练习)——2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)1.2 燃烧热 能源(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第一章 化学反应与能量(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)河南省正阳高中2020-2021学年高二下学期第三次素质检测化学试题吉林省长春市第二十九中学2021-2022学年高二上学期第一学程考试化学试题河南省濮阳县实验高中2021-2022学年高二上学期第二次月考化学试题(已下线)1.1.2 热化学方程式 燃烧热(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)第一章 化学反应的热效应(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)BBWYhjhx1102海南省海口市秀英区某校2023-2024学年高二上学期期中检测化学试题(已下线)2010年云南省玉溪一中高二下学期期末考试化学试题(已下线)2011届广东省中山市高三化学模拟试卷(八)(已下线)2011-2012年海南省海南中学高二下学期期中考试理科化学试卷(已下线)2013届贵州晴隆民族中学高三上学期期中考试理科综合化学试卷(已下线)2013学年海南省琼海市嘉积中学高一下学期教学质量监测(二)理科化学卷(已下线)2014-2015学年北京市第六十六中学高二上第一次质量检测化学试卷西藏自治区日喀则市南木林高级中学2019届高三第一次月考理综化学试题江西省吉安县第三中学2018-2019学年高二上学期第一次月考化学试题云南省曲靖市罗平县第三中学2020届高二下学期开学考试化学试题宁夏石嘴山市第三中学2020-2021学年高二上学期第一次月考化学试题西藏自治区林芝市第二高级中学2020-2021学年高二上学期第二学段考试理综化学试题云南省玉溪第二中学2020-2021学年高二上学期期中质量检测化学试题湖南省名校联考联合体2021-2022学年高二上学期12月大联考化学试题广东省深圳实验学校高中部2022-2023学年高二上学期第一阶段考试化学试题广西玉林市博白县中学2023-2024学年高三上学期10月月考化学试题新疆伊犁州霍城县江苏中学2023-2024学年高二上学期9月月考化学试卷广东省汕头市潮南区龙岭中英文学校2023-2024学年高二上学期10月月考化学试题
真题
3 . 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________ kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________ ;
(3)在溶积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
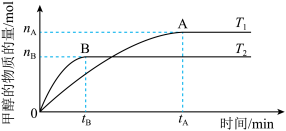
下列说法正确的是________ (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)= mol·L-1·min-1
mol·L-1·min-1
②该反应在T时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为______ ;
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为________ 、正极的反应式为________ 。理想状态下,该燃料电池消耗1mol甲醇所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为________ (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
(1)用太阳能分解10mol水消耗的能量是
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)在溶积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);

下列说法正确的是
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=
 mol·L-1·min-1
mol·L-1·min-1②该反应在T时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时
 增大
增大(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为
您最近一年使用:0次



