解题方法
1 . 游离态氮称为惰性氮,游离态氮转化为化合态氮称之为氮的活化,在氮的循环系统中,氮的过量“活化”会导致氮向大气和水体过量迁移,氮的循环平衡被打破,导致全球环境问题。
已知:SO2、CO、NH3等都可以催化还原氮氧化物生成惰性氮。
在25℃,101kPa时,
a.
b.
c.
(1)结合以上热化学方程式,写出NO与NH3反应生成惰性氮的热化学方程式_______ 。
(2)工业合成氨是氮的活化重要途径之一,在一定条件下,将N2和H2通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是_______(填字母)。
(3)在合成氨工业中,为提高化学反应速率并提高原料的平衡转化率可采取的措施为_____(填字母)。
(4)在有氧条件下,新型催化剂M能催化CO与 反应生成N2,该反应的方程式为
反应生成N2,该反应的方程式为 。
。
①现向某密闭容器中充入等物质的量浓度的 和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:
和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:
在0~5min内,以CO2的浓度变化表示的反应速率为_______ mol/(L·min),在10min时,CO的转化率为_______ 。此温度下,该反应的化学平衡常数K=_______ (保留两位有效数字)。
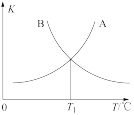
②该反应的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示正反应的平衡常数(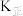 )的是
)的是_______ (填“A”或“B”),原因是_______ 。
已知:SO2、CO、NH3等都可以催化还原氮氧化物生成惰性氮。
在25℃,101kPa时,
a.

b.

c.

(1)结合以上热化学方程式,写出NO与NH3反应生成惰性氮的热化学方程式
(2)工业合成氨是氮的活化重要途径之一,在一定条件下,将N2和H2通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是_______(填字母)。
| A.容器中气体密度不变 | B. |
| C.容器中压强不变 | D.N2、H2、NH3分子数之比为1:3:2 |
| A.升高温度 | B.将氨液化从体系中分离 |
| C.加入催化剂 | D.增大压强 |
 反应生成N2,该反应的方程式为
反应生成N2,该反应的方程式为 。
。①现向某密闭容器中充入等物质的量浓度的
 和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:
和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:| 0min | 5min | 10min | 15min | 20min | |
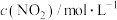 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
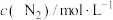 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
②该反应的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示正反应的平衡常数(
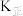 )的是
)的是
您最近一年使用:0次



