名校
解题方法
1 . 某校化学课外兴趣小组为了探究影响化学反应速率的因素,做了以下实验。
(1)用三支试管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分别滴入0.1 mol·L-1 H2C2O4溶液,实验报告如下。
①实验1、3研究的是_________ 对反应速率的影响。
②表中V=_________ mL。
(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为KMnO4与H2C2O4的反应放热,温度升高,速率加快。
②乙同学认为随着反应的进行,因_________ ,故速率加快。
(3)为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:
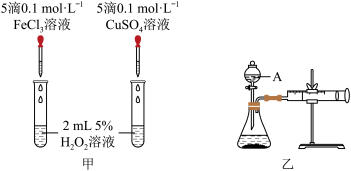
①装置乙中仪器A的名称为_________ 。
②定性分析:如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是____________________________________ 。
③定量分析:如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_______________ 。
(1)用三支试管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分别滴入0.1 mol·L-1 H2C2O4溶液,实验报告如下。
| 实验编号 |  KMnO4溶液 | 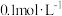 H2C2O4溶液 | 水 | 反应温度/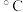 | 反应时间/s |
| 1 | 5.0mL | 5.0mL | 0 | 20 | 125 |
| 2 | 5.0mL | V | 1.0mL | 20 | 320 |
| 3 | 5.0mL | 5.0mL | 0 | 50 | 30 |
②表中V=
(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为KMnO4与H2C2O4的反应放热,温度升高,速率加快。
②乙同学认为随着反应的进行,因
(3)为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:

①装置乙中仪器A的名称为
②定性分析:如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是
③定量分析:如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是
您最近一年使用:0次
2020-04-01更新
|
878次组卷
|
3卷引用:江西省抚州市南城县第二中学2019-2020学年高一下学期开学考试(自强班)化学试题
名校
2 . 某研究性学习小组通过铁与盐酸反应的实验,研究影响反应速率的因素(铁的质量相等,铁块的形状一样,盐酸均过量),甲同学设计实验如下表:
请回答:
(1)若四组实验均以收集到500mL(已转化为标准状况下)氢气为标准,则上述实验中还需要测定的数据是________ 。
(2)实验________ 和______ 是研究铁的状态对该反应速率的影响(填实验编号,下同);实验______ 和______ 是研究温度对该反应速率的影响。
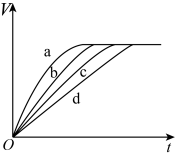
(3)测定在不同时间t产生氢气体积V的数据,根据数据绘制得到图,则曲线c、d分别对应的实验组别可能是_______ 、______ 。
(4)乙同学设计了下列一组实验:所用铁块的形状、质量均相同,所用酸的体积相同,其浓度如下,你认为产生氢气速率最快的是______ 。
A 18.4mol·L-1硫酸 B 5.0mol·L-1硝酸 C 3.0mol·L-1盐酸 D 2.0mol·L-1硫酸
| 实验编号 | 盐酸浓度(mol·L-1) | 铁的状态 | 温度/°C |
| 1 | 2.00 | 块状 | 20 |
| 2 | 2.00 | 粉末 | 20 |
| 3 | 1.00 | 块状 | 20 |
| 4 | 2.00 | 块状 | 40 |
(1)若四组实验均以收集到500mL(已转化为标准状况下)氢气为标准,则上述实验中还需要测定的数据是
(2)实验
(3)测定在不同时间t产生氢气体积V的数据,根据数据绘制得到图,则曲线c、d分别对应的实验组别可能是

(4)乙同学设计了下列一组实验:所用铁块的形状、质量均相同,所用酸的体积相同,其浓度如下,你认为产生氢气速率最快的是
A 18.4mol·L-1硫酸 B 5.0mol·L-1硝酸 C 3.0mol·L-1盐酸 D 2.0mol·L-1硫酸
您最近一年使用:0次
名校
3 . 下列装置或操作能达到目的的是


| A.装置①用于测定生成氢气的速率 |
| B.装置②依据褪色快慢比较浓度对反应速率的影响 |
| C.装置③依据U形管两边液面的高低判断Na和水反应的热效应 |
| D.装置④依据出现浑浊的快慢比较温度对反应速率的影响 |
您最近一年使用:0次
2018-11-05更新
|
1902次组卷
|
18卷引用:江西省乐平中学2022-2023学年高二上学期11月期中考试化学试题
江西省乐平中学2022-2023学年高二上学期11月期中考试化学试题【全国百强校】广东省佛山市第一中学2018-2019学年高二上学期第一次段考化学试题黑龙江省大庆实验中学2019-2020学年高二上学期第一次月考化学试题福建省永泰县第一中学2019-2020学年高二上学期期中考试化学试题(已下线)2019年12月20日 《每日一题》人教版(选修4)——外界条件对化学反应速率的影响广东省梅州中学2021届高三热身测试化学试题山东省烟台市莱州第一中学2021-2022学年高二上学期10月月考化学试题广东省佛山市第二中学2020-2021学年高二上学期期中考试化学试题吉林省抚松县第一中学2021-2022学年高二下学期开学考试化学试题广东省江门市第一中学2022-2023学年高二上学期第一次月考化学试题云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题云南省玉溪市江川区第二中学2021-2022学年高二下学期开学考试化学试题云南省蒙自市第一高级中学2022-2023学年高二下学期3月月考化学试题宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题河北省石家庄市第二十七中学2023-2024学年高二上学期第一次月考化学试题重庆市第一中学校2023-2024学年高二上学期第一次月考化学试题吉林省长春市第二实验中学2023-2024学年高二上学期期中考试化学试题黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期第一次质量检测化学试题
名校
4 . 用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4 -+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。某实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计方案如下(KMnO4溶液已酸化):
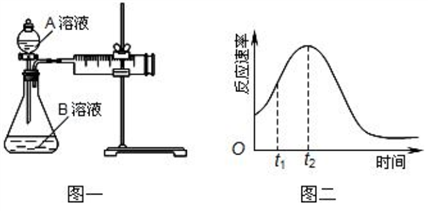
(1)该实验探究的是______ 对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_____ (填实验序号)。
(2)若实验①在2min末注射器的活塞向右移动到了b mL的位置,则这段时间的反应速率可表示为v(CO2)=______ mL/min。若实验②在t min收集了4.48×10-3L CO2(标准状况下),则t min末c(MnO4-)=______ 。
(3)该小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①___________ 、②___________ 。
(4)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2、K2=5.4×10-5,写出草酸的电离方程式_______ 、________ 。试从电离平衡移动的角度解释K1>>K2的原因_______________ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.lmol·L-l H2C2O4溶液 | 30mL 0.01mol.L-l KMnO4溶液 |
| ② | 20mL 0.2mol·L-l H2C2O4溶液 | 30mL 0.01mol.L-l KMnO4溶液 |

(1)该实验探究的是
(2)若实验①在2min末注射器的活塞向右移动到了b mL的位置,则这段时间的反应速率可表示为v(CO2)=
(3)该小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①
(4)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2、K2=5.4×10-5,写出草酸的电离方程式
您最近一年使用:0次
2017-10-22更新
|
523次组卷
|
2卷引用:江西省景德镇市昌江区景德镇一中2020-2021学年高二上学期期中考试化学试题(1班)



