1 . 采取高效经济方式利用 对人类社会发展具有重要意义。以
对人类社会发展具有重要意义。以 和
和 为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
Ⅰ.

Ⅱ.
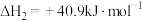
回答以下问题:
(1)已知:
 ,则反应Ⅰ的
,则反应Ⅰ的
___________  。
。
(2)有利于提高 平衡转化率的措施有___________(填标号)。
平衡转化率的措施有___________(填标号)。
(3)在催化剂作用下,测得 平衡转化率(曲线Y)和平衡时
平衡转化率(曲线Y)和平衡时 的选择性(曲线X)随温度变化如图所示。(已知:
的选择性(曲线X)随温度变化如图所示。(已知: 的选择性
的选择性 )
)

① 加氢制
加氢制 时,温度选择
时,温度选择 的原因为
的原因为___________ 。
②510K时,往恒容密闭容器中按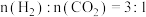 充入
充入 和
和 ,若平衡时容器内
,若平衡时容器内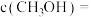
 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
___________ (列计算式即可)。
(4) 和
和 在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
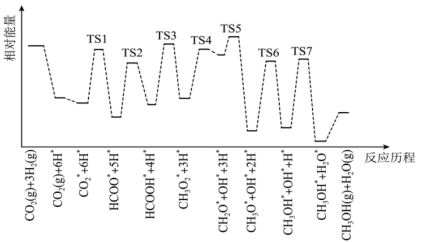
①气体在催化剂表面的吸附是___________ (填“吸热”或“放热”)过程。
②该反应历程中反应速率最快步骤的化学方程式为___________ 。
(5)甲醇催化制取丙烯( )的过程中发生如下反应:
)的过程中发生如下反应:
Ⅰ.
Ⅱ.
反应Ⅰ的Arrhenius经验公式的实验数据如图所示,已知Arrhenius经验公式为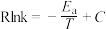 (
( 为活化能,
为活化能, 为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是
为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是___________ 。

 对人类社会发展具有重要意义。以
对人类社会发展具有重要意义。以 和
和 为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):Ⅰ.


Ⅱ.

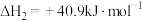
回答以下问题:
(1)已知:

 ,则反应Ⅰ的
,则反应Ⅰ的
 。
。(2)有利于提高
 平衡转化率的措施有___________(填标号)。
平衡转化率的措施有___________(填标号)。A.增大 投料比 投料比 | B.增大压强 |
| C.使用高效催化剂 | D.及时将 分离 分离 |
 平衡转化率(曲线Y)和平衡时
平衡转化率(曲线Y)和平衡时 的选择性(曲线X)随温度变化如图所示。(已知:
的选择性(曲线X)随温度变化如图所示。(已知: 的选择性
的选择性 )
)
①
 加氢制
加氢制 时,温度选择
时,温度选择 的原因为
的原因为②510K时,往恒容密闭容器中按
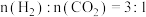 充入
充入 和
和 ,若平衡时容器内
,若平衡时容器内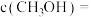
 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
(4)
 和
和 在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
①气体在催化剂表面的吸附是
②该反应历程中反应速率最快步骤的化学方程式为
(5)甲醇催化制取丙烯(
 )的过程中发生如下反应:
)的过程中发生如下反应:Ⅰ.

Ⅱ.

反应Ⅰ的Arrhenius经验公式的实验数据如图所示,已知Arrhenius经验公式为
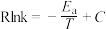 (
( 为活化能,
为活化能, 为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是
为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是
您最近一年使用:0次
名校
解题方法
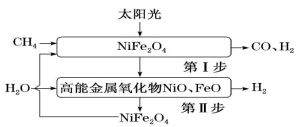
2 . 氢能是一种理想的绿色能源,一种太阳能两步法甲烷蒸气重整制氢原理合成示意图如下:
(1)第I步: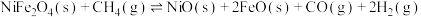
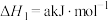 。总反应可表示为:
。总反应可表示为: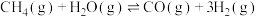
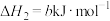 。写出第II步反应的热化学方程式:
。写出第II步反应的热化学方程式:___________ 。
(2)实验测得分步制氢比直接利用 和
和 反应具有更高的反应效率,原因是
反应具有更高的反应效率,原因是________ 。
(3)第I、II步反应的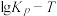 图像如下。
图像如下。
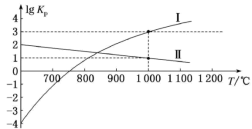
由图像可知a___________ b(填“大于”或“小于”), 时第I步反应平衡时
时第I步反应平衡时 的平衡分压
的平衡分压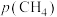
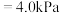 ,则平衡混合气体中
,则平衡混合气体中 的体积分数为
的体积分数为___________ (保留一位小数)。
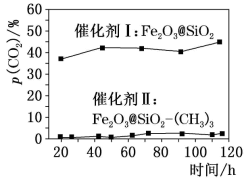
(4)第I步反应产生的合成气(CO和 的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应:
的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应: ,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内
,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内 的分数,据此应选择的催化剂是
的分数,据此应选择的催化剂是___________ (填“I”或“II”),选择的依据是___________ 。

(1)第I步:
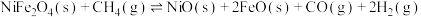
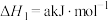 。总反应可表示为:
。总反应可表示为: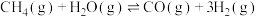
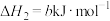 。写出第II步反应的热化学方程式:
。写出第II步反应的热化学方程式:(2)实验测得分步制氢比直接利用
 和
和 反应具有更高的反应效率,原因是
反应具有更高的反应效率,原因是(3)第I、II步反应的
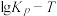 图像如下。
图像如下。
由图像可知a
 时第I步反应平衡时
时第I步反应平衡时 的平衡分压
的平衡分压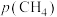
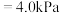 ,则平衡混合气体中
,则平衡混合气体中 的体积分数为
的体积分数为(4)第I步反应产生的合成气(CO和
 的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应:
的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应: ,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内
,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内 的分数,据此应选择的催化剂是
的分数,据此应选择的催化剂是
您最近一年使用:0次
名校
解题方法
3 . (1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
其他条件不变时:探究温度对化学反应速率的影响,应选择实验_______ (填实验编号); 若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为_______ 和_______ 。
(2)研究表明,SO2催化氧化的反应速率方程为:v = k(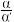 −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
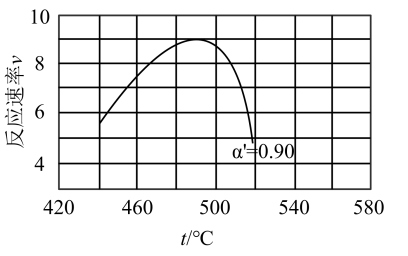
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。下列说法正确的是_______
A.v达到最大值时,SO2平衡转化率α最大
B.t < tm时,v逐渐提高,原因是升高温度,k逐渐增大
C.t > tm后,v逐渐下降,原因是升高温度,α逐渐降低
D.温度是影响反应速率的主要因素,温度越高,反应速率越快
(3)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示:
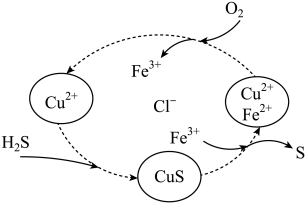
图2
①该循环过程中 Fe3+起的作用是:________ 写出该该反应的化学方程式_______
| 实验 编号 | 实验温 度/℃ | c(Na2S2O3) /(mol·L-1) | V(Na2S2O3) /mL | c(H2SO4) /(mol·L-1) | V(H2SO4) /mL | V(H2O) /mL |
| ① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
| ② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
| ③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
| ④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
(2)研究表明,SO2催化氧化的反应速率方程为:v = k(
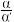 −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v ~ t曲线,如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。下列说法正确的是
A.v达到最大值时,SO2平衡转化率α最大
B.t < tm时,v逐渐提高,原因是升高温度,k逐渐增大
C.t > tm后,v逐渐下降,原因是升高温度,α逐渐降低
D.温度是影响反应速率的主要因素,温度越高,反应速率越快
(3)将H2S 和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示:

图2
①该循环过程中 Fe3+起的作用是:
您最近一年使用:0次



