名校
1 . 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述不正确的是

| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图甲所示实验中反应速率:①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 |
| C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查图乙所示装置的气密性,可关闭A处旋塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近半年使用:0次
2024-04-05更新
|
948次组卷
|
4卷引用:福建省福州格致中学2023-2024学年高一下学期3月月考化学试卷
解题方法
2 . 利用反应2NO(g)+2CO(g) 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
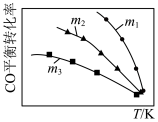
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.若m=2,反应达平衡时,NO的转化率为40%,则N2的体积分数为15.4% |
B.该反应的 |
C.投料比: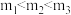 |
| D.汽车排气管中的催化剂可提高NO的平衡转化率 |
您最近半年使用:0次
解题方法
3 .  干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法
干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法错误 的是

 干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法
干法重整中镍基催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少,其中涉及的相关数据如表。催化剂表面发生的不同积碳反应在不同温度下的质量增量如图。下列说法
基元反应 |
|
| ||
|
|
|
| |
积碳: | 65.5 | 136.8 | 103.1 | 109.8 |
消碳: | 139.7 | 326.6 | 117.5 | 51.0 |
吸附在催化剂表面上的物种用*标注 | ||||
| A.一氧化碳歧化反应是放热反应 |
| B.甲烷裂解是镍基催化剂表面积碳的主要来源 |
C. 的焓变为 的焓变为 |
D.由上表判断,催化剂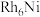 劣于 劣于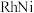 |
您最近半年使用:0次
名校
4 . 下列关于反应热的说法正确的是
| A.使用催化剂只改变可逆反应中正反应的活化能 |
| B.反应物的总键能小于生成物的总键能,则反应为吸热反应 |
C.已知红磷比白磷更稳定,  |
D.  ,则 ,则 燃烧热为 燃烧热为 |
您最近半年使用:0次
5 . 氮氧化物会导致光化学烟雾和酸雨,在 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是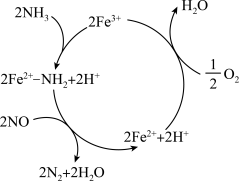
A.基态 的价层电子排布式为 的价层电子排布式为 |
| B.电负性:N>O>H>Fe |
| C.该过程中存在极性键和非极性键的断裂和形成 |
D.图中的总反应可表示为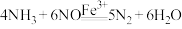 |
您最近半年使用:0次
2024-02-25更新
|
258次组卷
|
5卷引用:福建省福州第三中学2023-2024学年高三上学期第五次质量检测化学试题
名校
6 . 铜-铈氧化物(xCuO·yCeO2)可除去H2中少量CO,反应机理如图。Ce是一种活泼金属,价电子为4f15d16s2,步骤(ⅰ)中Cu、Ce的化合价均发生变化。


| A.反应ⅰ中,Cu元素的化合价从+2变成+1 |
| B.反应ⅰ中,Ce元素的化合价从+4变成+2 |
| C.当温度超过150℃时,CO转化率明显下降,可能是因为催化剂的催化活性下降 |
| D.温度过高,催化剂中Cu2+(或Cu+)可能被H2(或CO)还原为Cu造成催化活性下降 |
您最近半年使用:0次
2024-02-24更新
|
232次组卷
|
2卷引用:福建省福建师范大学附属中学2023-2024学年高三下学期综合测试三(4月月考)化学试题
名校
7 . 某合成氨速率方程为: (k为速率常数),部分数据如下表。下列说法正确的是
(k为速率常数),部分数据如下表。下列说法正确的是
 (k为速率常数),部分数据如下表。下列说法正确的是
(k为速率常数),部分数据如下表。下列说法正确的是| 实验 |  | 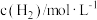 | 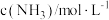 |  |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
| A.α=1,γ=-1 |
| B.采用适当催化剂,反应活化能、焓变均减小 |
| C.恒容容器中反应时,充He气,压强增大反应速率加快 |
| D.k与物质性质有关,与反应温度、压强、反应物浓度无关 |
您最近半年使用:0次
名校
解题方法
8 . 用硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO 转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表。
表中a、b的值分别为:a=___________ 、b=___________
(2)该反应的离子方程式为___________ 。
(3)若t1<t2,则根据实验①和②得到的结论是___________ 。
(4)某小组同学按实验①进行实验,测得溶液褪色时间t1=2.5min,求该条件下的化学反应速率v(H2C2O4)=___________ ,其反应速率变化如图,其中x1~x2时间内速率变快的主要原因可能是:产物Mn2+是反应的催化剂、___________ 。

(5)请你设计实验④验证MnSO4对该反应起催化作用,完成下表中内容。
 转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表。
| 实验编号 | 温度 | 初始pH | 0.1mol/L草酸溶液/mL | 0.01mol/LKMnO4溶的体积/mL | 蒸馏水体积/mL | 待测数据(反应混合液褪色时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | a | b | t3 |
(2)该反应的离子方程式为
(3)若t1<t2,则根据实验①和②得到的结论是
(4)某小组同学按实验①进行实验,测得溶液褪色时间t1=2.5min,求该条件下的化学反应速率v(H2C2O4)=

(5)请你设计实验④验证MnSO4对该反应起催化作用,完成下表中内容。
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
| 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
您最近半年使用:0次
9 . 采取高效经济方式利用 对人类社会发展具有重要意义。以
对人类社会发展具有重要意义。以 和
和 为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
Ⅰ.

Ⅱ.
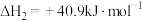
回答以下问题:
(1)已知:
 ,则反应Ⅰ的
,则反应Ⅰ的
___________  。
。
(2)有利于提高 平衡转化率的措施有___________(填标号)。
平衡转化率的措施有___________(填标号)。
(3)在催化剂作用下,测得 平衡转化率(曲线Y)和平衡时
平衡转化率(曲线Y)和平衡时 的选择性(曲线X)随温度变化如图所示。(已知:
的选择性(曲线X)随温度变化如图所示。(已知: 的选择性
的选择性 )
)

① 加氢制
加氢制 时,温度选择
时,温度选择 的原因为
的原因为___________ 。
②510K时,往恒容密闭容器中按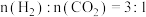 充入
充入 和
和 ,若平衡时容器内
,若平衡时容器内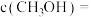
 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
___________ (列计算式即可)。
(4) 和
和 在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
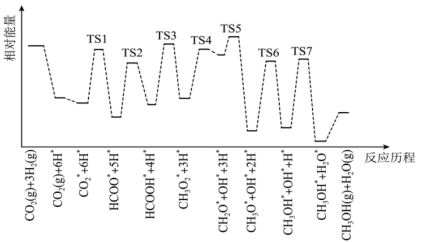
①气体在催化剂表面的吸附是___________ (填“吸热”或“放热”)过程。
②该反应历程中反应速率最快步骤的化学方程式为___________ 。
(5)甲醇催化制取丙烯( )的过程中发生如下反应:
)的过程中发生如下反应:
Ⅰ.
Ⅱ.
反应Ⅰ的Arrhenius经验公式的实验数据如图所示,已知Arrhenius经验公式为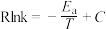 (
( 为活化能,
为活化能, 为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是
为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是___________ 。

 对人类社会发展具有重要意义。以
对人类社会发展具有重要意义。以 和
和 为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
为原料合成甲醇主要发生反应Ⅰ和反应Ⅱ(不考虑其他反应):Ⅰ.


Ⅱ.

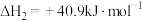
回答以下问题:
(1)已知:

 ,则反应Ⅰ的
,则反应Ⅰ的
 。
。(2)有利于提高
 平衡转化率的措施有___________(填标号)。
平衡转化率的措施有___________(填标号)。A.增大 投料比 投料比 | B.增大压强 |
| C.使用高效催化剂 | D.及时将 分离 分离 |
 平衡转化率(曲线Y)和平衡时
平衡转化率(曲线Y)和平衡时 的选择性(曲线X)随温度变化如图所示。(已知:
的选择性(曲线X)随温度变化如图所示。(已知: 的选择性
的选择性 )
)
①
 加氢制
加氢制 时,温度选择
时,温度选择 的原因为
的原因为②510K时,往恒容密闭容器中按
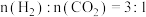 充入
充入 和
和 ,若平衡时容器内
,若平衡时容器内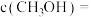
 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
(4)
 和
和 在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注,“TS”表示过渡状态。
①气体在催化剂表面的吸附是
②该反应历程中反应速率最快步骤的化学方程式为
(5)甲醇催化制取丙烯(
 )的过程中发生如下反应:
)的过程中发生如下反应:Ⅰ.

Ⅱ.

反应Ⅰ的Arrhenius经验公式的实验数据如图所示,已知Arrhenius经验公式为
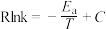 (
( 为活化能,
为活化能, 为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是
为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改变的外界条件是
您最近半年使用:0次
10 . 下列装置及设计不能达到实验目的的是


| A.测定中和反应的反应热 |
| B.验证Fe3+与I-反应是可逆反应 |
| C.探究温度对化学平衡的影响 |
| D.比较Fe3+和Cu2+对H2O2分解反应的催化效果 |
您最近半年使用:0次







