名校
1 . 为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验。请回答下列问题:
(1)实验①的目的是___ 。
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是____ (用实验中所提供的几种试剂)。
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图所示的实验。请回答相关问题:
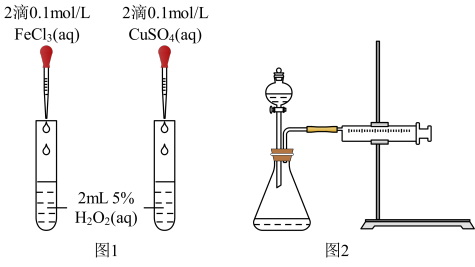
①定性分析:如图1可通过观察____ ,定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是___ 。
②定量分析:用图2所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是___ 。
(4)MnO2对H2O2分解反应也有催化作用,另一个同学用图2装置,将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如下:
①实验结果表明,催化剂的催化效果与___ 有关。
②实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因___ 。
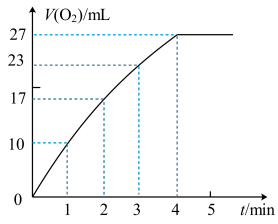
| 编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入3滴FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡;试管B中产生的气泡量增多 |
| ② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2溶液 | 两支试管中均未明显见到有气泡产生 |
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图所示的实验。请回答相关问题:

①定性分析:如图1可通过观察
②定量分析:用图2所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(4)MnO2对H2O2分解反应也有催化作用,另一个同学用图2装置,将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如下:
| MnO2状态 | 触摸锥形瓶情况 | 该温度下针筒内收集到气体的体积 | 所需时间 |
| 粉末状 | 很烫 | 30mL | 3min |
| 块状 | 微热 | 30mL | 9min |
②实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因
您最近一年使用:0次
名校
2 . 利用如图实验装置进行相应实验,能达到实验目的的是
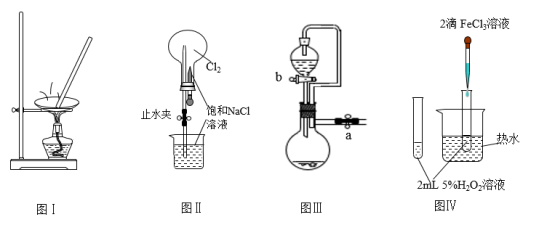

| A.利用图Ⅰ装置蒸发KCl溶液制备无水KCl |
| B.利用图Ⅱ装置进行喷泉实验 |
| C.图Ⅲ装置中,关闭a、打开b,可检查装置的气密性 |
D.利用图Ⅳ装置验证 分解反应有催化作用 分解反应有催化作用 |
您最近一年使用:0次
2021-10-11更新
|
377次组卷
|
5卷引用:福建省莆田市第二中学2022届高三10月月考化学试题
福建省莆田市第二中学2022届高三10月月考化学试题福建省泉州市城东中学2021-2022学年高三上学期10月月考化学试题福建省福州市六校联考2022-2023学年高一下学期期末考试化学试题四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)
3 . 用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是
| A | B | C | D |
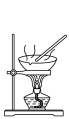 | 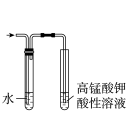 | 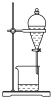 | 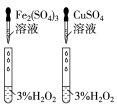 |
蒸发结晶制备 晶体 晶体 | 检验溴乙烷消去产物 | 分离苯和溴苯 | 探究不同催化剂 对  分解速率的影响 分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-18更新
|
657次组卷
|
6卷引用:福建省漳州市七校(厦大附中、龙海一中、南靖一中、平和一中、诏安一中、长泰一中、龙海二中)2021-2022学年高三下学期毕业班4月诊断性联考化学试题
名校
4 . 过氧化钙是一种温和的氧化剂,常温下为白色的固体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。某实验小组拟选用如下操作与装置(部分固定装置略)制备过氯化钙。
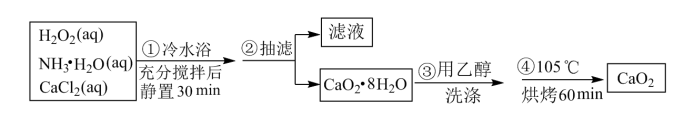

(1)三颈烧瓶中发生的主要反应的化学方程式为_______ 。
(2)用恒压分液漏斗盛装H2O2和浓氨水相比用普通分液漏斗盛装的好处是_______ 。
(3)该反应常用冰水浴控制温度在0°C左右,其可能的原因分析:其一,该反应是放热反应,温度低有利于提高CaO2·8H2O的产率;其二,_______ ;
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O。检验CaO2·8H2O是否洗涤干净的试剂为_______ 。
(5)过氧化钙产品纯度测定实验步骤如下:
第一步:准确称取ag产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的(NH4)2C2O4,沉淀完全,过滤并洗涤沉淀;
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴MnSO4溶液,然后逐滴滴入浓度为cmol·L-1的KMnO4溶液至终点,消耗KMnO4溶液VmL。
①滴定前,滴入MnSO4溶液的目的是_______ 。
②滴定终点的现象为_______ 。
③产品的纯度为_______ (用字母表示)。
④若第三步用稀盐酸溶解,所测纯度_______ (填“偏低”“不变”或“偏高”)


(1)三颈烧瓶中发生的主要反应的化学方程式为
(2)用恒压分液漏斗盛装H2O2和浓氨水相比用普通分液漏斗盛装的好处是
(3)该反应常用冰水浴控制温度在0°C左右,其可能的原因分析:其一,该反应是放热反应,温度低有利于提高CaO2·8H2O的产率;其二,
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O。检验CaO2·8H2O是否洗涤干净的试剂为
(5)过氧化钙产品纯度测定实验步骤如下:
第一步:准确称取ag产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的(NH4)2C2O4,沉淀完全,过滤并洗涤沉淀;
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴MnSO4溶液,然后逐滴滴入浓度为cmol·L-1的KMnO4溶液至终点,消耗KMnO4溶液VmL。
①滴定前,滴入MnSO4溶液的目的是
②滴定终点的现象为
③产品的纯度为
④若第三步用稀盐酸溶解,所测纯度
您最近一年使用:0次
5 . 下列装置及设计不能达到实验目的的是


| A.测定中和反应的反应热 |
| B.验证Fe3+与I-反应是可逆反应 |
| C.探究温度对化学平衡的影响 |
| D.比较Fe3+和Cu2+对H2O2分解反应的催化效果 |
您最近一年使用:0次
名校
6 . “化学多米诺实验“即只需控制第一个反应,利用反应中气体产生的压力和虹吸作用原理使若干化学实验依次发生。如图是一个“化学多米诺实验”。
已知:①Cu2++4NH3·H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2分解的催化剂)
②A和C中的硫酸溶液浓度相同
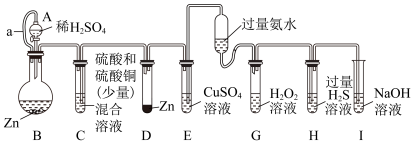
下列有关分析错误的是
已知:①Cu2++4NH3·H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2分解的催化剂)
②A和C中的硫酸溶液浓度相同

下列有关分析错误的是
| A.B装置中反应速率大于D装置中反应速率 |
| B.E装置中现象为试管内蓝色液面下降 |
| C.H装置中出现浅黄色浑浊 |
| D.该实验成功的重要条件是整套装置气密性良好 |
您最近一年使用:0次
2023-09-02更新
|
182次组卷
|
2卷引用:福建省政和县第一中学2023-2024学年高三上学期第一次月考化学试题
解题方法
7 . 铜和稀硝酸在无氧环境下会生成弱酸 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。

实验过程现象记录如下表。
(1)仪器a的名称为_______ 。
(2)滴入硝酸前,为营造无氧环境,应进行的操作是_______ 。
(3)反应过程中产生的 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为_______ 。
(4)溶液呈绿色是 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
根据以上实验现象可知, 和
和_______ (填化学式)相互作用达到平衡呈绿色。
(5)取适量150 min时反应液于试管中,加入_______ ,溶液由蓝色变为绿色,,说明150 min时反应液中含有 。
。
(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因_______ 。
(7)基于上述装置,选择合适试剂,设计实验证明 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用_______ (简述实验方案及观测指标)。
 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
实验过程现象记录如下表。
| 时间/min | 0~75 | 75~150 | 150~225 | 225~300 | 300~375 |
| 溶液颜色 | 接近无色 | 无色→浅蓝色 | 浅蓝色→绿色 | 绿色→深蓝色 | 浅蓝色 |
| 生成NO体积/mL | 0 | 1.0 | 42.0 | 137.5 | 0.5 |
| 反应体系温度/℃ | 26.6 | 26.8 | 26.8~27.2 | 27.2~28.8 | 28.8~28.6 |
(2)滴入硝酸前,为营造无氧环境,应进行的操作是
(3)反应过程中产生的
 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为(4)溶液呈绿色是
 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:| 序号 | 实验操作 | 现象 |
| a | 往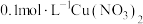 溶液中通入NO 溶液中通入NO | 溶液始终为蓝色 |
| b | 往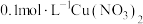 溶液中加入 溶液中加入 | 溶液变为绿色 |
| c | 往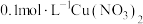 溶液中加入 溶液中加入 后逐滴加入 后逐滴加入 硝酸 硝酸 | 溶液先变为绿色后逐渐变为蓝色 |
 和
和(5)取适量150 min时反应液于试管中,加入
 。
。(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因
(7)基于上述装置,选择合适试剂,设计实验证明
 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用
您最近一年使用:0次



