下列装置及设计不能达到实验目的的是


| A.测定中和反应的反应热 |
| B.验证Fe3+与I-反应是可逆反应 |
| C.探究温度对化学平衡的影响 |
| D.比较Fe3+和Cu2+对H2O2分解反应的催化效果 |
更新时间:2024-01-28 20:46:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.在稀溶液中,1molH2SO4(aq)与1molBa(OH)2(aq)完全反应所放出的热量为中和热 |
| B.等质量的硫粉和硫蒸气分别完全燃烧,后者放出的热量更多 |
| C.乙炔(C2H2)的燃烧热为1299.6kJ•mol-1,则2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)的△H=-2599.2kJ•mol-1 |
| D.中和热测定实验中,可分多次把NaOH溶液倒入盛有稀盐酸的小烧杯中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于热化学反应的描述正确的是( )
| A.中和热测定时,用铜丝代替玻璃棒搅拌,会使中和热测定的数值偏大 |
| B.1mol甲烷燃烧生成水和二氧化碳所放出的热量是甲烷的燃烧热 |
| C.CO(g)的燃烧热△H=-283.0kJ/mol,则 2CO2(g)=2CO(g)+O2(g)△H=+566.0kJ/mol |
| D.HCl和NaOH反应的中和热-57.3kJ/mol,则H2SO4和NaOH反应的反应热△H=-114.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某同学用50mL 0.50 mol∙L-1的盐酸与50mL0.55 mol∙L-1的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算反应热。下列说法不正确 的是
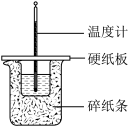

| A.采用0.55 mol∙L-1的NaOH溶液是保证盐酸完全被中和 |
| B.图中实验装置缺少玻璃搅拌器,玻璃搅拌器搅拌时上下移动搅拌 |
| C.测量反应混合液的温度时要随时读取温度,记录下最高温度 |
| D.若烧杯上不盖硬纸板,测得的反应放出的热量数据偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知SO2+4I-+4H+=S↓+2I2+2H2O,现进行如下图所示实验。下列说法错误的是


| A.改变c(H+)对反应速率没有影响 |
| B.该反应能够证明SO2既有氧化性,又有还原性 |
| C.整个反应过程中,KI可能起到了催化剂的作用 |
D.该过程中SO2发生的总反应可能为3SO2+2H2O=2SO +S↓+4H+ +S↓+4H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
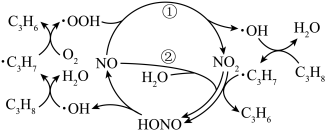
【推荐2】“接触法制硫酸”的主要反应是2SO2+O2 2SO3在催化剂表面的反应历程如下:
2SO3在催化剂表面的反应历程如下:
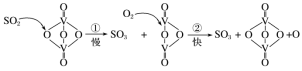
下列说法正确的是
 2SO3在催化剂表面的反应历程如下:
2SO3在催化剂表面的反应历程如下:
下列说法正确的是
| A.过程中既有V—O键的断裂,又有V—O键的形成 |
| B.反应②的活化能比反应①大 |
| C.该反应的催化剂是V2O4 |
| D.使用催化剂只能加快正反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中进行反应:X2(g)+3Y2(g) 2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
 2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。| A.c(Z)=0.5 mol·L-1 | B.c(Y2)=0.5 mol·L-1 |
| C.c(X2)=0.2 mol·L-1 | D.c(Y2)=0.6 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知X(g)+3Y (g) 2W(g)+M (g) △H=-a kJ·mol-1(a>0)一定温度下,在体积恒定的密闭容器中,加入1 mol X(g)与3mol Y (g),下列说法正确的是( )
2W(g)+M (g) △H=-a kJ·mol-1(a>0)一定温度下,在体积恒定的密闭容器中,加入1 mol X(g)与3mol Y (g),下列说法正确的是( )
 2W(g)+M (g) △H=-a kJ·mol-1(a>0)一定温度下,在体积恒定的密闭容器中,加入1 mol X(g)与3mol Y (g),下列说法正确的是( )
2W(g)+M (g) △H=-a kJ·mol-1(a>0)一定温度下,在体积恒定的密闭容器中,加入1 mol X(g)与3mol Y (g),下列说法正确的是( )| A.充分反应后,放出热量为a kJ |
| B.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2 |
| C.若增大Y的浓度,正反应速率增大,逆反应速率减小 |
| D.当X的物质的量分数不再改变,表明该反应已达平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于可逆反应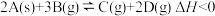 ,在一定条件下达到平衡状态,下列有关叙述正确的是( )
,在一定条件下达到平衡状态,下列有关叙述正确的是( )
①增大物质A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动, 减小
减小
③压强增大一倍,平衡不移动, 、
、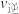 不变
不变
④增大物质B的浓度,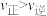
⑤加入催化剂,物质B的转化率提高
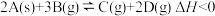 ,在一定条件下达到平衡状态,下列有关叙述正确的是( )
,在一定条件下达到平衡状态,下列有关叙述正确的是( )①增大物质A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,
 减小
减小③压强增大一倍,平衡不移动,
 、
、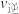 不变
不变④增大物质B的浓度,
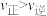
⑤加入催化剂,物质B的转化率提高
| A.①②⑤ | B.④ | C.②③④ | D.④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向某密闭容器中加入2molC(s)和1mol (g),在催化剂存在下发生反应:
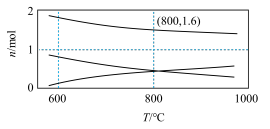
(g),在催化剂存在下发生反应: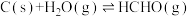 。不同温度下,平衡时各组分的物质的量如图所示。下列说法正确的是
。不同温度下,平衡时各组分的物质的量如图所示。下列说法正确的是
 (g),在催化剂存在下发生反应:
(g),在催化剂存在下发生反应: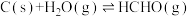 。不同温度下,平衡时各组分的物质的量如图所示。下列说法正确的是
。不同温度下,平衡时各组分的物质的量如图所示。下列说法正确的是
A.该反应的 |
B.600℃达到平衡时,若增大容器的体积,则平衡不移动, (g)的浓度不变 (g)的浓度不变 |
C.700℃时,若恒容条件下向平衡体系中充入惰性气体,则平衡不移动, (g)的浓度不变 (g)的浓度不变 |
| D.800℃时,该反应的平衡常数K=1.5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
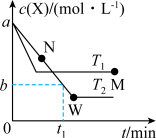
【推荐3】在恒容密闭容器中通入X并发生反应: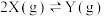 ,温度下T1、T2下X的物质的量浓度
,温度下T1、T2下X的物质的量浓度 随时间t变化的曲线如图所示。下列叙述不正确的是
随时间t变化的曲线如图所示。下列叙述不正确的是
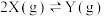 ,温度下T1、T2下X的物质的量浓度
,温度下T1、T2下X的物质的量浓度 随时间t变化的曲线如图所示。下列叙述不正确的是
随时间t变化的曲线如图所示。下列叙述不正确的是
A.T1>T2, |
| B.M点时再加入一定量X,平衡后X的体积分数减小 |
C.M点的正反速率 大于N点的逆反应速率 大于N点的逆反应速率 |
D.T2下,在0~t1时间内,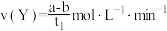 |
您最近一年使用:0次

 的平衡转化率增大
的平衡转化率增大
 的
的 溶液和0.05
溶液和0.05 溶液等体积混合充分反应后,取混合液分别完成下列实验,能说明溶液中存在化学平衡
溶液等体积混合充分反应后,取混合液分别完成下列实验,能说明溶液中存在化学平衡 的是
的是 溶液
溶液 溶液
溶液 溶液
溶液

