名校
1 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理]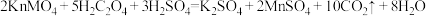
[实验内容及记录]
(1)请完成此实验设计,其中:
_______ ,
_______ 。
(2)实验①、②探究的是_______ 对化学反应速率的影响,根据表中的实验数据,可以得到的结论是_______ 。
(3)探究温度对化学反应速率的影响,应选择_______ (填实验编号)。
(4)该小组同学根据经验绘制了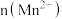 随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中
随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中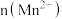 随时间变化的实际趋势如图乙所示。
随时间变化的实际趋势如图乙所示。

该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
①该小组同学提出的假设是_______ 。
②能佐证该假设成立的实验证据是_______ 。
[实验原理]
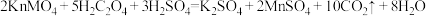
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | |||
| ① | 25 | 3.0 |  | 2.0 | 3.0 | 1.5 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| ③ | 50 | 2.0 |  | 2.0 | 3.0 | 1.7 |
(1)请完成此实验设计,其中:


(2)实验①、②探究的是
(3)探究温度对化学反应速率的影响,应选择
(4)该小组同学根据经验绘制了
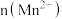 随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中
随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中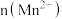 随时间变化的实际趋势如图乙所示。
随时间变化的实际趋势如图乙所示。
该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | ||||
| ④ | 25 | 2.0 | 3.0 | 2.0 | 3.0 |  | t |
②能佐证该假设成立的实验证据是
您最近一年使用:0次
名校
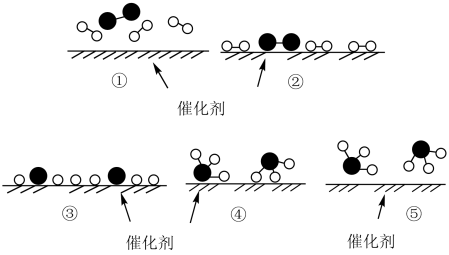
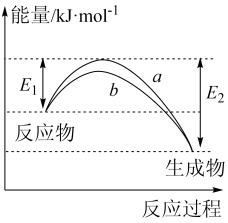
2 . 德国化学家 F.Haber 利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用 、
、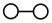 、
、 分别表示N2、H2、NH3,下列说法不正确的是
分别表示N2、H2、NH3,下列说法不正确的是
 、
、 、
、 分别表示N2、H2、NH3,下列说法不正确的是
分别表示N2、H2、NH3,下列说法不正确的是

| A.过程②为反应物吸附在催化剂表面,没有发生化学变化 |
| B.合成氨反应中,反应物断键吸收的总能量大于生成物形成新键所释放的总能量 |
| C.过程④为放热过程 |
| D.使用催化剂,能加快合成氨反应的速率 |
您最近一年使用:0次
解题方法
3 . 铜和稀硝酸在无氧环境下会生成弱酸 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。

实验过程现象记录如下表。
(1)仪器a的名称为_______ 。
(2)滴入硝酸前,为营造无氧环境,应进行的操作是_______ 。
(3)反应过程中产生的 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为_______ 。
(4)溶液呈绿色是 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
根据以上实验现象可知, 和
和_______ (填化学式)相互作用达到平衡呈绿色。
(5)取适量150 min时反应液于试管中,加入_______ ,溶液由蓝色变为绿色,,说明150 min时反应液中含有 。
。
(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因_______ 。
(7)基于上述装置,选择合适试剂,设计实验证明 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用_______ (简述实验方案及观测指标)。
 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
实验过程现象记录如下表。
| 时间/min | 0~75 | 75~150 | 150~225 | 225~300 | 300~375 |
| 溶液颜色 | 接近无色 | 无色→浅蓝色 | 浅蓝色→绿色 | 绿色→深蓝色 | 浅蓝色 |
| 生成NO体积/mL | 0 | 1.0 | 42.0 | 137.5 | 0.5 |
| 反应体系温度/℃ | 26.6 | 26.8 | 26.8~27.2 | 27.2~28.8 | 28.8~28.6 |
(2)滴入硝酸前,为营造无氧环境,应进行的操作是
(3)反应过程中产生的
 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为(4)溶液呈绿色是
 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:| 序号 | 实验操作 | 现象 |
| a | 往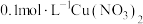 溶液中通入NO 溶液中通入NO | 溶液始终为蓝色 |
| b | 往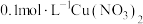 溶液中加入 溶液中加入 | 溶液变为绿色 |
| c | 往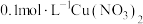 溶液中加入 溶液中加入 后逐滴加入 后逐滴加入 硝酸 硝酸 | 溶液先变为绿色后逐渐变为蓝色 |
 和
和(5)取适量150 min时反应液于试管中,加入
 。
。(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因
(7)基于上述装置,选择合适试剂,设计实验证明
 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用
您最近一年使用:0次
解题方法
4 . 我国科学家采用磷化硼(BP)纳米颗粒成功地实现了高选择性电工化还原CO2制CH3OH,CO2在阴极催化剂表面的变化及反应历程如图所示:
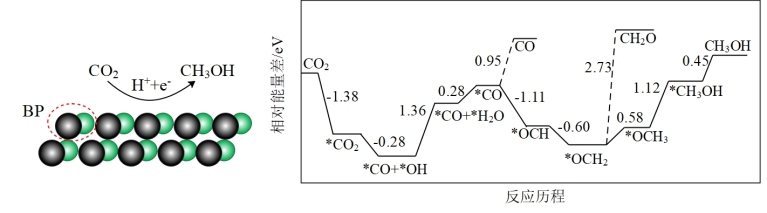
下列说法正确的是( )

下列说法正确的是( )
| A.制备CH3OH过程中得到相对较多的副产物是CH2O |
| B.在催化剂上生成CH3OH的电极反应式为CO2+6H++6e-=CH3OH+H2O |
| C.在催化剂上生成CH3OH的过程中有极性键和非极性键的断裂和生成 |
| D.*CO+*OH=*CO+*H2O为放热过程 |
您最近一年使用:0次
名校
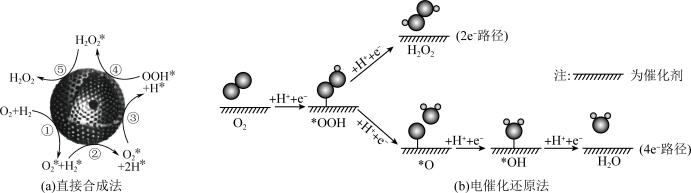
5 . 以Pd纳米粒子为核、空心多孔碳球为壳的封装型催化剂将H2和O2直接合成 的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
 的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
| A.直接合成法中,步骤②吸收能量,步骤④释放能量 |
| B.电催化还原法制备H2O2的优点之一是避免了H2和O2共存的易爆环境 |
| C.电催化还原时,2e-路径的步骤少,反应速率快 |
D.若催化剂表面对*OOH吸附过强,则易生成O*,导致 的产率降低 的产率降低 |
您最近一年使用:0次
2022-05-05更新
|
623次组卷
|
6卷引用:福建省连城县第一中学2022-2023学年高二上学期第一次月考化学试题
福建省连城县第一中学2022-2023学年高二上学期第一次月考化学试题福建省三明市2022届普通高中毕业班下学期5月质量测试化学试题重庆市缙云教育联盟2021-2022学年高一6月质量检测化学试题湖南省岳阳市一中2021-2022学年高三下学期第三次模拟考试试题(已下线)专题07 化学反应中的能量变化-2022年高考真题模拟题分项汇编(已下线)微专题36 高考“明星”考点—催化剂-备战2023年高考化学一轮复习考点微专题
名校
6 . 过氧化钙是一种温和的氧化剂,常温下为白色的固体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。某实验小组拟选用如下操作与装置(部分固定装置略)制备过氯化钙。
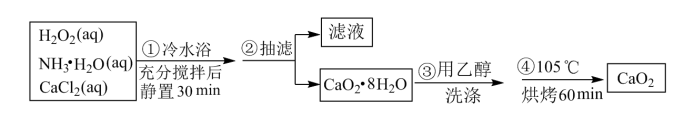

(1)三颈烧瓶中发生的主要反应的化学方程式为_______ 。
(2)用恒压分液漏斗盛装H2O2和浓氨水相比用普通分液漏斗盛装的好处是_______ 。
(3)该反应常用冰水浴控制温度在0°C左右,其可能的原因分析:其一,该反应是放热反应,温度低有利于提高CaO2·8H2O的产率;其二,_______ ;
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O。检验CaO2·8H2O是否洗涤干净的试剂为_______ 。
(5)过氧化钙产品纯度测定实验步骤如下:
第一步:准确称取ag产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的(NH4)2C2O4,沉淀完全,过滤并洗涤沉淀;
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴MnSO4溶液,然后逐滴滴入浓度为cmol·L-1的KMnO4溶液至终点,消耗KMnO4溶液VmL。
①滴定前,滴入MnSO4溶液的目的是_______ 。
②滴定终点的现象为_______ 。
③产品的纯度为_______ (用字母表示)。
④若第三步用稀盐酸溶解,所测纯度_______ (填“偏低”“不变”或“偏高”)


(1)三颈烧瓶中发生的主要反应的化学方程式为
(2)用恒压分液漏斗盛装H2O2和浓氨水相比用普通分液漏斗盛装的好处是
(3)该反应常用冰水浴控制温度在0°C左右,其可能的原因分析:其一,该反应是放热反应,温度低有利于提高CaO2·8H2O的产率;其二,
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O。检验CaO2·8H2O是否洗涤干净的试剂为
(5)过氧化钙产品纯度测定实验步骤如下:
第一步:准确称取ag产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的(NH4)2C2O4,沉淀完全,过滤并洗涤沉淀;
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴MnSO4溶液,然后逐滴滴入浓度为cmol·L-1的KMnO4溶液至终点,消耗KMnO4溶液VmL。
①滴定前,滴入MnSO4溶液的目的是
②滴定终点的现象为
③产品的纯度为
④若第三步用稀盐酸溶解,所测纯度
您最近一年使用:0次
名校
7 . 已知反应2NO(g)+2H2(g) N2(g)+2H2O(g)△H=-752kJ·mol-1的反应机理如下:
N2(g)+2H2O(g)△H=-752kJ·mol-1的反应机理如下:
①2NO(g) N2O2(g)(快)
N2O2(g)(快)
②N2O2(g)+H2(g) N2O(g)+H2O(g)(慢)
N2O(g)+H2O(g)(慢)
③N2O(g)+H2(g) N2(g)+H2O(g)(快)
N2(g)+H2O(g)(快)
下列有关说法错误的是
 N2(g)+2H2O(g)△H=-752kJ·mol-1的反应机理如下:
N2(g)+2H2O(g)△H=-752kJ·mol-1的反应机理如下:①2NO(g)
 N2O2(g)(快)
N2O2(g)(快)②N2O2(g)+H2(g)
 N2O(g)+H2O(g)(慢)
N2O(g)+H2O(g)(慢)③N2O(g)+H2(g)
 N2(g)+H2O(g)(快)
N2(g)+H2O(g)(快)下列有关说法错误的是
| A.增大H2(g)的浓度能增大单位体积内气体的活化分子数,有效碰撞次数增多,速率加快 |
| B.该反应的速率主要取决于②的快慢 |
| C.N2O2和N2O是该反应的催化剂 |
| D.总反应中逆反应的活化能比正反应的活化能大 |
您最近一年使用:0次
2022-04-18更新
|
258次组卷
|
3卷引用:福建省平潭翰英中学2022-2023学年高二上学期第一次月考化学试题
名校
解题方法
8 . “一锅法”用三氧化钉(RuCl3)催化硝基苯(PhNO2,Ph—表示苯基)与醇(RCH2OH)反应生成仲胺(RCH2NHPh)的反应过程如图所示,[Ru]表示催化剂。下列叙述错误的是
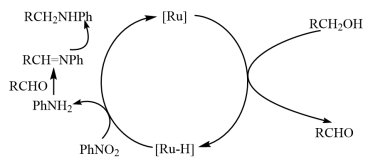

| A.RCHO是中间体,不是产物 |
| B.存在反应PhNH2+RCHO→RCH=NPh+H2O |
| C.还原反应的氢均来自RCH2OH |
| D.反应过程中Ru的成键数目有变化 |
您最近一年使用:0次
9 . 用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是
| A | B | C | D |
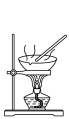 | 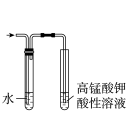 | 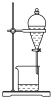 | 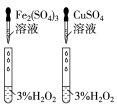 |
蒸发结晶制备 晶体 晶体 | 检验溴乙烷消去产物 | 分离苯和溴苯 | 探究不同催化剂 对  分解速率的影响 分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-18更新
|
657次组卷
|
6卷引用:福建省漳州市七校(厦大附中、龙海一中、南靖一中、平和一中、诏安一中、长泰一中、龙海二中)2021-2022学年高三下学期毕业班4月诊断性联考化学试题
名校
解题方法
10 . 下列实验方案合理的是
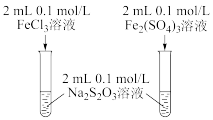 |  |
A.探究 对 对 与 与 反应速率的影响 反应速率的影响 | B.熔化 固体 固体 |
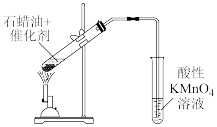 | 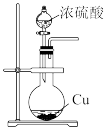 |
| C.验证石蜡油发生了裂化(或裂解)反应 | D.实验室制备SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-06更新
|
722次组卷
|
5卷引用:福建省泉州市2022届高三下学期3月质量监测(三)化学试题
福建省泉州市2022届高三下学期3月质量监测(三)化学试题福建省泉州市2022届高中毕业班质量检测(三)化学试题湖南师范大学附属中学2022届高三二模(第九次月考)化学试题(已下线)专题12 化学实验方案的设计与评价-三年(2020-2022)高考真题分项汇编巩固训练7



