名校
1 . 某合成氨速率方程为: (k为速率常数),部分数据如下表。下列说法正确的是
(k为速率常数),部分数据如下表。下列说法正确的是
 (k为速率常数),部分数据如下表。下列说法正确的是
(k为速率常数),部分数据如下表。下列说法正确的是| 实验 |  | 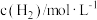 | 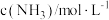 |  |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
| A.α=1,γ=-1 |
| B.采用适当催化剂,反应活化能、焓变均减小 |
| C.恒容容器中反应时,充He气,压强增大反应速率加快 |
| D.k与物质性质有关,与反应温度、压强、反应物浓度无关 |
您最近一年使用:0次
2 . 下列装置及设计不能达到实验目的的是


| A.测定中和反应的反应热 |
| B.验证Fe3+与I-反应是可逆反应 |
| C.探究温度对化学平衡的影响 |
| D.比较Fe3+和Cu2+对H2O2分解反应的催化效果 |
您最近一年使用:0次
名校
3 . 碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)查阅资料得知,反应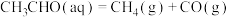 在含有少量
在含有少量 的溶液中分两步进行:第I步反应为
的溶液中分两步进行:第I步反应为 (慢反应),第II步为快反应。增大
(慢反应),第II步为快反应。增大 的浓度
的浓度___________ (填“能”或“不能”)明显增大总反应的平均速率,理由为______________________________ 。
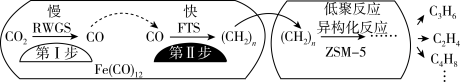
(2)用催化剂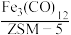 催化
催化 加氢合成乙烯的反应,所得产物含
加氢合成乙烯的反应,所得产物含 、
、 、
、 等副产物,反应过程如图。
等副产物,反应过程如图。
催化剂中添加 、K、
、K、 助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得
助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得 转化率和各产物的物质的量分数如表。
转化率和各产物的物质的量分数如表。
欲提高单位时间内乙烯的产量,在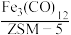 中添加
中添加__________ 助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是__________ 。
a.明显降低了该体系中所有反应的活化能
b.降低了生成乙烯反应的焓变值使反应趋势增大
c.降低了 转化率
转化率
d.明显降低了生成乙烯反应的活化能,对其他反应几乎无影响
(3)在一密闭容器中,起始时向该容器中充入 和
和 且
且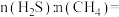 2:1,发生反应:
2:1,发生反应:
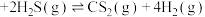 。0.11
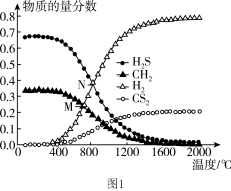
。0.11 时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高
时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是__________ (列举一条)。
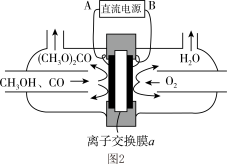
(4)合成碳酸二甲酯的工作原理如图2所示。阳极的电极反应式为__________ ,离子交换膜a为__________ (填“阳膜”、“阴膜”)。
(1)查阅资料得知,反应
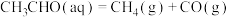 在含有少量
在含有少量 的溶液中分两步进行:第I步反应为
的溶液中分两步进行:第I步反应为 (慢反应),第II步为快反应。增大
(慢反应),第II步为快反应。增大 的浓度
的浓度(2)用催化剂
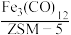 催化
催化 加氢合成乙烯的反应,所得产物含
加氢合成乙烯的反应,所得产物含 、
、 、
、 等副产物,反应过程如图。
等副产物,反应过程如图。
催化剂中添加
 、K、
、K、 助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得
助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得 转化率和各产物的物质的量分数如表。
转化率和各产物的物质的量分数如表。助剂 |
| 各产物在所有产物中的占比(%) | ||
|
| 其他 | ||
| 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
| 9.8 | 80.7 | 12.5 | 6.8 |
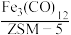 中添加
中添加a.明显降低了该体系中所有反应的活化能
b.降低了生成乙烯反应的焓变值使反应趋势增大
c.降低了
 转化率
转化率d.明显降低了生成乙烯反应的活化能,对其他反应几乎无影响
(3)在一密闭容器中,起始时向该容器中充入
 和
和 且
且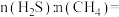 2:1,发生反应:
2:1,发生反应:
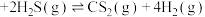 。0.11
。0.11 时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高
时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是
(4)合成碳酸二甲酯的工作原理如图2所示。阳极的电极反应式为

您最近一年使用:0次
名校
4 . 利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
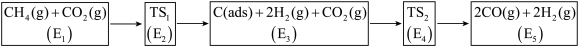
说明:
①C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ•mol-1),TS表示过渡态.
②括号中为断开该化学键需要吸收的能量:C-H(413kJ•mol-1),C=O(745kJ•mol-1),CO中的化学键(1075kJ•mol-1),下列说法不正确的是
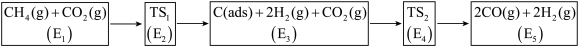
说明:
①C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ•mol-1),TS表示过渡态.
②括号中为断开该化学键需要吸收的能量:C-H(413kJ•mol-1),C=O(745kJ•mol-1),CO中的化学键(1075kJ•mol-1),下列说法不正确的是
| A.若E3+E2<E4+E1,则决定速率步骤的化学方程式为CH4(g)=C(ads)+2H2(g) |
| B.制备合成气总反应的△H可表示为(E5-E1)kJ•mol-1 |
| C.若△H=+120kJ•mol-1,断开H-H需要吸收的能量为436kJ•mol-1 |
| D.使用催化剂后,CO和H2平衡产率不改变 |
您最近一年使用:0次
名校
解题方法
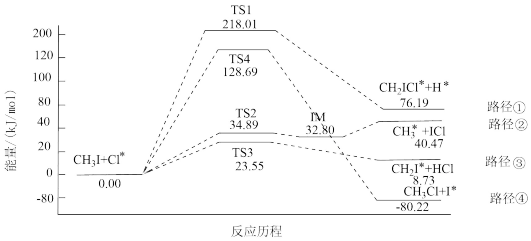
5 . 研究 与自由基
与自由基 原子(用
原子(用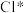 表示)的反应有助于保护臭氧层。已知:
表示)的反应有助于保护臭氧层。已知: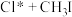 反应有4条反应路径(
反应有4条反应路径( 表示过渡态,
表示过渡态,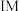 表示中间物)如图所示。(基元反应指反应中一步直接转化为产物),下列说法错误的是
表示中间物)如图所示。(基元反应指反应中一步直接转化为产物),下列说法错误的是
 与自由基
与自由基 原子(用
原子(用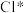 表示)的反应有助于保护臭氧层。已知:
表示)的反应有助于保护臭氧层。已知: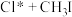 反应有4条反应路径(
反应有4条反应路径( 表示过渡态,
表示过渡态,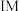 表示中间物)如图所示。(基元反应指反应中一步直接转化为产物),下列说法错误的是
表示中间物)如图所示。(基元反应指反应中一步直接转化为产物),下列说法错误的是
| A.路径①的ΔH>0 | B.路径②是基元反应 |
| C.路径③的速率最快 | D.路径④的逆反应的活化能最大 |
您最近一年使用:0次
2022-12-02更新
|
524次组卷
|
7卷引用:福建省德化一中、永安一中、漳平一中三校协作2022-2023学年高三上学期12月联考化学试题
福建省德化一中、永安一中、漳平一中三校协作2022-2023学年高三上学期12月联考化学试题福建省宁德第一中学2023届高三上学期一模考试化学试题福建省莆田第二十五中学2023-2024学年高三上学期月考四化学试题山东省淄博市2022届高三下学期第一次模拟考试化学试题(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)山东省泰安市2022-2023学年高三上学期1月期末考试化学试题湖北省部分重点中学2022-2023学年高三下学期2月质量检测化学试题
解题方法
6 . 化学在日常生活和生产中有着重要的应用。下列说法不正确的是
| A.热的纯碱溶液去油污效果好 |
B.焊接钢材时,常用饱和 溶液处理焊接点 溶液处理焊接点 |
| C.冰在室温下自动融化成水,是熵增的重要结果 |
| D.使用高效催化剂是提高原料平衡转化率的有效方法 |
您最近一年使用:0次
名校
解题方法
7 . 为比较 和
和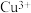 对
对 分解的催化效果,某化学研究小组的同学分别设计了图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了图甲、乙所示的实验。请回答相关问题:
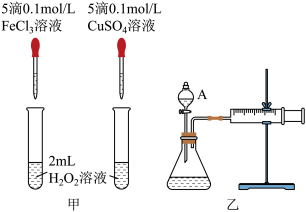
(1)定性比较:图甲可通过观察_______ 定性比较得出结论;有同学提出将 改为
改为 更合理,其理由是
更合理,其理由是_______ 。
(2)定量比较:如图乙所示,实验时均以生成40 气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是_______ ,实验中需要测量的数据是_______ 。
 和
和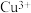 对
对 分解的催化效果,某化学研究小组的同学分别设计了图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了图甲、乙所示的实验。请回答相关问题:
(1)定性比较:图甲可通过观察
 改为
改为 更合理,其理由是
更合理,其理由是(2)定量比较:如图乙所示,实验时均以生成40
 气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
您最近一年使用:0次
名校
8 . 下列叙述中,不能用勒夏特列原理解释的是
| A.工业上采用高压条件合成氨气 |
| B.在铂铑合金催化下缩短N2和H2合成氨的时间 |
| C.Cl2在饱和食盐水中的溶解程度比在水中的小 |
D. ∆H<0,平衡后,升高温度体系颜色变深 ∆H<0,平衡后,升高温度体系颜色变深 |
您最近一年使用:0次
2022-10-18更新
|
276次组卷
|
5卷引用:福建省德化第一中学2022-2023学年高二上学期第一次质检化学试题
名校
解题方法
9 . 已知Cl2(g) + CO(g) COCl2(g)的速率方程
COCl2(g)的速率方程 [k为速率常数,只受温度影响],该反应可认为经过以下反应历程:
[k为速率常数,只受温度影响],该反应可认为经过以下反应历程:
第一步: Cl2 2Cl 快速平衡
2Cl 快速平衡
第二步: Cl+ CO COCl 快速平衡
COCl 快速平衡
第三步: COCl+Cl2→COCl2+Cl 慢反应
下列说法正确的是
 COCl2(g)的速率方程
COCl2(g)的速率方程 [k为速率常数,只受温度影响],该反应可认为经过以下反应历程:
[k为速率常数,只受温度影响],该反应可认为经过以下反应历程: 第一步: Cl2
 2Cl 快速平衡
2Cl 快速平衡第二步: Cl+ CO
 COCl 快速平衡
COCl 快速平衡第三步: COCl+Cl2→COCl2+Cl 慢反应
下列说法正确的是
| A.第一步反应和第二步反应的活化能较高 |
| B.Cl和COCl是该总反应的中间产物,也是该总反应的催化剂 |
| C.c(CO)、c(Cl2)分别增大相同的倍数,对总反应速率的影响程度前者大 |
| D.第三步反应的有效碰撞频率较大 |
您最近一年使用:0次
2022-10-14更新
|
745次组卷
|
4卷引用:福建省福州第三中学2022-2023学年高二上学期半期考试化学试题
名校
解题方法
10 . 我国科学家通过双功能催化剂催化水煤气变换反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,此时该反应总熵变记作△S。低温即可获得高转化率和高反应速率,反应过程示意图如图:
CO2(g)+H2(g) △H<0,此时该反应总熵变记作△S。低温即可获得高转化率和高反应速率,反应过程示意图如图:
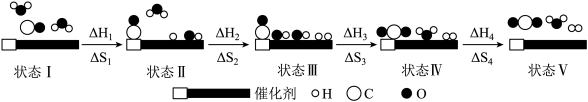
下列说法不正确的是
 CO2(g)+H2(g) △H<0,此时该反应总熵变记作△S。低温即可获得高转化率和高反应速率,反应过程示意图如图:
CO2(g)+H2(g) △H<0,此时该反应总熵变记作△S。低温即可获得高转化率和高反应速率,反应过程示意图如图:
下列说法不正确的是
| A.△H=△H1+△H2+△H3+△H4 |
| B.△S=△S1+△S2+△S3+△S4 |
| C.状态III→状态IV过程的△S3<0,△H3<0 |
| D.催化剂的使用使反应放出热量增多,温度升高导致反应速率加快 |
您最近一年使用:0次
2022-09-02更新
|
773次组卷
|
6卷引用:福建省三明第一中学2022-2023学年高二上学期第一次月考化学试题
福建省三明第一中学2022-2023学年高二上学期第一次月考化学试题浙江省山水联盟2022-2023学年高三上学期8月联考化学试题(已下线)易错点20 化学反应机理-备战2023年高考化学考试易错题(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷A(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)第二章 第三节 化学反应的方向




