名校
1 . 为减少大气污染,科学家采取多种措施处理工业废气中排放的氮氧化物(NOx)、SO2等。回答下列问题:
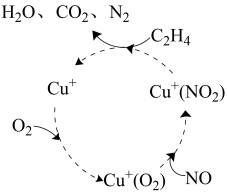
(1)某脱硝反应机理如图所示,Cu+的作用为____ ,C2H4参与的反应方程式为____ 。
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
①若有3molNO参与反应,则被NO氧化的NH3的物质的量为____ 。
②催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是____ 。
③350℃时NO的百分含量与氨氮比的关系如图所示,若只改变氨气的投放量,当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是____ (用化学方程式表示)。

(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点,ClO2在酸性条件下稳定,是性能优良的脱硫脱硝试剂。
①ClO 也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为
也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为____ 。
②某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。
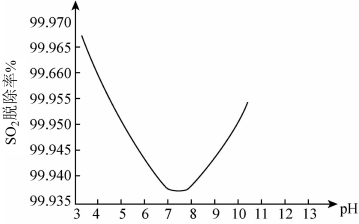
当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是:____ ;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是____ 。
(1)某脱硝反应机理如图所示,Cu+的作用为

(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
4N2(g)+6H2O(g) △H=-1627kJ·mol-1。①若有3molNO参与反应,则被NO氧化的NH3的物质的量为
②催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是
③350℃时NO的百分含量与氨氮比的关系如图所示,若只改变氨气的投放量,当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是
(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点,ClO2在酸性条件下稳定,是性能优良的脱硫脱硝试剂。
①ClO
 也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为
也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为②某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。

当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是:
您最近一年使用:0次
2022-08-29更新
|
242次组卷
|
4卷引用:福建省三明第一中学2022-2023学年高二上学期第一次月考化学试题
2 . 由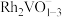 簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。
簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。
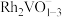 簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。
簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。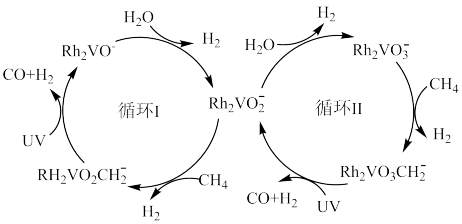
A.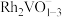 在循环中起催化作用 在循环中起催化作用 |
B.该反应可用于制取合成气 、 、 |
C.过程中包含反应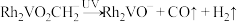 |
D.反应过程中金属元素 、V的价态均不变 、V的价态均不变 |
您最近一年使用:0次
2022-08-25更新
|
1084次组卷
|
7卷引用:福建省泉州第一中学2022-2023学年高三上学期12月月考化学试题
福建省泉州第一中学2022-2023学年高三上学期12月月考化学试题河南省十所名校高中毕业班尖子生2023届高三上学期第一次考试化学试题河南省“顶尖计划”2022-2023学年高三上学期第一次考试化学试题(已下线)易错点20 化学反应机理-备战2023年高考化学考试易错题(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)2023年湖南卷高考真题变式题(选择题11-14)2024届安徽省六安第一中学高三下学期质量检测(三 )化学试题
名校
解题方法
3 . 科研人员提出催化合成碳酸二甲酯(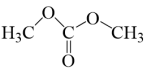 )的示意图如图所示,下列说法错误的是
)的示意图如图所示,下列说法错误的是

 )的示意图如图所示,下列说法错误的是
)的示意图如图所示,下列说法错误的是
A.过程①中有 键的断裂 键的断裂 |
B. 是中间产物 是中间产物 |
C.总反应的化学方程式为CO2+2CH3OH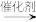  +H2O +H2O |
| D.二氧化碳、甲醇、碳酸二甲酯均能与NaOH溶液反应 |
您最近一年使用:0次
2022-07-21更新
|
92次组卷
|
6卷引用:福建省福州第三中学2021-2022学年高三上学期第六次质量检测化学试题
福建省福州第三中学2021-2022学年高三上学期第六次质量检测化学试题江西省抚州市部分中学2021-2022学年高二下学期联考化学试题(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)河南省濮阳市2021-2022学年高三上学期期中考试(11月考)化学试题江西省石城中学2022-2023学年高二下学期第三次半月考化学试题河南省名校大联考2021-2022学年高三上学期期中考试化学试题
4 . 在相同条件下研究催化剂I、Ⅱ对反应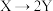 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
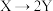 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则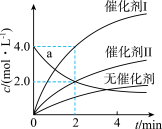
| A.无催化剂时,反应不能进行 |
| B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低 |
| C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化 |
D.使用催化剂Ⅰ时, 内, 内,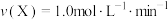 |
您最近一年使用:0次
2022-06-10更新
|
14492次组卷
|
61卷引用:福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题
福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题上海市复旦大学附属中学2022-2023学年高二上学期9月月考化学试题湖南省长沙市雅礼中学2022-2023学年高二上学期第一次月考化学试题江苏省扬州中学2022-2023学年高二上学期10月月考化学试题山东省莱州一中2022-2023学年高二上学期第一次月考化学试题湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题河南省洛阳市新安县第一高级中学2022-2023学年高三上学期9月阶段性考试化学试题宁夏银川市第二中学2022-2023学年高三上学期统练三化学试题吉林省延边第二中学2022-2023学年高三上学期第三次阶段测试化学试题广东省高州市第七中学等三校2022-2023学年高二上学期11月月考化学试题福建省厦门外国语学校石狮分校2022-2023学年高二上学期期中考试化学试题2022年新高考广东化学高考真题(已下线)2022年广东卷高考真题变式题(11-16)(已下线)专题09 化学反应速率、化学平衡-2022年高考真题模拟题分项汇编(已下线)专题09 化学反应速率、化学平衡-三年(2020-2022)高考真题分项汇编(已下线)第11练 以化学平衡图像突破化学平衡移动原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题13 化学反应速率与化学平衡-备战2023年高考化学母题题源解密(广东卷)(已下线)第20讲 化学反应速率(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第18讲 化学反应速率(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)【2022】【高二化学】【期中考】-178广东省信宜市第二中学2022-2023学年高二上学期期中考试化学试题河南省开封市祥符高级中学2023-2024学年高二上学期第一次月考化学试题广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题安徽省马鞍山市第二中学2022-2023学年高二上学期11月期中考试化学试题江苏省苏州实验中学科技城校2023-2024学年高二上学期10月月考化学试题广东省佛山市顺德区郑裕彤中学2023-2024学年上学期高一10月月考化学试题安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题福建省泉州市晋江市南侨中学2023-2024学年高二上学期11月期中考试化学试题北京市第二十二中学2022-2023学年高二上学期期中考试化学试题北京市第五十五中学2022-2023学年高三上学期期中考试化学试题广东省乐昌市第二中学2023-2024学年高三下学期保温测试(5月模拟)化学试题(已下线)专题09 化学反应速率与化学平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题17 化学平衡图表分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型114 影响化学反应速率的因素(已下线)回归教材重难点08 聚焦热、速率、平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)天津市红桥区2022-2023学年高三上学期期末考试化学试题章末检测卷(二) 化学反应速率与化学平衡四川省成都市树德中学2022-2023学年高一下学期期末考试化学试题(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题第二章 化学反应速率与化学平衡 第一节 化学反应速率 第2课时 影响化学反应速率的因素 活化能(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)考点1 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省珠海市2023-2024年高二上学期期中联考化学试题河南省实验中学2023-2024学年高二上学期期中考试化学试题广东省广州市第四十一中学2023-2024学年高二上学期期中考试化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)天津市和平区2023-2024学年高二上学期期末考试化学试卷广东省台山市某校2023-2024学年高二上学期期中考试化学试题山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题
名校
5 . 甲烷可在铑/铈氧化物的催化下与过氧化氢反应,转化为甲醇和甲基过氧化氢(CH3OOH),实现了天然气的高效利用,其原理如图所示,下列说法错误的是


| A.反应③中有极性键的断裂与生成 |
| B.反应⑤中,Ce的化合价降低 |
| C.铑/铈氧化物改变了CH4和H2O2的反应历程,降低了反应的活化能 |
| D.若用H2l8O2作反应物,一段时间后CH3OH、CH3OOH和铑/铈氧化物中均含有18O |
您最近一年使用:0次
2022-06-05更新
|
385次组卷
|
3卷引用:福建省惠安第一中学2022-2023学年高三上学期第三次月考化学试题
名校
6 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理]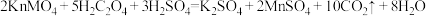
[实验内容及记录]
(1)请完成此实验设计,其中:
_______ ,
_______ 。
(2)实验①、②探究的是_______ 对化学反应速率的影响,根据表中的实验数据,可以得到的结论是_______ 。
(3)探究温度对化学反应速率的影响,应选择_______ (填实验编号)。
(4)该小组同学根据经验绘制了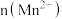 随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中
随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中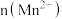 随时间变化的实际趋势如图乙所示。
随时间变化的实际趋势如图乙所示。

该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
①该小组同学提出的假设是_______ 。
②能佐证该假设成立的实验证据是_______ 。
[实验原理]
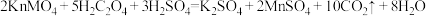
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | |||
| ① | 25 | 3.0 |  | 2.0 | 3.0 | 1.5 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| ③ | 50 | 2.0 |  | 2.0 | 3.0 | 1.7 |
(1)请完成此实验设计,其中:


(2)实验①、②探究的是
(3)探究温度对化学反应速率的影响,应选择
(4)该小组同学根据经验绘制了
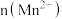 随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中
随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中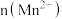 随时间变化的实际趋势如图乙所示。
随时间变化的实际趋势如图乙所示。
该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | ||||
| ④ | 25 | 2.0 | 3.0 | 2.0 | 3.0 |  | t |
②能佐证该假设成立的实验证据是
您最近一年使用:0次
名校
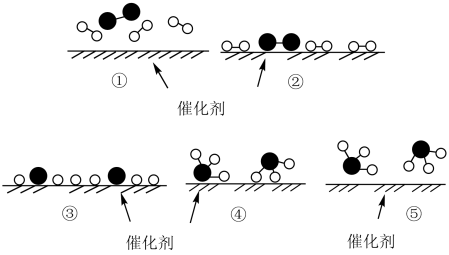
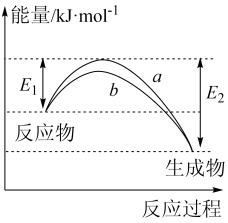
7 . 德国化学家 F.Haber 利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用 、
、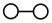 、
、 分别表示N2、H2、NH3,下列说法不正确的是
分别表示N2、H2、NH3,下列说法不正确的是
 、
、 、
、 分别表示N2、H2、NH3,下列说法不正确的是
分别表示N2、H2、NH3,下列说法不正确的是

| A.过程②为反应物吸附在催化剂表面,没有发生化学变化 |
| B.合成氨反应中,反应物断键吸收的总能量大于生成物形成新键所释放的总能量 |
| C.过程④为放热过程 |
| D.使用催化剂,能加快合成氨反应的速率 |
您最近一年使用:0次
解题方法
8 . 铜和稀硝酸在无氧环境下会生成弱酸 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。

实验过程现象记录如下表。
(1)仪器a的名称为_______ 。
(2)滴入硝酸前,为营造无氧环境,应进行的操作是_______ 。
(3)反应过程中产生的 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为_______ 。
(4)溶液呈绿色是 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
根据以上实验现象可知, 和
和_______ (填化学式)相互作用达到平衡呈绿色。
(5)取适量150 min时反应液于试管中,加入_______ ,溶液由蓝色变为绿色,,说明150 min时反应液中含有 。
。
(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因_______ 。
(7)基于上述装置,选择合适试剂,设计实验证明 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用_______ (简述实验方案及观测指标)。
 。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
。某实验小组为探究铜和稀硝酸的反应,设计实验装置如图。
实验过程现象记录如下表。
| 时间/min | 0~75 | 75~150 | 150~225 | 225~300 | 300~375 |
| 溶液颜色 | 接近无色 | 无色→浅蓝色 | 浅蓝色→绿色 | 绿色→深蓝色 | 浅蓝色 |
| 生成NO体积/mL | 0 | 1.0 | 42.0 | 137.5 | 0.5 |
| 反应体系温度/℃ | 26.6 | 26.8 | 26.8~27.2 | 27.2~28.8 | 28.8~28.6 |
(2)滴入硝酸前,为营造无氧环境,应进行的操作是
(3)反应过程中产生的
 会进一步与Cu反应生成NO,其离子方程式为
会进一步与Cu反应生成NO,其离子方程式为(4)溶液呈绿色是
 和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:
和体系中某种微粒相互作用的结果,为探究该微粒进行下列实验:| 序号 | 实验操作 | 现象 |
| a | 往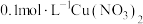 溶液中通入NO 溶液中通入NO | 溶液始终为蓝色 |
| b | 往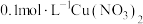 溶液中加入 溶液中加入 | 溶液变为绿色 |
| c | 往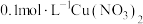 溶液中加入 溶液中加入 后逐滴加入 后逐滴加入 硝酸 硝酸 | 溶液先变为绿色后逐渐变为蓝色 |
 和
和(5)取适量150 min时反应液于试管中,加入
 。
。(6)结合平衡移动原理解释150~300 min反应液颜色变化的原因
(7)基于上述装置,选择合适试剂,设计实验证明
 对Cu与
对Cu与 硝酸的反应具有催化作用
硝酸的反应具有催化作用
您最近一年使用:0次
解题方法
9 . 我国科学家采用磷化硼(BP)纳米颗粒成功地实现了高选择性电工化还原CO2制CH3OH,CO2在阴极催化剂表面的变化及反应历程如图所示:
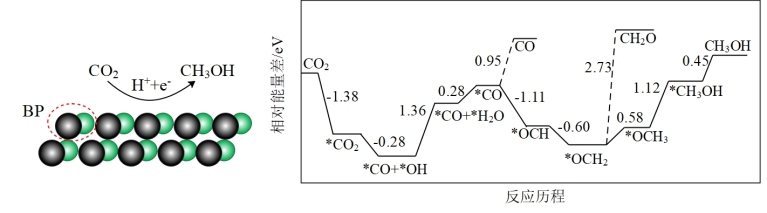
下列说法正确的是( )

下列说法正确的是( )
| A.制备CH3OH过程中得到相对较多的副产物是CH2O |
| B.在催化剂上生成CH3OH的电极反应式为CO2+6H++6e-=CH3OH+H2O |
| C.在催化剂上生成CH3OH的过程中有极性键和非极性键的断裂和生成 |
| D.*CO+*OH=*CO+*H2O为放热过程 |
您最近一年使用:0次
名校
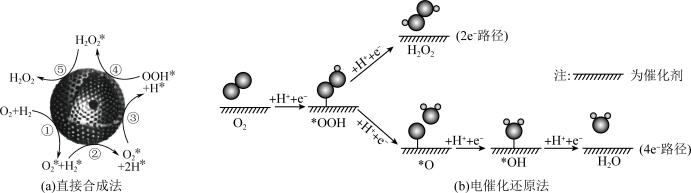
10 . 以Pd纳米粒子为核、空心多孔碳球为壳的封装型催化剂将H2和O2直接合成 的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
 的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是
| A.直接合成法中,步骤②吸收能量,步骤④释放能量 |
| B.电催化还原法制备H2O2的优点之一是避免了H2和O2共存的易爆环境 |
| C.电催化还原时,2e-路径的步骤少,反应速率快 |
D.若催化剂表面对*OOH吸附过强,则易生成O*,导致 的产率降低 的产率降低 |
您最近一年使用:0次
2022-05-05更新
|
626次组卷
|
6卷引用:福建省连城县第一中学2022-2023学年高二上学期第一次月考化学试题
福建省连城县第一中学2022-2023学年高二上学期第一次月考化学试题福建省三明市2022届普通高中毕业班下学期5月质量测试化学试题重庆市缙云教育联盟2021-2022学年高一6月质量检测化学试题湖南省岳阳市一中2021-2022学年高三下学期第三次模拟考试试题(已下线)专题07 化学反应中的能量变化-2022年高考真题模拟题分项汇编(已下线)微专题36 高考“明星”考点—催化剂-备战2023年高考化学一轮复习考点微专题



