1 . 大气污染物的治理和“碳中和”技术的开发应用成为化学研究的热点。如图表示 在
在 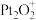 表面与
表面与  反应转化成无害气体的过程。设
反应转化成无害气体的过程。设  为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法错误 的是
 在
在 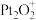 表面与
表面与  反应转化成无害气体的过程。设
反应转化成无害气体的过程。设  为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法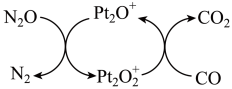
A. 和 和  分子中均有 分子中均有  个 个  键 键 |
B. 转化为 转化为 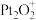 失去的电子数为 失去的电子数为  |
C. 转化成无害气体时的催化剂是 转化成无害气体时的催化剂是 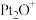 |
| D.题图转化过程中,氮元素被还原,碳元素被氧化 |
您最近一年使用:0次
解题方法
2 . 下列关于图像的描述不正确的是
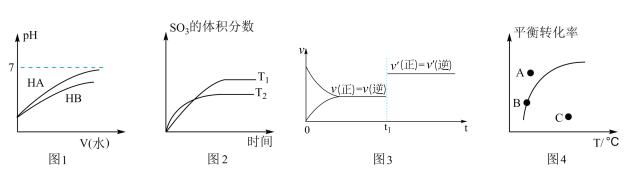

A.由图1可知 是一种弱酸 是一种弱酸 |
B.若图2发生的反应为: ,由图可知该反应的正反应是放热反应 ,由图可知该反应的正反应是放热反应 |
C.图3是可逆反应: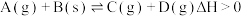 的速率时间图像,在 的速率时间图像,在 时刻改变条件只能是加入催化剂 时刻改变条件只能是加入催化剂 |
D.由4图可知,反应过程中 的点是 的点是 点 点 |
您最近一年使用:0次
名校
3 . 过氧乙酸(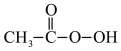 )是一种高效消毒剂。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
)是一种高效消毒剂。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
请回答下列问题:
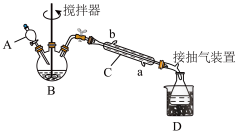
(1)仪器C的名称是_______________ ;仪器C中冷水流入口是_____ (填a或b);
(2)为更好地控制反应温度,应采用方法是_________________ ;
(3)生成过氧乙酸的化学方程式为________________________________________ ;
(4)不同反应物比例,实验测得生成过氧乙酸含量(%)随时间的变化数据(见下表),由表中数据可知,反应物最佳比例(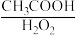 )是
)是______ ,反应所需时间约________ (选填1、3、5、7)小时;
(5)请设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率;可供选择的试剂和主要器材有:a.过氧乙酸溶液、b.1mol/L的FeCl3溶液、c.0.5mol/L的Fe2(SO4)3溶液、d.0.5mol/L的CuCl2溶液、e.1mol/L的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i.带导气管的试管。
你选择的试剂及器材是a、_______ 、f、g、i(选填序号)。
(6)碘量法分析:取2.00mL过氧乙酸试样(已除去残余H2O2)稀释成100mL,从中取出5.00mL,再加入10mL10%KI溶液和几滴淀粉溶液,摇匀(CH3COOOH+2I−+2H+=I2+CH3COOH+H2O),反应完全后再用0.1000mol/L的Na2S2O3标准液滴定至终点(反应方程式为2Na2S2O3+I2=Na2S4O6+2NaI),共消耗14.00mLNa2S2O3标准液。该样品中过氧乙酸的物质的量浓度是_____ mol/L。
 )是一种高效消毒剂。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
)是一种高效消毒剂。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
请回答下列问题:

(1)仪器C的名称是
(2)为更好地控制反应温度,应采用方法是
(3)生成过氧乙酸的化学方程式为
(4)不同反应物比例,实验测得生成过氧乙酸含量(%)随时间的变化数据(见下表),由表中数据可知,反应物最佳比例(
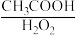 )是
)是反应物比例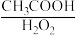 | 反应时间(小时) | ||||
| 0.5 | 1 | 3 | 5 | 7 | |
| 2∶1 | 7.38 | 8.46 | 9.42 | 11.26 | 13.48 |
| 1∶1 | 10.56 | 12.92 | 13.54 | 20.72 | 20.70 |
| 1∶2 | 6.14 | 7.10 | 7.96 | 10.38 | 12.36 |
(5)请设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率;可供选择的试剂和主要器材有:a.过氧乙酸溶液、b.1mol/L的FeCl3溶液、c.0.5mol/L的Fe2(SO4)3溶液、d.0.5mol/L的CuCl2溶液、e.1mol/L的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i.带导气管的试管。
你选择的试剂及器材是a、
(6)碘量法分析:取2.00mL过氧乙酸试样(已除去残余H2O2)稀释成100mL,从中取出5.00mL,再加入10mL10%KI溶液和几滴淀粉溶液,摇匀(CH3COOOH+2I−+2H+=I2+CH3COOH+H2O),反应完全后再用0.1000mol/L的Na2S2O3标准液滴定至终点(反应方程式为2Na2S2O3+I2=Na2S4O6+2NaI),共消耗14.00mLNa2S2O3标准液。该样品中过氧乙酸的物质的量浓度是
您最近一年使用:0次



