1 . 已知锌与稀盐酸反应放热,某学生为了探究反应过程中的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有 、
、 两种浓度,每次实验稀盐酸的用量为
两种浓度,每次实验稀盐酸的用量为 ,锌有细颗粒与粗颗粒两种规格,用量为
,锌有细颗粒与粗颗粒两种规格,用量为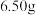 。实验温度为
。实验温度为 、
、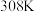 。
。
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在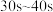 范围内盐酸的平均反应速率
范围内盐酸的平均反应速率
_______ (忽略溶液体积变化)。
②反应速率最大的时间段(如 )为
)为_______ ,可能原因是_______ ;
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率,在不影响产生气体总量的情况下,你认为他选择的溶液可以是_______(填相应字母);
(4)某化学研究小组的同学为比较 和
和 对
对 分解的催化效果,设计了图所示的实验。
分解的催化效果,设计了图所示的实验。
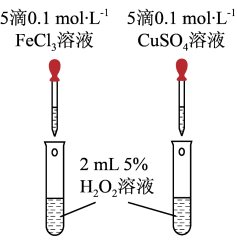
①如图可通过观察_______ 现象,比较得出比较 和
和 对
对 分解的催化效果结论。
分解的催化效果结论。
②该实验存在明显不合理的地方,你认为不合理的地方是_______ 。
 、
、 两种浓度,每次实验稀盐酸的用量为
两种浓度,每次实验稀盐酸的用量为 ,锌有细颗粒与粗颗粒两种规格,用量为
,锌有细颗粒与粗颗粒两种规格,用量为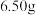 。实验温度为
。实验温度为 、
、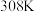 。
。(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
| 编号 |  | 锌规格 | 盐酸浓度/ | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和 (Ⅲ)实验①和实验④探究锌规格(粗、细)对该反应速率的影响。 |
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |
| 时间(s) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
氢气体积( ) ) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
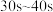 范围内盐酸的平均反应速率
范围内盐酸的平均反应速率
②反应速率最大的时间段(如
 )为
)为(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率,在不影响产生气体总量的情况下,你认为他选择的溶液可以是_______(填相应字母);
A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. |
 和
和 对
对 分解的催化效果,设计了图所示的实验。
分解的催化效果,设计了图所示的实验。
①如图可通过观察
 和
和 对
对 分解的催化效果结论。
分解的催化效果结论。②该实验存在明显不合理的地方,你认为不合理的地方是
您最近一年使用:0次
名校
解题方法
2 . 下列实验设计及操作能达到实验目的的是
| A | B | C | D |
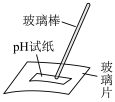 | 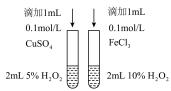 | 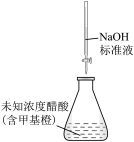 | 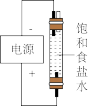 |
| 测NaClO溶液的pH | 比较 、 、 对反应速率的影响 对反应速率的影响 | 测定醋酸浓度 | 制备“84”消毒液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-03更新
|
0次组卷
|
3卷引用:湖南省邵阳市新邵县2023-2024学年高二上学期期末考试化学试题
名校
3 . 随着经济的发展,能源与环境问题越来越受到人们的重视和关注,资源利用和环境保护是当前重要研究课题,回答下列问题:
(1)合成气( 、
、 、
、 )在工业上可用来生产甲醇,有关反应的热化学方程式及不同温度下的化学平衡常数如表所示:
)在工业上可用来生产甲醇,有关反应的热化学方程式及不同温度下的化学平衡常数如表所示:
则反应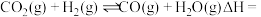
_______  (用含a、b代数式表示),
(用含a、b代数式表示),
_______ 0(填“>”或“<”)。
(2)科学家提出利用 与
与 制备“合成气”(
制备“合成气”( 、
、 ),可能的反应历程如下图所示:
),可能的反应历程如下图所示:
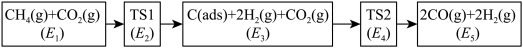
注: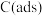 表示吸附性活性炭,E表示相对总能量,
表示吸附性活性炭,E表示相对总能量, 表示过渡态。
表示过渡态。
若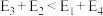 则决定制备“合成气”反应速率的化学方程式为
则决定制备“合成气”反应速率的化学方程式为_______ 。
(3)一定条件下,向密闭容器中通入一定量的 和
和 制备甲醇,投料比
制备甲醇,投料比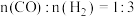 ,反应为
,反应为 ;测得容器内总压强与反应时间的关系如下图所示。
;测得容器内总压强与反应时间的关系如下图所示。
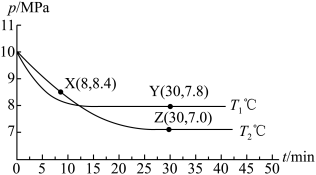
①X点的逆反应速率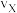 (逆)与Y点的正反应速率
(逆)与Y点的正反应速率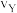 (正)的大小关系:
(正)的大小关系: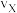 (逆)
(逆)_______ 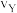 (正)(填“>”、“<”或“=”)。
(正)(填“>”、“<”或“=”)。
②图中Z点的压强平衡常数
_______ 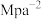 (保留两位有效数字;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(保留两位有效数字;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)利用电化学方法通过微生物电催化将 有效地转化为
有效地转化为 ,装置如图所示。
,装置如图所示。
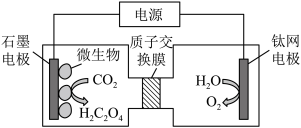
阴极区电极反应式为_______ ;当体系的温度升高到一定程度,电极反应的速率反而迅速下降,其主要原因是_______ 。装置工作时,阴极区除生成 外,还可能生成副产物并降低电解效率。已知:电解效率
外,还可能生成副产物并降低电解效率。已知:电解效率 ,标准状况下,当右池生成氧气体积为
,标准状况下,当右池生成氧气体积为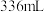 时,测得左池
时,测得左池 的物质的量为
的物质的量为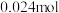 ,则电解效率为
,则电解效率为_______ 。
(1)合成气(
 、
、 、
、 )在工业上可用来生产甲醇,有关反应的热化学方程式及不同温度下的化学平衡常数如表所示:
)在工业上可用来生产甲醇,有关反应的热化学方程式及不同温度下的化学平衡常数如表所示:| 热化学方程式 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | ||
Ⅰ.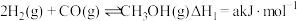 |  | 2.50 | 0.340 | 0.150 |
Ⅱ.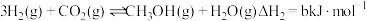 |  | 2.50 | 0.578 | 0.378 |
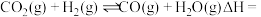
 (用含a、b代数式表示),
(用含a、b代数式表示),
(2)科学家提出利用
 与
与 制备“合成气”(
制备“合成气”( 、
、 ),可能的反应历程如下图所示:
),可能的反应历程如下图所示: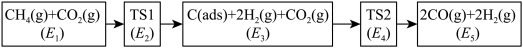
注:
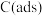 表示吸附性活性炭,E表示相对总能量,
表示吸附性活性炭,E表示相对总能量, 表示过渡态。
表示过渡态。若
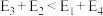 则决定制备“合成气”反应速率的化学方程式为
则决定制备“合成气”反应速率的化学方程式为(3)一定条件下,向密闭容器中通入一定量的
 和
和 制备甲醇,投料比
制备甲醇,投料比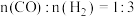 ,反应为
,反应为 ;测得容器内总压强与反应时间的关系如下图所示。
;测得容器内总压强与反应时间的关系如下图所示。
①X点的逆反应速率
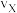 (逆)与Y点的正反应速率
(逆)与Y点的正反应速率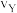 (正)的大小关系:
(正)的大小关系: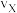 (逆)
(逆)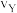 (正)(填“>”、“<”或“=”)。
(正)(填“>”、“<”或“=”)。②图中Z点的压强平衡常数

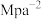 (保留两位有效数字;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(保留两位有效数字;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)利用电化学方法通过微生物电催化将
 有效地转化为
有效地转化为 ,装置如图所示。
,装置如图所示。
阴极区电极反应式为
 外,还可能生成副产物并降低电解效率。已知:电解效率
外,还可能生成副产物并降低电解效率。已知:电解效率 ,标准状况下,当右池生成氧气体积为
,标准状况下,当右池生成氧气体积为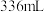 时,测得左池
时,测得左池 的物质的量为
的物质的量为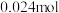 ,则电解效率为
,则电解效率为
您最近一年使用:0次
2023-02-11更新
|
112次组卷
|
2卷引用:湖南省怀化市2022-2023学年高二上学期期末考试化学试题



