1 . 某学生为探究锌与稀盐酸反应的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00mol·L-1、2.00mol·L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g。实验温度为25℃、35℃。(已知Zn2+对该反应的反应速率无影响)
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30~40s范围内盐酸的平均反应速率ν(HCl)=_______ (忽略溶液体积变化);
②反应速率最大的时间段(如0~10s)为_______ ,可能原因是_______ ;
③反应速率后段明显下降的主要影响因素是_______ 。
(3)测量氢气体积时,在不影响产生H2气体总量的情况下,往往在盐酸中分别加入相同体积的下列溶液以减慢反应速率,你认为可行的是_______(填序号)。
(4)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
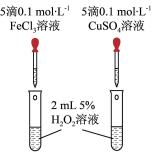
①如图可通过观察_______ 现象,比较得出Fe3+和Cu2+对H2O2分解的催化效果结论;
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______ 。
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
| 编号 | t/℃ | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | I.实验①和②探究盐酸浓度对该反应速率的影响; II.实验 III.实验 |
| ② | 25 | 粗颗粒 | 1.00 | |
| ③ | 35 | 粗颗粒 | 2.00 | |
| ④ | 25 | 细颗粒 | 2.00 |
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积/mL | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(如0~10s)为
③反应速率后段明显下降的主要影响因素是
(3)测量氢气体积时,在不影响产生H2气体总量的情况下,往往在盐酸中分别加入相同体积的下列溶液以减慢反应速率,你认为可行的是_______(填序号)。
| A.NaNO3溶液 | B.NaCl溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |

①如图可通过观察
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
您最近一年使用:0次
名校
2 . (1)甲元素位于元素周期表的第3周期Ⅱ A族,乙元素的原子结构示意图为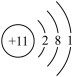
①写乙元素的元素符号:___________ 。
②甲元素原子核外有_________ 个电子层。
③甲元素的金属性(即原子失电子的能力)比乙元素_________ (填“强”或“弱”)。
(2)过氧化氢在适当条件下能发生分解反应:2H2O2=2H2O+O2↑,现进行如下实验探究:在甲、乙两支大小相同的试管中各装入3mL 5%的过氧化氢溶液,再向其中的甲试管中加入少量MnO2粉末。请给合实验现象填写下列空白。
①实验目的:研究催化剂对过氧化氢分解反应速率的影响。
②实验现象:___________ (选填“甲”或“乙”)试管中反应更剧烈,迅速放出无色气体。
③实验结论____________________________________________________ 。

①写乙元素的元素符号:
②甲元素原子核外有
③甲元素的金属性(即原子失电子的能力)比乙元素
(2)过氧化氢在适当条件下能发生分解反应:2H2O2=2H2O+O2↑,现进行如下实验探究:在甲、乙两支大小相同的试管中各装入3mL 5%的过氧化氢溶液,再向其中的甲试管中加入少量MnO2粉末。请给合实验现象填写下列空白。
①实验目的:研究催化剂对过氧化氢分解反应速率的影响。
②实验现象:
③实验结论
您最近一年使用:0次
名校
解题方法
3 . 某校兴趣小组同学为比较Fe3+和Cu2+对H2O2分解的催化效果,分别设计了如图甲、乙两种实验装置。

回答下列问题:
(1)若利用甲装置,可通过观察____ 的现象,从而定性比较得出结论。
(2)有同学提出将CuSO4溶液改为CuCl2溶液更为合理,其理由是____ 。写出H2O2在催化剂作用下发生反应的化学方程式:____ 。
(3)利用乙装置可进行定量分析,乙中仪器A的名称为____ ,实验时均以生成20mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是____ 。
(4)在Fe3+催化作用下,50mL某浓度的H2O2在标准状况下放出气体的体积和时间的关系如图所示,解释反应速率变化的原因:____ ;H2O2初始物质的量浓度为____ ;0~4min内H2O2的平均反应速率为____ mol·L-1·min-1。


回答下列问题:
(1)若利用甲装置,可通过观察
(2)有同学提出将CuSO4溶液改为CuCl2溶液更为合理,其理由是
(3)利用乙装置可进行定量分析,乙中仪器A的名称为
(4)在Fe3+催化作用下,50mL某浓度的H2O2在标准状况下放出气体的体积和时间的关系如图所示,解释反应速率变化的原因:

您最近一年使用:0次



