名校
解题方法
1 . 阅读题目,回答问题:
(1)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为___________ 。
(2)为探究 在
在 制取
制取 反应中的作用,某兴趣小组进行下列实验:向试管中加入
反应中的作用,某兴趣小组进行下列实验:向试管中加入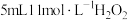 溶液,静置几分钟,无明显现象;滴加2滴
溶液,静置几分钟,无明显现象;滴加2滴 溶液,立即产生大量气泡,加
溶液,立即产生大量气泡,加 溶液反应
溶液反应 后,
后, 的浓度变为
的浓度变为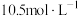 ,则20min内H2O2的平均反应速率为
,则20min内H2O2的平均反应速率为___________ 。
(3)H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等。某兴趣小组为探究外界条件对H2O2分解反应速率的影响,设计如表所示实验。填写表中空白内容:
(4)如图装置可以把氢气中蕴含的化学能转化为电能,被称为氢氧燃料电池。
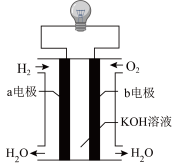
①该电池的正极是电极___________ (填“a”或“b”),负极发生反应的方程式为___________ 。
②电池工作时,当外电路中转移 电子时,消耗的
电子时,消耗的 在标准状况下体积为
在标准状况下体积为___________ 。
(1)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为
(2)为探究
 在
在 制取
制取 反应中的作用,某兴趣小组进行下列实验:向试管中加入
反应中的作用,某兴趣小组进行下列实验:向试管中加入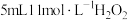 溶液,静置几分钟,无明显现象;滴加2滴
溶液,静置几分钟,无明显现象;滴加2滴 溶液,立即产生大量气泡,加
溶液,立即产生大量气泡,加 溶液反应
溶液反应 后,
后, 的浓度变为
的浓度变为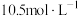 ,则20min内H2O2的平均反应速率为
,则20min内H2O2的平均反应速率为(3)H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等。某兴趣小组为探究外界条件对H2O2分解反应速率的影响,设计如表所示实验。填写表中空白内容:
| 试管编号 | 实验目的 |  溶液 溶液 | 温度 | 水的体积/mL |  溶液体积/mL 溶液体积/mL | |
| 质量分数 | 体积/mL | |||||
| I | 为编号Ⅱ实验的参照 | 12% | 5.0 | 常温 | 0 | 0 |
| Ⅱ | 温度对反应速率的影响 | 12% | 5.0 | 60℃ | 0 | 0 |
| Ⅲ | 为编号Ⅳ实验的参照 | 4.0% | 5.0 | 常温 | ① | 0 |
| Ⅳ | ② | 4.0% | 5.0 | 常温 | 0 | 1.0 |

①该电池的正极是电极
②电池工作时,当外电路中转移
 电子时,消耗的
电子时,消耗的 在标准状况下体积为
在标准状况下体积为
您最近一年使用:0次
2023-05-16更新
|
256次组卷
|
2卷引用:广东省广州市第六十五中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
2 . 为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验。请回答下列问题:
(1)实验①的目的是其它条件相同时,探究______ 条件对H2O2分解速率的影响。
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,请你用实验中所提供的几种试剂,对上述操作进行的改进是____________________________________ 。
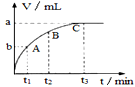
(3)某同学在50mL一定浓度的H2O2溶液中加入适量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是____ (填字母代号)。
(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该化学兴趣小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
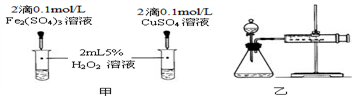
①定性分析:如图甲可通过观察________________________ ,定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是______________________ 。
②定量分析:用图乙所示装置做对照试验,实验时均以3min时间为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是________________ ,所需仪器为_______ 。
(5)通过对上述实验过程的分析,在实验设计时,要考虑_________ 思想方法的应用。
| 编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入2滴1mol/LFeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡; 试管B中产生的气泡量增多。 |
| ② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2溶液。 | 两支试管中均未明显见到有气泡产生。 |
(1)实验①的目的是其它条件相同时,探究
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,请你用实验中所提供的几种试剂,对上述操作进行的改进是
(3)某同学在50mL一定浓度的H2O2溶液中加入适量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是

(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该化学兴趣小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

①定性分析:如图甲可通过观察
②定量分析:用图乙所示装置做对照试验,实验时均以3min时间为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(5)通过对上述实验过程的分析,在实验设计时,要考虑
您最近一年使用:0次
2018-04-25更新
|
651次组卷
|
4卷引用:湖北省沙市中学2017-2018学年高一下学期期中考试化学试题
湖北省沙市中学2017-2018学年高一下学期期中考试化学试题江苏省启东中学2017-2018学年高一下学期期中考试化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第二单元 化学反应速率与化学平衡单元测试A卷河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学(实验班)试题
3 . 已知软锰矿和锰结核矿的主要成分均为MnO2,二氧化锰的制备和性质在生产生活和化学实验中有广泛应用。
二氧化锰的制备:
锰粉的主要成分为NH4Cl、C和MnO2,将锰粉进行如图所示操作后,可得到二氧化锰固体。
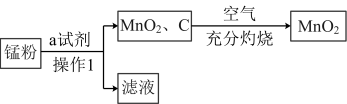
(1)某同学认为试剂a为蒸馏水,你认为______ (填“能”或“不能”)实现实验目的。
(2)操作1的名称是______ ,所用到的玻璃仪器有烧杯、玻璃棒和______ 。
(3)在空气中充分灼烧的目的是_________ 。
二氧化锰的性质检验:
Ⅰ.氧化性
(4)实验室用MnO2与浓盐酸反应制备Cl2,可以选用的装置是______ (填字母)。
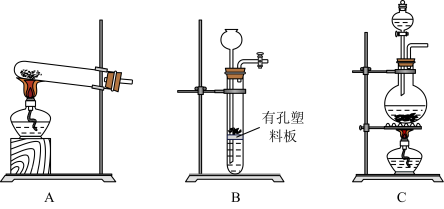
(5)将MnO2放在NH3气流中加热,可得到棕黑色的Mn2O3和N2,该反应的化学方程式为_______ 。
Ⅱ.还原性
(6)下列流程所发生的反应中,氧化剂与还原剂的物质的量之比为______ 。

Ⅲ.催化性
MnO2是实验室制取O2的催化剂。某同学设计实验探究双氧水分解的实验方案如下表所示。
(7)本实验的待测数据是___________ 。
(8)由实验①和②可得出的结论是______________________ 。
二氧化锰的制备:
锰粉的主要成分为NH4Cl、C和MnO2,将锰粉进行如图所示操作后,可得到二氧化锰固体。

(1)某同学认为试剂a为蒸馏水,你认为
(2)操作1的名称是
(3)在空气中充分灼烧的目的是
二氧化锰的性质检验:
Ⅰ.氧化性
(4)实验室用MnO2与浓盐酸反应制备Cl2,可以选用的装置是

(5)将MnO2放在NH3气流中加热,可得到棕黑色的Mn2O3和N2,该反应的化学方程式为
Ⅱ.还原性
(6)下列流程所发生的反应中,氧化剂与还原剂的物质的量之比为

Ⅲ.催化性
MnO2是实验室制取O2的催化剂。某同学设计实验探究双氧水分解的实验方案如下表所示。
| 实验序号 | w(H2O2)/% | 粉状MnO2/g | 温度/℃ | 待测数据 |
| ① | 5 | 0 | 20 | |
| ② | 5 | 1.0 | 20 |
(8)由实验①和②可得出的结论是
您最近一年使用:0次
名校
4 . 某学习小组对硝酸工业活性炭脱硝工艺进行探究。回答下列问题:
Ⅰ.硝酸工业产生的烟气中含有大量 ,工艺如图所示:
,工艺如图所示:
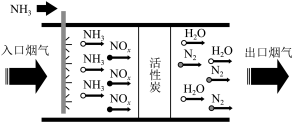
(1)该流程中活性炭是催化剂,加入催化剂的目的是___________ 。
(2)若要使 和
和 恰好充分反应。则反应混合物中
恰好充分反应。则反应混合物中 与
与 的体积比为
的体积比为___________ (用含x的式子表示)。
Ⅱ.某同学为了探究干燥条件下 与
与 的反应,设计如图所示实验装置进行实验。
的反应,设计如图所示实验装置进行实验。

(3)装置A为氨气的发生装置,应选用___________ (填“X”或“Y”)为此实验制备氨气的装置,相关反应的化学方程式为___________ 。
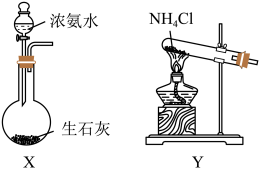
(4)该实验设计中存在缺陷,请写出解决方案:___________ 。
(5)装置D用于制备 气体。
气体。
①有同学推测反应过程中有可能产生NO,该同学做此推测的理由为___________ 。
②装置D中发生反应的实验现象为___________ 。
③ 能与碱液反应,故在拆装置之前,应该怎么操作
能与碱液反应,故在拆装置之前,应该怎么操作___________ 。
Ⅰ.硝酸工业产生的烟气中含有大量
 ,工艺如图所示:
,工艺如图所示:
(1)该流程中活性炭是催化剂,加入催化剂的目的是
(2)若要使
 和
和 恰好充分反应。则反应混合物中
恰好充分反应。则反应混合物中 与
与 的体积比为
的体积比为Ⅱ.某同学为了探究干燥条件下
 与
与 的反应,设计如图所示实验装置进行实验。
的反应,设计如图所示实验装置进行实验。
(3)装置A为氨气的发生装置,应选用

(4)该实验设计中存在缺陷,请写出解决方案:
(5)装置D用于制备
 气体。
气体。①有同学推测反应过程中有可能产生NO,该同学做此推测的理由为
②装置D中发生反应的实验现象为
③
 能与碱液反应,故在拆装置之前,应该怎么操作
能与碱液反应,故在拆装置之前,应该怎么操作
您最近一年使用:0次
名校
解题方法
5 . 亚硝酰硫酸( )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
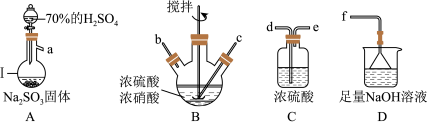
已知:i.亚硝酰硫酸遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解;
 .实验室制备亚硝酰硫酸的原理为
.实验室制备亚硝酰硫酸的原理为 ,
,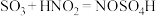 。
。
(1)仪器Ⅰ的名称为___________ ,按照气流从左到右的顺序,上述仪器的连接顺序为___________ (填仪器接口的字母,字母之间用“→”连接,部分仪器可以重复使用),C装置的作用为___________ 。
(2)反应需控制温度在25~40℃,采用的加热措施为___________ ,开始时反应缓慢,但某时刻反应速率明显加快,其原因可能是___________ 。
(3)测定亚硝酰硫酸的纯度:
步骤①:准确称取 产品,在特定条件下配制成
产品,在特定条件下配制成 溶液。
溶液。
步骤②:取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入 未知浓度
未知浓度 溶液(过量)和
溶液(过量)和 的
的 溶液,摇匀,发生反应
溶液,摇匀,发生反应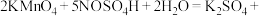
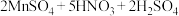
步骤③:向该溶液中滴加 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为
溶液的体积为 。
。
步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗 溶液的体积为
溶液的体积为 。
。
滴定终点时的现象为___________ ,亚硝酰硫酸的纯度为___________ (精确到 )。
)。
 )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
已知:i.亚硝酰硫酸遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解;
 .实验室制备亚硝酰硫酸的原理为
.实验室制备亚硝酰硫酸的原理为 ,
,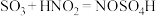 。
。(1)仪器Ⅰ的名称为
(2)反应需控制温度在25~40℃,采用的加热措施为
(3)测定亚硝酰硫酸的纯度:
步骤①:准确称取
 产品,在特定条件下配制成
产品,在特定条件下配制成 溶液。
溶液。步骤②:取
 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入 未知浓度
未知浓度 溶液(过量)和
溶液(过量)和 的
的 溶液,摇匀,发生反应
溶液,摇匀,发生反应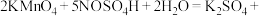
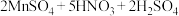
步骤③:向该溶液中滴加
 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为
溶液的体积为 。
。步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗
 溶液的体积为
溶液的体积为 。
。滴定终点时的现象为
 )。
)。
您最近一年使用:0次
2023-05-19更新
|
454次组卷
|
6卷引用:山东省聊城市百师联盟2023届高三下学期(二轮复习联考)模拟预测(三)化学试题
山东省聊城市百师联盟2023届高三下学期(二轮复习联考)模拟预测(三)化学试题山西省忻州市2023届高三下学期二轮复习联考(三)理综化学试题河南省开封市2022-2023学年高三下学期5月月考理综化学试题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)江西省丰城中学、新建二中2022-2023学年高二下学期期末联考化学试题(已下线)实验探究题
解题方法
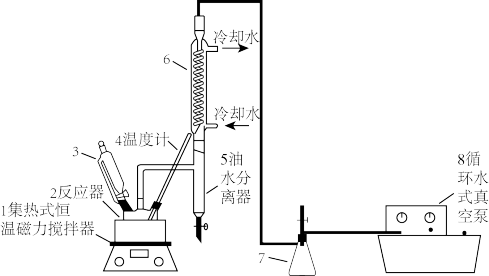
6 . 过氧乙酸(CH3COOOH)不仅在卫生医疗、食品消毒及漂白剂领域有广泛应用,也应用于环境工程、精细化工等领域。实验室利用醋酸(CH3COOH)与双氧水(H2O2)共热,在固体酸的催化下制备过氧乙酸(CH3COOOH),其装置如下图所示。请回答下列问题:
实验步骤:
Ⅰ.先在反应瓶中加入冰醋酸、乙酸丁酯和固体酸催化剂,开通仪器1和8,温度维持为55℃;
Ⅱ.待真空度达到反应要求时,打开仪器3的活塞,逐滴滴入浓度为35%的双氧水,再通入冷却水;
Ⅲ.从仪器5定期放出乙酸丁酯和水的混合物,待反应结束后分离反应器2中的混合物,得到粗产品。
(1)反应器 2中制备过氧乙酸(CH3COOOH)的化学反应方程式为_______ 。
(2)反应中维持冰醋酸过量,目的是提高_______ ;分离反应器 中的混合物得到粗产品,分离的方法是
中的混合物得到粗产品,分离的方法是_______ 。
(3)实验中加入乙酸丁酯的主要作用是_______(选填字母序号)。
(4)待观察到_______ (填现象)时,反应结束。
(5)粗产品中过氧乙酸(CH3COOOH)含量的测定:取一定体积的样品V mL,分成6等份,用过量KI溶液与过氧化物作用,以0.1 mol·L-1的硫代硫酸钠溶液滴定碘(I2+2S2O =2I-+S4O
=2I-+S4O );重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为
);重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为_______ mol·L-1。
(6)通过研究发现Fe3+、Cu2+可催化过氧乙酸分解为氧气和乙酸,现需设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率。可供选择的试剂和主要器材有:a. 过氧乙酸溶液、b. 1mol·L-1的FeCl3溶液、c. 0.5 mol·L-1的Fe2(SO4)3溶液、d. 0.5 mol·L-1的CuCl2溶液、e.1 mol·L-1的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i. 带导气管的试管。
你设计的实验方案为_______ 。

实验步骤:
Ⅰ.先在反应瓶中加入冰醋酸、乙酸丁酯和固体酸催化剂,开通仪器1和8,温度维持为55℃;
Ⅱ.待真空度达到反应要求时,打开仪器3的活塞,逐滴滴入浓度为35%的双氧水,再通入冷却水;
Ⅲ.从仪器5定期放出乙酸丁酯和水的混合物,待反应结束后分离反应器2中的混合物,得到粗产品。
(1)反应器 2中制备过氧乙酸(CH3COOOH)的化学反应方程式为
(2)反应中维持冰醋酸过量,目的是提高
 中的混合物得到粗产品,分离的方法是
中的混合物得到粗产品,分离的方法是(3)实验中加入乙酸丁酯的主要作用是_______(选填字母序号)。
| A.作为反应溶剂,提高反应速率 |
| B.与固体酸一同作为催化剂使用,提高反应速率 |
| C.与水形成沸点更低的混合物,利于水的蒸发,提高产率 |
| D.增大油水分离器5的液体量,便于实验观察 |
(5)粗产品中过氧乙酸(CH3COOOH)含量的测定:取一定体积的样品V mL,分成6等份,用过量KI溶液与过氧化物作用,以0.1 mol·L-1的硫代硫酸钠溶液滴定碘(I2+2S2O
 =2I-+S4O
=2I-+S4O );重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为
);重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为(6)通过研究发现Fe3+、Cu2+可催化过氧乙酸分解为氧气和乙酸,现需设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率。可供选择的试剂和主要器材有:a. 过氧乙酸溶液、b. 1mol·L-1的FeCl3溶液、c. 0.5 mol·L-1的Fe2(SO4)3溶液、d. 0.5 mol·L-1的CuCl2溶液、e.1 mol·L-1的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i. 带导气管的试管。
你设计的实验方案为
您最近一年使用:0次
2022-06-25更新
|
156次组卷
|
2卷引用:辽宁省部分中学2021-2022学年高二下学期期末检测化学试题
7 . 亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。
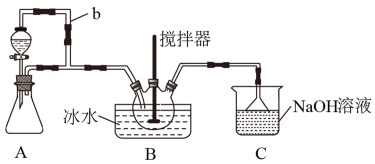
(1)装置A制取SO2
①A中反应的化学方程式为___ 。
②导管b的作用是___ 。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以是___ (只写1种)。
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是___ 。
(3)装置C的主要作用是___ (用离子方程式表示)。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是___ 。
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:__ MnO4-+__ C2O42-+__ =__ Mn2++__ +__ H2O
②滴定终点时的现象为___ 。
③亚硝酰硫酸的纯度=___ 。(精确到0.1%)[M(NOSO4H)=127g·mol-1]

(1)装置A制取SO2
①A中反应的化学方程式为
②导管b的作用是
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以是
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是
(3)装置C的主要作用是
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:
②滴定终点时的现象为
③亚硝酰硫酸的纯度=
您最近一年使用:0次
2020-03-10更新
|
390次组卷
|
3卷引用:【市级联考】福建省泉州市2019届高三毕业班下学期第一次质量检查理科综合化学试题
23-24高二·全国·假期作业
8 . 某学生为探究锌与稀盐酸反应的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00mol·L-1、2.00mol·L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g。实验温度为25℃、35℃。(已知Zn2+对该反应速率无影响)
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30~40s范围内盐酸的平均反应速率ν(HCl)=___________ (忽略溶液体积变化);
②反应速率最大的时间段(如0~10s)为___________ ,可能原因是___________ ;
③反应速率后段明显下降的主要影响因素是___________ 。
(3)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。___________ 现象,比较得出Fe3+和Cu2+对H2O2分解的催化效果结论;
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是___________ 。
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
| 编号 | t/℃ | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | I.实验①和②探究盐酸浓度对该反应速率的影响; Ⅱ.实验 Ⅲ.实验 |
| ② | 25 | 粗颗粒 | 1.00 | |
| ③ | 35 | 粗颗粒 | 2.00 | |
| ④ | 25 | 细颗粒 | 2.00 |
(2)实验①记录如下(换算成标况):
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积/mL | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(如0~10s)为
③反应速率后段明显下降的主要影响因素是
(3)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
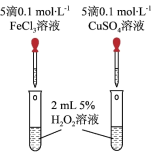
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
您最近一年使用:0次
名校
9 . 氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。
Ⅰ. 某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
(1)实验①和②的目的是___ 。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是__________ (写出一种即可)。
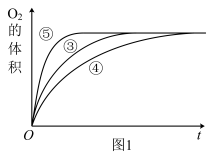
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图1所示。分析该图能够得出的实验结论是____ 。
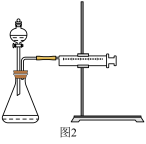
Ⅱ. MnO2对H2O2的分解有催化作用,某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将状态不同的0.1 g MnO2分别加入盛有50 mL等浓度的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出大试管中发生反应的化学方程式:__ ,该反应是____ 反应(填“放热”或“吸热”)。
(2)实验结果表明,催化剂的催化效果与____ 有关。
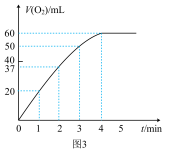
(3)实验过程中放出气体的体积(标准状况)和时间的关系如图3所示。解释反应速率变化的原因:__ ,计算H2O2的初始物质的量浓度为____ 。(保留两位有效数字)
Ⅰ. 某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液+1 mL H2O | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+1 mL HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+1 mL NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图1所示。分析该图能够得出的实验结论是



Ⅱ. MnO2对H2O2的分解有催化作用,某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将状态不同的0.1 g MnO2分别加入盛有50 mL等浓度的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
| MnO2状态 | 触摸试管情况 | 观察结果 | 反应完成所需时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 4 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(2)实验结果表明,催化剂的催化效果与
(3)实验过程中放出气体的体积(标准状况)和时间的关系如图3所示。解释反应速率变化的原因:
您最近一年使用:0次
2019-06-12更新
|
255次组卷
|
3卷引用:江苏省宝应中学2017-2018学年高二第二学期期中考试化学试题
名校
10 . (1)某小组同学在烧杯中加入5mL1.0mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,则该反应是_____________ (填“吸热”或“放热”)反应,其能量变化可用图中的____________ (填“B”或“C”)表示。

(2)已知拆开1molH-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mol NH3时反应___________ (填“放出”或“吸收”)________ kJ 的热量。
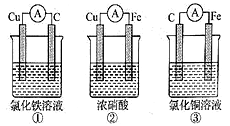
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是______ (填序号),写出正极的电极反应_____________________ 。若构建原电池时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为________ g。

(2)已知拆开1molH-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mol NH3时反应
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是

您最近一年使用:0次
2018-06-23更新
|
131次组卷
|
3卷引用:【全国百强校】江西省高安中学2017-2018学年高一6月月考(创新班)化学试题



