名校
1 . 当前,世界多国相继规划了“碳达峰”、“碳中和”的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)工业上有一种方法是用 来生产燃料甲醇。为探究该反应原理,进行如下实验:某温度下,在容积为5L的密闭容器中,充入4mol
来生产燃料甲醇。为探究该反应原理,进行如下实验:某温度下,在容积为5L的密闭容器中,充入4mol 和12mol
和12mol 在一定条件下发生反应生成
在一定条件下发生反应生成 ,测得
,测得 、
、 (g)和
(g)和 (g)的物质的量(n)随时间变化如图所示。
(g)的物质的量(n)随时间变化如图所示。

①反应到第2分钟时,氢气的浓度为___________ 。
②该温度下,此反应的平衡常数K=___________ (保留一位小数)。
③保持温度和体积不变,向上述平衡体系中再同时充入1.5mol 和0.5mol
和0.5mol ,平衡
,平衡___________ (填“正向”“逆向”或“不”)移动。
④下列措施中,一定能使 的平衡转化率增大的是
的平衡转化率增大的是___________ (填标号)。
A.在原容器中充入1mol氦气 B.在原容器中再充入1mol
C.在原容器中再充入1mol D.使用更有效的催化剂
D.使用更有效的催化剂
E.增大容器的容积 F.将水蒸气从体系中分离
(2)甲醇的组成元素的电负性从大到小依次为___________ 。
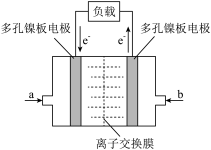
(3)甲醇被称为21世纪新型燃料,可用于甲醇燃料电池,如图(电解质溶液为稀硫酸),则a处通入的是(填“甲醇”或“氧气”)___________ ,其电极上发生的电极反应式为___________ 。若将电解质溶液换成KOH溶液,则该燃料电池的电极总反应式为___________ 。
(1)工业上有一种方法是用
 来生产燃料甲醇。为探究该反应原理,进行如下实验:某温度下,在容积为5L的密闭容器中,充入4mol
来生产燃料甲醇。为探究该反应原理,进行如下实验:某温度下,在容积为5L的密闭容器中,充入4mol 和12mol
和12mol 在一定条件下发生反应生成
在一定条件下发生反应生成 ,测得
,测得 、
、 (g)和
(g)和 (g)的物质的量(n)随时间变化如图所示。
(g)的物质的量(n)随时间变化如图所示。
①反应到第2分钟时,氢气的浓度为
②该温度下,此反应的平衡常数K=
③保持温度和体积不变,向上述平衡体系中再同时充入1.5mol
 和0.5mol
和0.5mol ,平衡
,平衡④下列措施中,一定能使
 的平衡转化率增大的是
的平衡转化率增大的是A.在原容器中充入1mol氦气 B.在原容器中再充入1mol

C.在原容器中再充入1mol
 D.使用更有效的催化剂
D.使用更有效的催化剂E.增大容器的容积 F.将水蒸气从体系中分离
(2)甲醇的组成元素的电负性从大到小依次为
(3)甲醇被称为21世纪新型燃料,可用于甲醇燃料电池,如图(电解质溶液为稀硫酸),则a处通入的是(填“甲醇”或“氧气”)

您最近一年使用:0次
名校
2 . 一定条件下的恒容密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),下图表示反应过程中能量 的变化。下列说法不正确的是
2NH3(g),下图表示反应过程中能量 的变化。下列说法不正确的是

 2NH3(g),下图表示反应过程中能量 的变化。下列说法不正确的是
2NH3(g),下图表示反应过程中能量 的变化。下列说法不正确的是
| A.加入催化剂不改变该反应的反应热 |
| B.b 曲线是加入催化剂时的能量变化曲线 |
| C.在常温、体积一定的条件下,通入 1 mol N2和 3 mol H2反应后放出的热量为 92 kJ |
| D.温度降低,平衡正向移动,N2转化率增大 |
您最近一年使用:0次
2023-08-19更新
|
204次组卷
|
3卷引用:湖南省张家界市慈利县第一中学2023-2024学年高二上学期第二次月考化学试题



