1 . 实验室模拟工业处理含铬废水,操作及现象如图1,反应过程中铬元素的化合价变化如图2,下列说法正确的是
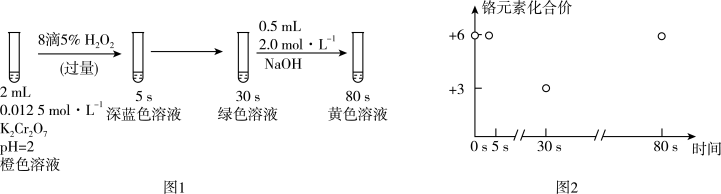
已知:深蓝色溶液中生成了CrO5

已知:深蓝色溶液中生成了CrO5
| A.实验开始至5s,铬元素被氧化 |
B.实验开始至30s,溶液中生成Cr3+的总反应离子方程式为: +3H2O2+8H+=2Cr3++7H2O+3O2↑ +3H2O2+8H+=2Cr3++7H2O+3O2↑ |
| C.30s至80s的过程,一定是氧气氧化了Cr3+ |
| D.80s时,溶液中又生成了Cr2O3,颜色相比于开始时浅,是水稀释所致 |
您最近一年使用:0次
解题方法
2 . 铜及其化合物有广泛的应用。氯化亚铜(CuCl)微溶于水,不溶于酒精,在潮湿空气中易水解氧化。某课外小组以某工业废渣(主要成分为硅、铜、碳等)为原料制备CuCl的流程示意图如图所示。
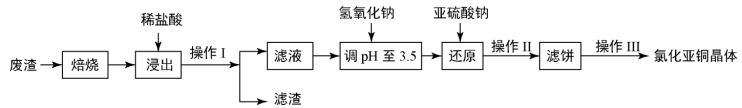
(1)“滤渣”的主要成分为______ (填化学式)。
(2)“还原”过程中Cu2+还原为CuCl,请写出反应的离子方程式:_________ 。
(3)还原过程中加入的Na2SO3过量,目的是除去氧气防止CuCl被氧化,原理是______ (用化学方程式表示)。
(4)CuCl在潮湿的环境中容易被氧化生成Cu2(OH)3Cl,反应化学方程式是__________ 。
(5)CuCl粗品中含有Cu2+加入铜粉和盐酸,Cu2+转化为CuCl,反应的离子方程式是__________ ,操作Ⅲ中包括对滤饼的醇洗,醇洗的目的是_________ 。
(6)CuCl在含有Cl-的溶液中存在平衡:CuCl+2Cl- [CuCl3]2-,加水稀释,Cl-浓度
[CuCl3]2-,加水稀释,Cl-浓度__________ (填写“变大”、“变小”或“”不变)。

(1)“滤渣”的主要成分为
(2)“还原”过程中Cu2+还原为CuCl,请写出反应的离子方程式:
(3)还原过程中加入的Na2SO3过量,目的是除去氧气防止CuCl被氧化,原理是
(4)CuCl在潮湿的环境中容易被氧化生成Cu2(OH)3Cl,反应化学方程式是
(5)CuCl粗品中含有Cu2+加入铜粉和盐酸,Cu2+转化为CuCl,反应的离子方程式是
(6)CuCl在含有Cl-的溶液中存在平衡:CuCl+2Cl-
 [CuCl3]2-,加水稀释,Cl-浓度
[CuCl3]2-,加水稀释,Cl-浓度
您最近一年使用:0次



