实验室模拟工业处理含铬废水,操作及现象如图1,反应过程中铬元素的化合价变化如图2,下列说法正确的是
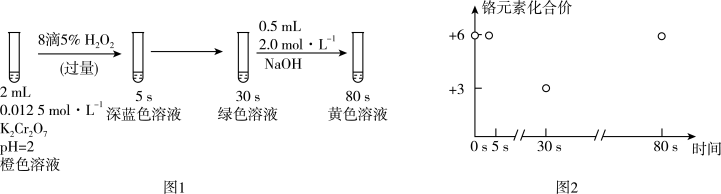
已知:深蓝色溶液中生成了CrO5

已知:深蓝色溶液中生成了CrO5
| A.实验开始至5s,铬元素被氧化 |
B.实验开始至30s,溶液中生成Cr3+的总反应离子方程式为: +3H2O2+8H+=2Cr3++7H2O+3O2↑ +3H2O2+8H+=2Cr3++7H2O+3O2↑ |
| C.30s至80s的过程,一定是氧气氧化了Cr3+ |
| D.80s时,溶液中又生成了Cr2O3,颜色相比于开始时浅,是水稀释所致 |
更新时间:2024-01-12 22:58:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写正确的是( )
| A.Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O32- + 6H+ =2S↓ +3H2O |
| B.向饱和Na2CO3溶液中通入过量CO2,CO32-+CO2+H2O═2HCO3- |
| C.CuSO4与过量浓氨水反应的离子方程式:Cu2++2NH3·H2O= Cu(OH)2↓+2NH4+ |
| D.Fe与稀硝酸反应,当n(Fe)∶n(HNO3)=1∶2时,3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列反应的离子方程式书写正确的是( )
A.氯化镁溶液与石灰乳反应: |
B.Na与 溶液反应: 溶液反应: |
C. 溶液中通入少量 溶液中通入少量 |
D.向氯化亚铁溶液中加入双氧水: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上以软锰矿(主要成分为 )为主要原料制备高锰酸钾(
)为主要原料制备高锰酸钾( )的方法如下:
)的方法如下:

已知:①熔烧时有 和KCl生成。
和KCl生成。
② 歧化法:调溶液pH至弱碱性,歧化生成
歧化法:调溶液pH至弱碱性,歧化生成 和
和
下列说法正确的是
 )为主要原料制备高锰酸钾(
)为主要原料制备高锰酸钾( )的方法如下:
)的方法如下:
已知:①熔烧时有
 和KCl生成。
和KCl生成。②
 歧化法:调溶液pH至弱碱性,歧化生成
歧化法:调溶液pH至弱碱性,歧化生成 和
和
下列说法正确的是
A.熔烧时所用坩埚的材质可以选用 |
B.熔烧时理论上每生成1 mol  转移 转移 个电子 个电子 |
C.电解法与 歧化法的理论产率之比为3:2 歧化法的理论产率之比为3:2 |
D.采用 歧化法时,可将滤液蒸发结晶得到 歧化法时,可将滤液蒸发结晶得到 固体 固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式书写正确的是
A. 与 与 的反应: 的反应: |
B.向 溶液中加入稀 溶液中加入稀 |
C.向 溶液中滴加 溶液中滴加 溶液: 溶液: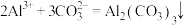 |
D.向 溶液中滴加足量 溶液中滴加足量 溶液: 溶液: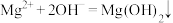 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在容积为2L的恒容密闭容器中,一定温度下,发生反应:aM(g)+bN(g)  cQ(g),气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是
cQ(g),气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是

 cQ(g),气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是
cQ(g),气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是
| A.该温度下此反应的平衡常数的值K=25/4 |
| B.平衡时,M的转化率为50℅,若条件改为恒温恒压,则达平衡时M的转化率小于50℅ |
| C.若开始时向容器中充入2molM和1molN,达到平衡时,M的体积分数小于50℅ |
| D.在5min时,再向体系中充入少量He,重新达到平衡前v(正)>V(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在较稀 溶液中,存在如下水解平衡:
溶液中,存在如下水解平衡: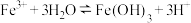 ,以下叙述不正确的是
,以下叙述不正确的是
 溶液中,存在如下水解平衡:
溶液中,存在如下水解平衡: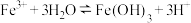 ,以下叙述不正确的是
,以下叙述不正确的是A.通入氯化氢气体, 数目增多,体系颜色变浅 数目增多,体系颜色变浅 |
| B.升温,平衡右移,体系颜色变深 |
C.加水, 数目增多,pH减小 数目增多,pH减小 |
D.加入 溶液,生成红褐色沉淀 溶液,生成红褐色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.中和热测定实验时,如果没有环形玻璃搅拌棒,可用环形铜质搅拌棒代替 |
B.向 酸性溶液中加入 酸性溶液中加入 草酸,溶液褪色速率先慢后快 草酸,溶液褪色速率先慢后快 |
| C.重铬酸钾溶液中滴加氢氧化钠,溶液由黄色变橙色 |
D.将装有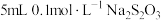 和 和 混合液的试管放入冷水中,溶液不会变浑浊 混合液的试管放入冷水中,溶液不会变浑浊 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实中不能用勒夏特列原理解释是
| A.由H2、I2(g)、HI(g)气体组成的平衡体系压缩体积后颜色变深 |
| B.实验室常用排饱和食盐水法收集氯气 |
| C.红棕色的NO2,加压后颜色先变深后变浅 |
D.工业制取金属钾[Na(l)+KCl(l) NaCl(l)+ K(g)]时,使K变成蒸气从混合体系中分离出来 NaCl(l)+ K(g)]时,使K变成蒸气从混合体系中分离出来 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定温度下,向2L的密闭容器中充入1mol 和3mol
和3mol 发生反应N2+3H2
发生反应N2+3H2 2NH3,5min时测得
2NH3,5min时测得 。下列说法正确的是
。下列说法正确的是
 和3mol
和3mol 发生反应N2+3H2
发生反应N2+3H2 2NH3,5min时测得
2NH3,5min时测得 。下列说法正确的是
。下列说法正确的是A.5min内, |
| B.适当升高温度可以使正反应速率和逆反应速率都加快 |
C.增大 的浓度可以使 的浓度可以使 完全反应 完全反应 |
D.5min时反应物与生成物的物质的量比为 |
您最近一年使用:0次

 溶液中加入金属钠:
溶液中加入金属钠:
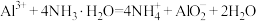
 :
:
 溶于
溶于 溶液中:
溶液中:
 通入亚硫酸钠溶液:
通入亚硫酸钠溶液: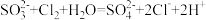

 溶液处理水垢中的
溶液处理水垢中的 :
:
 CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①恒容通入惰性气体 ②增加CO浓度 ③减压④恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①恒容通入惰性气体 ②增加CO浓度 ③减压④恒压通入惰性气体,能提高COCl2转化率的是( )

