解题方法
1 . 反应 I2(g)+H2(g) 2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)
2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)
(1)该温度下,该反应的化学平衡常数 K=___________ 。
(2)相同温度下,按以下初始浓度进行实验:
① 反应向__________ 方向(填“正反应”或者“逆反应”)进行,结合计算说明理由:___________ 。
②该反应达到平衡时,容器中c(HI)=___________ mmol•L-1,I2 的转化率是___________ 。
 2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)
2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)(1)该温度下,该反应的化学平衡常数 K=
(2)相同温度下,按以下初始浓度进行实验:
| 物质 | 初始浓度 |
| c(I2)/mmol•L-1 | 1.00 |
| c(H2)/mmol•L-1 | 1.00 |
| c(HI)/mmol•L-1 | 1.00 |
②该反应达到平衡时,容器中c(HI)=
您最近一年使用:0次
20-21高二上·全国·假期作业
2 . (1)合成氨工艺的一个重要工序是铜洗,其目的是用铜液(醋酸二氨合铜,氨水)吸收在生产过程中产生的CO和CO2等气体,铜液吸收CO的反应是放热反应,其反应的化学方程式如下:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac,如果要提高上述反应的反应速率,可以采取的措施是___________ (填字母)。
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+OH-⇌O2NC6H4COO-+C2H5OH,两种反应物的初始浓度均为0.050mol·L-1,15℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
列式计算该反应在120~180s与180~240s区间的平均反应速率___________ 、___________ ;比较两者大小可得出的结论是___________ 。
(3)反应AX3(g)+X2(g)⇌AX5(g)在容积为10L的密闭容器中进行,起始时AX3和X2均为0.2mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
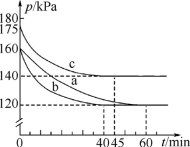
①列式计算实验a从反应开始至达到平衡时的反应速率v(AX5)=___________ 。
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为___________ (填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b___________ ,c___________ 。
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+OH-⇌O2NC6H4COO-+C2H5OH,两种反应物的初始浓度均为0.050mol·L-1,15℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| α/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
列式计算该反应在120~180s与180~240s区间的平均反应速率
(3)反应AX3(g)+X2(g)⇌AX5(g)在容积为10L的密闭容器中进行,起始时AX3和X2均为0.2mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

①列式计算实验a从反应开始至达到平衡时的反应速率v(AX5)=
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为
您最近一年使用:0次



