名校
1 . 合成氨是人类科学技术上的一项重大突破,其反应原理为: △H=-92.4kJ·L-1,一种工业合成氨的简易流程图如下:
△H=-92.4kJ·L-1,一种工业合成氨的简易流程图如下:
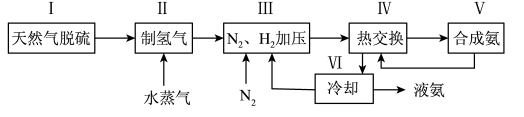
(1)步骤II中制氢气原理如下:
I.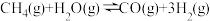 △H=+206.4kJ·L-1
△H=+206.4kJ·L-1
II. △H=-41.2kJ·L-1
△H=-41.2kJ·L-1
①对于反应I,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是____________________ 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
②利用反应II,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为_______________ 。
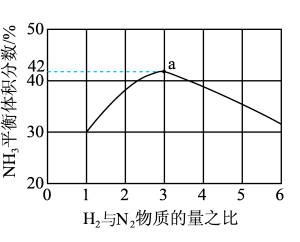
(2)图1表示500℃、60.0Mpa条件下,原料气投料比平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:________ 。
(3)上述流程图中,使合成氨气放出的能量得到充分利用的主要步骤是(填序号)________ 。简述本流程中提高合成氨原料总转化率的方法:_______________ 。
 △H=-92.4kJ·L-1,一种工业合成氨的简易流程图如下:
△H=-92.4kJ·L-1,一种工业合成氨的简易流程图如下:
(1)步骤II中制氢气原理如下:
I.
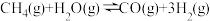 △H=+206.4kJ·L-1
△H=+206.4kJ·L-1II.
 △H=-41.2kJ·L-1
△H=-41.2kJ·L-1①对于反应I,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
②利用反应II,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为
(2)图1表示500℃、60.0Mpa条件下,原料气投料比平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:

(3)上述流程图中,使合成氨气放出的能量得到充分利用的主要步骤是(填序号)
您最近一年使用:0次



