名校
1 . 发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g)⇌CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H______ (填“增大”、“减小”或“不变”),判断的理由是________ 。
(2)CO2制备甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH=-49.0 kJ·mol-1,在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
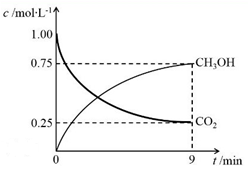
①该反应化学平衡常数K的表达式是____________________ 。
②0~9min时间内,该反应的平均反应速率ν(H2) =_______ 。
③在相同条件下,密闭容器的体积缩小至0.5 L时,此反应达平衡时放出的热量(Q)可能是________ (填字母序号)kJ。
a. 0< Q <29.5 b. 29.5< Q <36.75 c. 36.75< Q <49 d. 49< Q <98
④在一定条件下,体系中CO2的平衡转化率(α)与L和 X的关系如图所示,L和X分别表示温度或压强。
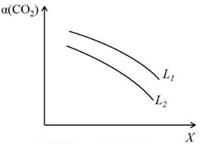
i. X表示的物理量是:_____________ 。
ii. 判断L1与L2的大小关系,并简述理由:_______________________ 。
(1)将煤转化成水煤气的反应:C(s)+H2O(g)⇌CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H
(2)CO2制备甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH=-49.0 kJ·mol-1,在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。

①该反应化学平衡常数K的表达式是
②0~9min时间内,该反应的平均反应速率ν(H2) =
③在相同条件下,密闭容器的体积缩小至0.5 L时,此反应达平衡时放出的热量(Q)可能是
a. 0< Q <29.5 b. 29.5< Q <36.75 c. 36.75< Q <49 d. 49< Q <98
④在一定条件下,体系中CO2的平衡转化率(α)与L和 X的关系如图所示,L和X分别表示温度或压强。

i. X表示的物理量是:
ii. 判断L1与L2的大小关系,并简述理由:
您最近一年使用:0次
2017-07-21更新
|
255次组卷
|
2卷引用:贵州省思南中学2016-2017学年高二下学期期末考试化学试题



