2011·上海虹口·二模
1 . 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。已知:SO2(g)+ O2(g)
O2(g) SO3(g)
SO3(g) +98kJ/mol
+98kJ/mol
(1)某温度下该反应的平衡常数K= ,若在此温度下,向100L的恒容密闭容器中,充入3.0molSO2(g)、16.0molO2(g)和3.0molSO3(g),则反应开始时v(正)
,若在此温度下,向100L的恒容密闭容器中,充入3.0molSO2(g)、16.0molO2(g)和3.0molSO3(g),则反应开始时v(正)__ v(逆)(填“<”、“>”或“=”)。
(2)一定温度下,向一带活塞的体积为20L的密闭容器中充入0.4molSO2和0.2molO2,达到平衡后体积变为16L,则平衡后SO2转化的百分率为__ 。
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是__ (填字母)。
A.保持温度和容器体积不变,充入0.2molO2
B.保持温度和容器内压强不变,充入0.4molSO3
C.降低温度
D.移动活塞压缩气体
(4)若以如图所示装置,用电化学原理生产硫酸,为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为__ 。

 O2(g)
O2(g) SO3(g)
SO3(g) +98kJ/mol
+98kJ/mol(1)某温度下该反应的平衡常数K=
 ,若在此温度下,向100L的恒容密闭容器中,充入3.0molSO2(g)、16.0molO2(g)和3.0molSO3(g),则反应开始时v(正)
,若在此温度下,向100L的恒容密闭容器中,充入3.0molSO2(g)、16.0molO2(g)和3.0molSO3(g),则反应开始时v(正)(2)一定温度下,向一带活塞的体积为20L的密闭容器中充入0.4molSO2和0.2molO2,达到平衡后体积变为16L,则平衡后SO2转化的百分率为
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是
A.保持温度和容器体积不变,充入0.2molO2
B.保持温度和容器内压强不变,充入0.4molSO3
C.降低温度
D.移动活塞压缩气体
(4)若以如图所示装置,用电化学原理生产硫酸,为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为

您最近一年使用:0次
2 . 含氮化合物在化学工业中有着重要的应用,回答下列问题:
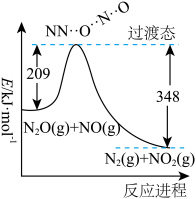
(1)由N2O和NO反应生成N2和NO2的能量变化(表示生成1molN2的能量变化)如图所示,该反应的热化学方程式为______________________ 。
(2)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________ ;若有1mol硝酸铵完全分解,则转移电子的数目为___________ (设NA为阿伏伽德罗常数的值)。
(3)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
①该反应在60~90s与90~120s内的平均反应速率分别约为___________ ,___________ ;比较两者大小可得出的结论是______________________ 。
②计算T℃时该反应的平衡常数为______________________ 。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________ (写出一条即可)。
(1)由N2O和NO反应生成N2和NO2的能量变化(表示生成1molN2的能量变化)如图所示,该反应的热化学方程式为

(2)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=
(3)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-
 O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。| t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
| a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
②计算T℃时该反应的平衡常数为
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为
您最近一年使用:0次



