名校
解题方法
1 . 研究化学反应中的能量变化对生产、生活有重要的意义。
(1)甲烷是一种高效清洁的新能源, 完全燃烧生成液态水时放出的热量为
完全燃烧生成液态水时放出的热量为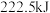 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(2)已知:


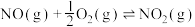


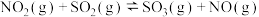


则
___________ (填含 、
、 的表达式),
的表达式),
___________ (填含 、
、 的表达式)。
的表达式)。
(3)已知: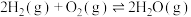
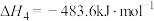 。查阅文献资料得部分化学键的键能如表所示:
。查阅文献资料得部分化学键的键能如表所示:
①合成氨反应 的活化能
的活化能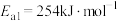 ,则氨分解反应
,则氨分解反应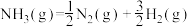 的活化能
的活化能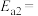
___________  。
。
②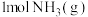 完全燃烧生成
完全燃烧生成 和水蒸气时放出
和水蒸气时放出___________ kJ的热量;又已知
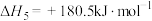 ,则氨催化氧化的热化学方程式为
,则氨催化氧化的热化学方程式为___________ 。
(4)研究氮氧化物与大气中悬浮的海盐粒子的相互作用时,涉及反应:

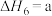
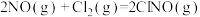
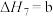
则反应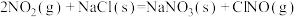 的
的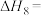
___________ (用含a、b的表达式表示)。
(1)甲烷是一种高效清洁的新能源,
 完全燃烧生成液态水时放出的热量为
完全燃烧生成液态水时放出的热量为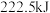 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)已知:



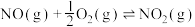


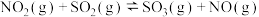


则

 、
、 的表达式),
的表达式),
 、
、 的表达式)。
的表达式)。(3)已知:
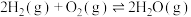
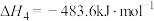 。查阅文献资料得部分化学键的键能如表所示:
。查阅文献资料得部分化学键的键能如表所示:| 化学键 | H—H |  | N—H |
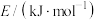 | 436 | 946 | 391 |
 的活化能
的活化能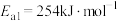 ,则氨分解反应
,则氨分解反应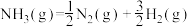 的活化能
的活化能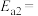
 。
。②
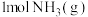 完全燃烧生成
完全燃烧生成 和水蒸气时放出
和水蒸气时放出
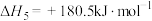 ,则氨催化氧化的热化学方程式为
,则氨催化氧化的热化学方程式为(4)研究氮氧化物与大气中悬浮的海盐粒子的相互作用时,涉及反应:

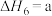
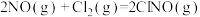
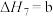
则反应
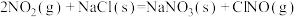 的
的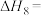
您最近一年使用:0次
2023-11-13更新
|
211次组卷
|
2卷引用:福建省泉州市2023-2024学年高二上学期期中考试化学试题
解题方法
2 . 回答下列问题:
(1)合成气(CO、H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。工业上用CO和H2合成CH3OH: △H。则该反应的平衡常数表达式为
△H。则该反应的平衡常数表达式为_______ ;
(2)测得不同温度下反应的平衡常数 如下表:
如下表:
下列说法错误的是_______。
(3)工业上,利用水煤气法制取合成气,其中发生的一步反应为:CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知
CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知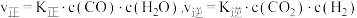 (k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数
(k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数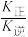 =
=_______ 。
(4)以天然气为原料生产合成气也有多种方法,其中Sparg工艺的原理为CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
①T℃下,该反应的平衡常数K=_______ 。
②实验1中,CO的平衡体积分数为_______ %(保留三位有效数字)。
③V1:V2=_______ 。
(1)合成气(CO、H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。工业上用CO和H2合成CH3OH:
 △H。则该反应的平衡常数表达式为
△H。则该反应的平衡常数表达式为(2)测得不同温度下反应的平衡常数
 如下表:
如下表:| 温度/℃ | T1 | 100 | T2 | 200 | 300 |
| 平衡常数K | 100 | 13 | 1 | 1.9×10-2 | 2.4×10-4 |
| A.△H<0 |
| B.该反应的ΔS<0 |
| C.T2时,某时刻1L容器中含0.1mol CO、0.2mol H2和0.3mol CH3OH,此时v正>v逆 |
| D.T1时,向1L密闭容器中投入0.1mol CO和0.2mol H2,平衡时CO转化率为50% |
 CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知
CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知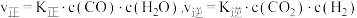 (k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数
(k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数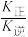 =
=(4)以天然气为原料生产合成气也有多种方法,其中Sparg工艺的原理为CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:| 实验编号 | 容器体积 | 物质浓度/mol·L-1 | ||
| CH4 | CO2 | CO | ||
| 1 | V1 | 0.02 | 0.02 | 0.10 |
| 2 | V2 | x | x | 0.05 |
②实验1中,CO的平衡体积分数为
③V1:V2=
您最近一年使用:0次
解题方法
3 . Bodensteins研究了反应:
 ,在716 K时,气体混合物中碘化氢的物质的量分数
,在716 K时,气体混合物中碘化氢的物质的量分数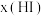 与反应时间t的关系如表所示:
与反应时间t的关系如表所示:
(1)根据上述实验结果,该反应的平衡常数K的计算式为_______ 。
(2)上述反应中,正反应速率 ,逆反应速率
,逆反应速率 ,其中
,其中 、
、 为正、逆反应速率常数,则
为正、逆反应速率常数,则 为
为_______ (用含K和 的代数式表示)。若起始时,
的代数式表示)。若起始时, ,
, ,则在
,则在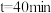 时,
时,
_______ 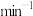 。
。

 ,在716 K时,气体混合物中碘化氢的物质的量分数
,在716 K时,气体混合物中碘化氢的物质的量分数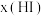 与反应时间t的关系如表所示:
与反应时间t的关系如表所示: | 0 | 20 | 40 | 60 | 80 | 120 |
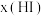 | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
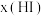 | 0 | 0.6 | 0.73 | 0.773 | 0.78 | 0.784 |
(2)上述反应中,正反应速率
 ,逆反应速率
,逆反应速率 ,其中
,其中 、
、 为正、逆反应速率常数,则
为正、逆反应速率常数,则 为
为 的代数式表示)。若起始时,
的代数式表示)。若起始时, ,
, ,则在
,则在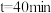 时,
时,
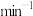 。
。
您最近一年使用:0次
2021-08-01更新
|
578次组卷
|
4卷引用:必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)
(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数及相关计算选择性必修1(SJ)专题2第二单元课时3 化学平衡常数平衡转化率2.2.3化学平衡常数 课后
名校
解题方法
4 . (1)下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
反应2H2(g)+O2(g)=2H2O(g)是__ (填“吸热”或“放热”)反应,这说明2molH2(g)和1mol O2(g)具有的能量比2mol H2O(g)具有的能量__ (填“高”或“低”)。
(2)氮及其化合物在工农业生产生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
已知:N2(g)+O2(g)=2NO(g) △H1 =+180.5 kJ/mol
C(s)+O2(g)=CO2(g) △H2=﹣393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H3=﹣221 kJ/mol
若某反应的平衡常数表达式为:K= ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:___ 。
(3)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,已知图中E1=134kJ·mol-1、E2=368kJ·mol-1,若在反应体系中加入催化剂,反应速率增大,E1的变化是__ (填“增大”“减小”或“不变”,下同),ΔH的变化是__ 。请写出NO2和CO反应的热化学方程式:__ 。

(4)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式:__ 。
| 物质 | H2(g) | O2(g) | H2O(g) |
| 能量 | 436 | 496 | 926 |
(2)氮及其化合物在工农业生产生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
已知:N2(g)+O2(g)=2NO(g) △H1 =+180.5 kJ/mol
C(s)+O2(g)=CO2(g) △H2=﹣393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H3=﹣221 kJ/mol
若某反应的平衡常数表达式为:K=
 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:(3)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,已知图中E1=134kJ·mol-1、E2=368kJ·mol-1,若在反应体系中加入催化剂,反应速率增大,E1的变化是

(4)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式:
您最近一年使用:0次
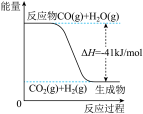
5 . 已知工业制氢气的反应为CO(g)+H2O(g)  CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
(1)增加H2O(g)的浓度,CO的转化率将________ (填“增大”、“减小”或“不变”)。
(2)平衡常数的表达式K=________ 。400 ℃时平衡常数K______ 9(填“>”、“<” 或“=”)。
(3)已知2H2(g)+O2(g) 2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:
2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:____ 。
 CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
(1)增加H2O(g)的浓度,CO的转化率将
(2)平衡常数的表达式K=
(3)已知2H2(g)+O2(g)
 2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:
2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:
您最近一年使用:0次
18-19高一下·陕西延安·期中
6 . 在2L的容器内,反应N2+3H2  2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:
2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:
(1)该反应的平衡常数表达式及平衡常数的值_________ ?
(2)此时间内,氮气、氢气、氨气的速率分别是多少_________ ?
 2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:
2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:(1)该反应的平衡常数表达式及平衡常数的值
(2)此时间内,氮气、氢气、氨气的速率分别是多少
您最近一年使用:0次
7 . (Ⅰ)已知在448 ℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为________ ;反应1/2H2(g)+1/2I2(g) HI(g)的平衡常数K3为
HI(g)的平衡常数K3为______________________________________ 。
(Ⅱ)在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________ 。
(2)该反应为________ (填“吸热”或“放热”)反应。
(3)能判断该反应达到化学平衡状态的依据是________ 。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。
(5)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,则下一时刻,反应将________ (填“正向”或“逆向”)进行。
 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为 HI(g)的平衡常数K3为
HI(g)的平衡常数K3为(Ⅱ)在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(5)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,则下一时刻,反应将
您最近一年使用:0次
2019-05-21更新
|
454次组卷
|
4卷引用:陕西省咸阳百灵中学2019-2020学年高二上学期期中考试化学(理)试题
陕西省咸阳百灵中学2019-2020学年高二上学期期中考试化学(理)试题湖北省汉川市第二中学2020-2021学年高二上学期期中考试化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡(已下线)2019年9月22日 《每日一题》选修4—— 每周一测
8 . 在一定温度下,10L密闭容器中加入5molSO2、4molO2,经10min后反应达平衡时有3molSO2发生了反应.试计算:
(1)用SO2表示该反应的反应速率为______ 。
(2)平衡时O2的转化率为______ 。
(3)平衡时O2在反应混合气中的物质的量分数______ 。
(4)平衡常数K值为______ 。
(1)用SO2表示该反应的反应速率为
(2)平衡时O2的转化率为
(3)平衡时O2在反应混合气中的物质的量分数
(4)平衡常数K值为
您最近一年使用:0次
名校
9 . 800K时,将0.1 mo A(g)和0.2 molB(g)充人体积为1 L的固定容积反应器中,发生如下反应:A(g)+2B(g)⇌2 C(g)+D(g),达到平衡时A的物质的量分数为20%。
(1)求达平衡时B的转化率α(B)___________ ;
(2)求该温度下的平衡常数K___________ ;
(3)若起始A的分压为10 kPa,求Kp___________ 。
(4)若在体积固定的某容器中充入0.2 mol A、0.1 mol B、0.1 mol C、0.5 mol D,则此时是否为平衡状态,请计算说明___________ 。
(1)求达平衡时B的转化率α(B)
(2)求该温度下的平衡常数K
(3)若起始A的分压为10 kPa,求Kp
(4)若在体积固定的某容器中充入0.2 mol A、0.1 mol B、0.1 mol C、0.5 mol D,则此时是否为平衡状态,请计算说明
您最近一年使用:0次
名校
10 . 在密闭恒温体积为V L的容器中充入2molCO和l0molH2O混合达到平衡时剩余0.5molCO。CO (g)+H2O(g)  CO2(g) +H2(g)。计算:
CO2(g) +H2(g)。计算:
(1)H2O的平衡转化率。
(2)该温度下的化学平衡常数。
(3)恒温条件下,若在该容器中再充入1.5molCO与1.5mol H2,则平衡如何移动?
 CO2(g) +H2(g)。计算:
CO2(g) +H2(g)。计算:(1)H2O的平衡转化率。
(2)该温度下的化学平衡常数。
(3)恒温条件下,若在该容器中再充入1.5molCO与1.5mol H2,则平衡如何移动?
您最近一年使用:0次



