在密闭恒温体积为V L的容器中充入2molCO和l0molH2O混合达到平衡时剩余0.5molCO。CO (g)+H2O(g)  CO2(g) +H2(g)。计算:
CO2(g) +H2(g)。计算:
(1)H2O的平衡转化率。
(2)该温度下的化学平衡常数。
(3)恒温条件下,若在该容器中再充入1.5molCO与1.5mol H2,则平衡如何移动?
 CO2(g) +H2(g)。计算:
CO2(g) +H2(g)。计算:(1)H2O的平衡转化率。
(2)该温度下的化学平衡常数。
(3)恒温条件下,若在该容器中再充入1.5molCO与1.5mol H2,则平衡如何移动?
更新时间:2017-11-27 17:31:22
|
相似题推荐
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】研究化学反应中的能量变化对生产、生活有重要的意义。
(1)甲烷是一种高效清洁的新能源, 完全燃烧生成液态水时放出的热量为
完全燃烧生成液态水时放出的热量为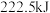 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(2)已知:


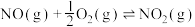


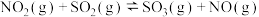


则
___________ (填含 、
、 的表达式),
的表达式),
___________ (填含 、
、 的表达式)。
的表达式)。
(3)已知: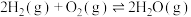
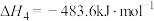 。查阅文献资料得部分化学键的键能如表所示:
。查阅文献资料得部分化学键的键能如表所示:
①合成氨反应 的活化能
的活化能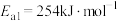 ,则氨分解反应
,则氨分解反应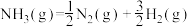 的活化能
的活化能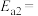
___________  。
。
②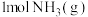 完全燃烧生成
完全燃烧生成 和水蒸气时放出
和水蒸气时放出___________ kJ的热量;又已知
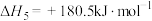 ,则氨催化氧化的热化学方程式为
,则氨催化氧化的热化学方程式为___________ 。
(4)研究氮氧化物与大气中悬浮的海盐粒子的相互作用时,涉及反应:

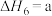
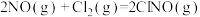
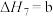
则反应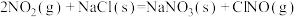 的
的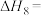
___________ (用含a、b的表达式表示)。
(1)甲烷是一种高效清洁的新能源,
 完全燃烧生成液态水时放出的热量为
完全燃烧生成液态水时放出的热量为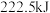 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)已知:



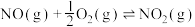


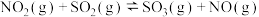


则

 、
、 的表达式),
的表达式),
 、
、 的表达式)。
的表达式)。(3)已知:
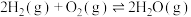
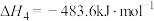 。查阅文献资料得部分化学键的键能如表所示:
。查阅文献资料得部分化学键的键能如表所示:| 化学键 | H—H |  | N—H |
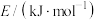 | 436 | 946 | 391 |
 的活化能
的活化能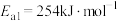 ,则氨分解反应
,则氨分解反应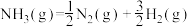 的活化能
的活化能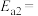
 。
。②
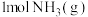 完全燃烧生成
完全燃烧生成 和水蒸气时放出
和水蒸气时放出
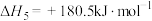 ,则氨催化氧化的热化学方程式为
,则氨催化氧化的热化学方程式为(4)研究氮氧化物与大气中悬浮的海盐粒子的相互作用时,涉及反应:

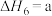
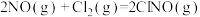
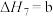
则反应
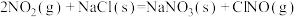 的
的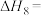
您最近一年使用:0次
【推荐2】完成下列问题
(1)已知C(s)+O2(g)=CO2(g)△H1=﹣393.5kJ/mol,
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ/mol,
C(s)+ O2(g)=CO(g)△H3=akJ/mol,则a=
O2(g)=CO(g)△H3=akJ/mol,则a=________ 。
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上常采用下列反应合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)△H1,下表所列数据是反应在不同温度下的化学平衡常数(K)
由表中数据判断△H1________ 0 (填“>”、“=”或“<”)。某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为________ ,此时的温度为________ (从上表中选择)。
(1)已知C(s)+O2(g)=CO2(g)△H1=﹣393.5kJ/mol,
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ/mol,
C(s)+
 O2(g)=CO(g)△H3=akJ/mol,则a=
O2(g)=CO(g)△H3=akJ/mol,则a=(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上常采用下列反应合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)△H1,下表所列数据是反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断△H1
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式:_______ 。
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g) 2NH3(g) ΔH=a kJ·mol-1,试根据表中所列键能数据估算a的数值:
2NH3(g) ΔH=a kJ·mol-1,试根据表中所列键能数据估算a的数值:_______ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599 kJ·mol-1③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:_______ 。
(1)实验测得,5 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式:
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g)
 2NH3(g) ΔH=a kJ·mol-1,试根据表中所列键能数据估算a的数值:
2NH3(g) ΔH=a kJ·mol-1,试根据表中所列键能数据估算a的数值:| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599 kJ·mol-1③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】已知一氧化碳与水蒸气的反应为
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
在密闭容器中,将1.0mol CO与3.6mol H2O混合加热到434℃,在434℃的平衡常数K1=9,
我们跟踪测定H2O的物质的量浓度,
如图所示:
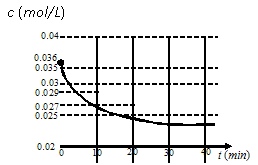
则0~20min的反应速率是 从434℃升温至800℃,800℃的平衡常数K2=1,则正反应为_____________(填“放热反应”或“吸热反应”或“不能确定”)。
求800℃平衡时CO转化为CO2的转化率(写出必要的计算过程)。
CO(g)+H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)在密闭容器中,将1.0mol CO与3.6mol H2O混合加热到434℃,在434℃的平衡常数K1=9,
我们跟踪测定H2O的物质的量浓度,
如图所示:

则0~20min的反应速率是 从434℃升温至800℃,800℃的平衡常数K2=1,则正反应为_____________(填“放热反应”或“吸热反应”或“不能确定”)。
求800℃平衡时CO转化为CO2的转化率(写出必要的计算过程)。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH
2Fe(s)+3CO2(g) ΔH
(1)已知:① Fe2O3(s)+ 3C(石墨)=2Fe(s)+3CO(g) ΔH1 ②C(石墨)+CO2(g)=2CO(g) ΔH2,则ΔH=______ (用含ΔH1、ΔH2代数式表示)
(2)高炉炼铁反应的平衡常数表达式K=_____________ 。
(3)在T℃时,该反应的平衡常数K=64,在 2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
①甲容器中CO的平衡转化率为______ 。
②下列说法正确的是______ 。
A. 若容器压强恒定,反应达到平衡状态 B. 若容器内气体密度恒定,反应达平衡
C. 甲容器中CO的平衡转化率大于乙的 D. 增加Fe2O3就能提高CO的转化率
 2Fe(s)+3CO2(g) ΔH
2Fe(s)+3CO2(g) ΔH (1)已知:① Fe2O3(s)+ 3C(石墨)=2Fe(s)+3CO(g) ΔH1 ②C(石墨)+CO2(g)=2CO(g) ΔH2,则ΔH=
(2)高炉炼铁反应的平衡常数表达式K=
(3)在T℃时,该反应的平衡常数K=64,在 2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
①甲容器中CO的平衡转化率为
②下列说法正确的是
A. 若容器压强恒定,反应达到平衡状态 B. 若容器内气体密度恒定,反应达平衡
C. 甲容器中CO的平衡转化率大于乙的 D. 增加Fe2O3就能提高CO的转化率
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】吸热反应N2(g)+O2(g) 2NO(g),在2000℃时,K=6.2×10-4。2000℃时,在10L密闭容器内放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2,通过计算回答:
2NO(g),在2000℃时,K=6.2×10-4。2000℃时,在10L密闭容器内放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2,通过计算回答:
(1)此反应的初始状态是否为化学平衡状态?
(2)若非化学平衡状态,反应将向哪个方向进行?
 2NO(g),在2000℃时,K=6.2×10-4。2000℃时,在10L密闭容器内放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2,通过计算回答:
2NO(g),在2000℃时,K=6.2×10-4。2000℃时,在10L密闭容器内放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2,通过计算回答:(1)此反应的初始状态是否为化学平衡状态?
(2)若非化学平衡状态,反应将向哪个方向进行?
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】在一定条件下,反应 的平衡常数为0.5,在体积为1L的容器中,已知CO(g)、
的平衡常数为0.5,在体积为1L的容器中,已知CO(g)、 的起始浓度分别为
的起始浓度分别为 、
、 ,反应达到平衡后再改变下列条件,通过计算判断平衡移动的方向。
,反应达到平衡后再改变下列条件,通过计算判断平衡移动的方向。
(1)保持体积不变,通入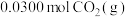 ;
;_______
(2)保持体积不变,通入CO(g)和 各0.0400 mol;
各0.0400 mol;_______
(3)保持温度不变,将容器体积扩大为原来的2倍。_______
 的平衡常数为0.5,在体积为1L的容器中,已知CO(g)、
的平衡常数为0.5,在体积为1L的容器中,已知CO(g)、 的起始浓度分别为
的起始浓度分别为 、
、 ,反应达到平衡后再改变下列条件,通过计算判断平衡移动的方向。
,反应达到平衡后再改变下列条件,通过计算判断平衡移动的方向。(1)保持体积不变,通入
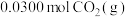 ;
;(2)保持体积不变,通入CO(g)和
 各0.0400 mol;
各0.0400 mol;(3)保持温度不变,将容器体积扩大为原来的2倍。
您最近一年使用:0次


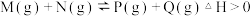 ,请回答下列问题:
,请回答下列问题: ,
,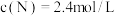 ;达到平衡后,M的转化率为
;达到平衡后,M的转化率为 ,求此时N的转化率
,求此时N的转化率 ,
,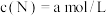 ,达到平衡后,
,达到平衡后,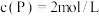 ,求a的值
,求a的值

