1 . 下列实验操作能完成相应实验目的的是
| 实验目的 | 实验操作 | |
| A | 验证碳与浓硫酸反应的产物 和 和 | 将气体依次通入澄清石灰水和品红溶液 |
| B | 比较四羟基合铝酸的 和碳酸的 和碳酸的 | 向四羟基合铝酸钠溶液中滴加碳酸氢钠 |
| C | 比较O-H…O和F-H…F的氢键键能大小 | 同温同压下,测定 和HF的沸点 和HF的沸点 |
| D | 检验 中是否含有碳碳双键 中是否含有碳碳双键 | 向 中加入少量溴水 中加入少量溴水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 硫及其化合物在日常生活、工业生产中都非常普遍。
(1)SO2、H2S都是常见的污染性气体,具有一定的毒性。请再写出两种与酸雨、光化学烟雾和臭氧层空洞均有关的污染性气体:___________ 。
(2)变废为宝是治理污染的常用手段。以V2O5为催化剂,将SO2氧化为SO3,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
(i)SO2(g)+V2O5(s) SO3(g)+V2O4(s),活化能为Ea1。
SO3(g)+V2O4(s),活化能为Ea1。
(ii)2V2O4(s)+O2(g) 2V2O5(s),活化能为Ea2。
2V2O5(s),活化能为Ea2。
能量变化如图所示。

总反应2SO2(g)+O2(g) 2SO3(g)的
2SO3(g)的
___________ kJ∙mol−1 (用E1~E5中的合理数据组成的代数式表示)。决定SO2催化氧化的总反应速率的是步骤___________ (填(i)或(ii)),其活化能为___________ kJ∙mol−1 (用E1~E5中的合理数据组成的代数式表示)。
(3)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++ ,
,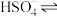 H++
H++ 。
。
①25℃时,Na2SO4溶液的pH___________ (填“>”“<”或“=”)7。
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数___________ (写出计算过程,结果保留三位有效数字)。
(4)液态水中,水存在自偶电离:H2O+H2O H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为___________ 。
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是___________ 。若保持温度不变,关于该所得溶液,下列说法正确的是___________ 。
A.加入少量冰醋酸,c( )与c(
)与c( )均减小
)均减小
B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c( )与c(
)与c( )的比值减小
)的比值减小
D.加入少量Na2SO4固体,c(Ac-)减小
(1)SO2、H2S都是常见的污染性气体,具有一定的毒性。请再写出两种与酸雨、光化学烟雾和臭氧层空洞均有关的污染性气体:
(2)变废为宝是治理污染的常用手段。以V2O5为催化剂,将SO2氧化为SO3,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
(i)SO2(g)+V2O5(s)
 SO3(g)+V2O4(s),活化能为Ea1。
SO3(g)+V2O4(s),活化能为Ea1。(ii)2V2O4(s)+O2(g)
 2V2O5(s),活化能为Ea2。
2V2O5(s),活化能为Ea2。能量变化如图所示。

总反应2SO2(g)+O2(g)
 2SO3(g)的
2SO3(g)的
(3)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++
 ,
,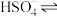 H++
H++ 。
。①25℃时,Na2SO4溶液的pH
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数
(4)液态水中,水存在自偶电离:H2O+H2O
 H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是
A.加入少量冰醋酸,c(
 )与c(
)与c( )均减小
)均减小B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c(
 )与c(
)与c( )的比值减小
)的比值减小D.加入少量Na2SO4固体,c(Ac-)减小
您最近一年使用:0次
2023-04-06更新
|
849次组卷
|
3卷引用:广东省汕头市金山中学2023届高三下学期一模化学试题
3 . 下列实验操作、现象及结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向菠菜汁中加入少量稀硝酸,再滴入几滴KSCN溶液 | 溶液变红 | 菠菜汁中含有Fe3+ |
| B | 将在酒精灯上灼烧后的铜丝迅速插入乙醇中 | 铜丝表面由黑色变为红色 | 乙醇具有还原性 |
| C | 相同温度下,用pH计分别测定0.010 mol/LHF溶液和0.010 mol/L CH3COOH溶液的pH | HF溶液pH更小 | Ka(HF)<Ka(CH3COOH) |
| D | 向0.01 mol/L FeCl3溶液中,加入少量FeCl3固体 | 溶液颜色加深 | Fe3+水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021·山东·模拟预测
名校
4 . 铬酸钠(Na2CrO4)水溶液中存在如下平衡:2H++2 ⇌2
⇌2 ⇌
⇌ +H2O,在1.00mol·L−1铬酸钠溶液中,各种含铬离子的分布分数与pH关系如图所示。
+H2O,在1.00mol·L−1铬酸钠溶液中,各种含铬离子的分布分数与pH关系如图所示。
 ⇌2
⇌2 ⇌
⇌ +H2O,在1.00mol·L−1铬酸钠溶液中,各种含铬离子的分布分数与pH关系如图所示。
+H2O,在1.00mol·L−1铬酸钠溶液中,各种含铬离子的分布分数与pH关系如图所示。
A.Na2CrO4溶液中, 发生水解而使溶液呈碱性 发生水解而使溶液呈碱性 |
| B.铬酸(H2CrO4)第二步电离电离常数Ka2=10−6.4 |
| C.要得到纯度较高的Na2CrO4溶液,应控制pH>9 |
D.pH=6时,Na2CrO4溶液中存在:c(Na+)=2c( )+2c( )+2c( )+2c( )+2c( ) ) |
您最近一年使用:0次
2021-05-14更新
|
546次组卷
|
5卷引用:化学-学科网2021年高三5月大联考(山东卷)
(已下线)化学-学科网2021年高三5月大联考(山东卷)(已下线)化学-学科网2021年高三5月大联考(广东卷)西藏林芝市第一中学2020-2021学年高三上学期第四次月考化学试题第三章 综合拔高练江苏省无锡市江阴市三校联考2023-2024学年高二下学期4月期中联考化学试题



