名校
解题方法
1 . 经测定某溶液中离子只有Na+、Ac-、H+、OH―四种,且离子浓度大小的排列顺序为:c(Ac-)>c(Na+)>c(H+)>c(OH-)。其可能的情形是
| A.该溶液由pH=3的HAc与pH=11的NaOH溶液等体积混合而成 |
| B.0.2mol/L的HAc溶液与0.1mol/L的NaOH溶液等体积混合 |
| C.在上述溶液中加入适量NaOH,可能使溶液中离子浓度大小改变为:c(Ac-)>c(Na+) >c(OH-) >c(H+) |
| D.该溶液由0.1mol/L的HAc溶液与等物质的量浓度等体积的NaOH溶液混合而成 |
您最近一年使用:0次
2021-08-07更新
|
250次组卷
|
2卷引用:第19届(2005年)全国高中学生化学竞赛(江苏赛区)预赛试题
解题方法
2 . 由下列实验操作和现象所得到的结论正确的是
| 实验操作和现象 | 结论 | |
| A | 向某溶液中滴加几滴新制氯水,再滴加少量 溶液,溶液变红 溶液,溶液变红 | 溶液中含有 |
| B | 室温下,测得相同浓度的 和 和 溶液的pH分别为8和9 溶液的pH分别为8和9 | 酸性: |
| C | 蔗糖溶液中加入少量稀硫酸,水浴加热 ,加氢氧化钠溶液至溶液呈碱性,再加入少量新制 ,加氢氧化钠溶液至溶液呈碱性,再加入少量新制 ,继续加热 ,继续加热 ,生成砖红色沉淀 ,生成砖红色沉淀 | 蔗糖完全水解 |
| D | 向等体积等浓度的稀硫酸中分别加入少量等物质的量的 和 和 固体, 固体, 溶解而 溶解而 不溶解 不溶解 | 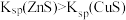 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 向含Na2CO3、Na[Al(OH)4](NaAlO2)的混合溶液中逐滴加入150mL1mol·L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )
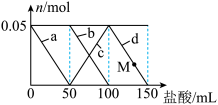

| A.a曲线表示的离子方程式为:[Al(OH)4]-+H+=Al(OH)3↓+H2O |
| B.b和c曲线表示的离子反应是不相同的 |
| C.M点时,溶液中沉淀的质量为3.9g |
D.原混合溶液中的CO 与[Al(OH)4]-的物质的量之比为1∶2 与[Al(OH)4]-的物质的量之比为1∶2 |
您最近一年使用:0次
解题方法
4 . 下列实验方案的设计能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 向苯与液溴的混合液中加入铁粉,将产生的气体直接通入AgNO3溶液中 | 验证液溴与萃发生取代反应 |
| B | 比较HF与HClO的酸性强弱 | 常温下,用pH试纸分别测定浓度均为0.1 mol·L-1的NaF溶液和NaClO溶液的pH |
| C | 验证FeCl3与KI的反应是可逆反应 | 向1 mL0.1 mol·L-1FeCl3溶液中滴加5 mL0.1 mol·L-1 KI溶液充分反应后,取少许混合液滴加KSCN溶液 |
| D | 除去NaCl固体表面的少量KCl杂质 | 用饱和NaCl溶液洗涤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列叙述正确的是
| A.KSp[MgF2]>KSp[Mg(OH)2],不能实现Mg(OH)2转化为MgF2。 |
| B.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大 |
| D.FeCl3与KSCN反应达到平衡时,加入KCl溶液,则溶液颜色变深 |
您最近一年使用:0次



